
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
次氯酸的酸性不强,却有很强的氧化性、漂白性,次氯酸的氧化性凭什么比高氯酸的强?
我们从一下几点来分析:
1. 化合价与原子的有效核电荷
在含氧酸中,中心原子(这里是氯原子)的化合价会影响其对电子的吸引能力,但需结合分子结构综合判断。
• 次氯酸中,氯为 + 1价;高氯酸中,氯为 + 7价。从化合价看,高氯酸中氯的正电性更强,似乎更易得到电子(表现氧化性),但实际并非如此,因为在这里,分子结构对氧化性的影响超过了中心原子化合价的影响。
• 次氯酸中的氯原子周围的电子云密度相对较高,且氧原子的孤电子对与氯原子的相互作用,使得氯原子的有效核电荷对“外来电子”的吸引力在反应中更具优势;而高氯酸中,氯原子与多个氧原子形成共价键,电子云分散,且分子整体更稳定,不易发生氧化还原反应。
2.从空间构型角度
物质的氧化性强弱,不仅取决于得电子的倾向,还与自身被还原时的难易程度(即分子的稳定性)有关。
次氯酸的分子结构为H - O - Cl,其中氯原子直接与氧原子相连,且次氯酸分子不稳定,容易发生分解,在分解过程中氯原子更容易获得电子,表现出强氧化性。
•高氯酸根结构非常稳定,空间构型为正四面体,对称性高,键能大,要使高氯酸中的氯从 + 7价被还原,需要克服较大的能量障碍,因此高氯酸的氧化性反而较弱(只有在浓热等极端条件下才表现出强氧化性)。
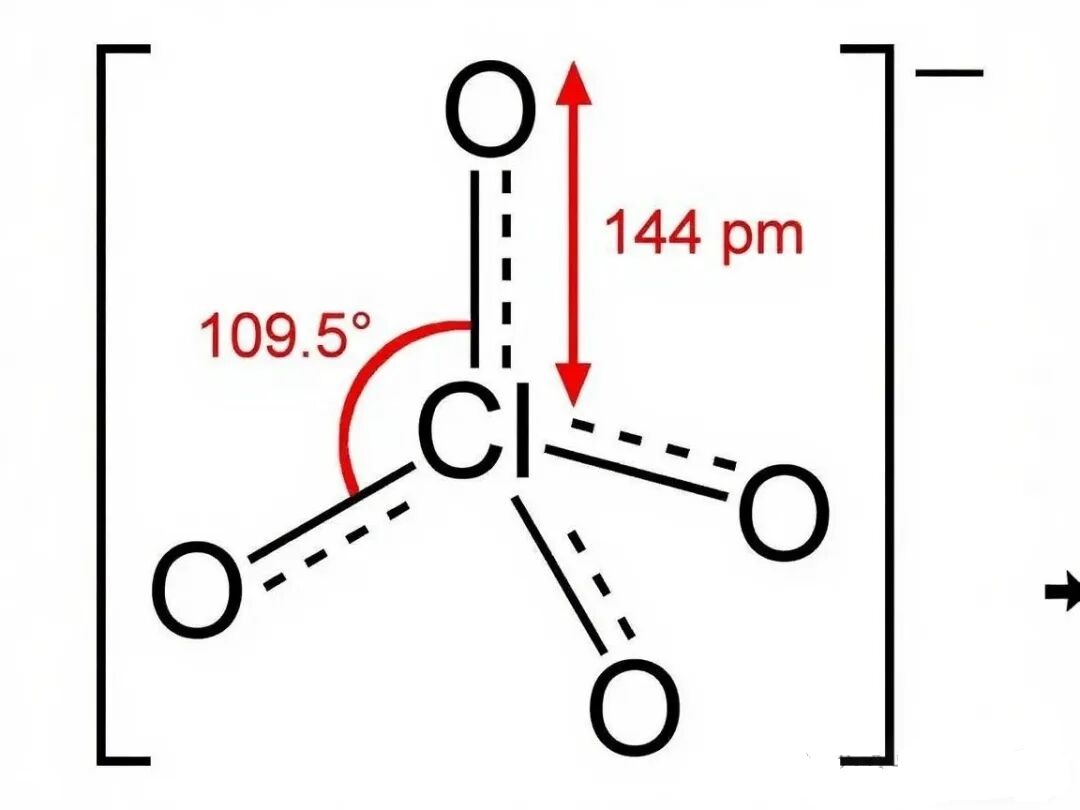
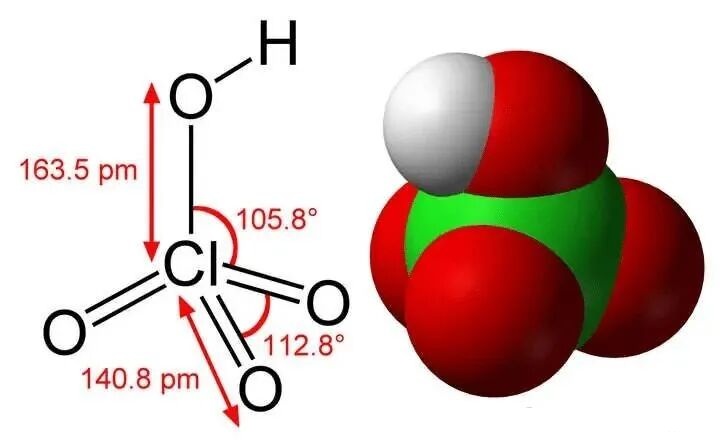
综上,次氯酸氧化性强于高氯酸,是因为次氯酸分子结构不稳定,氯原子更易被还原,而高氯酸分子稳定,难以表现出强氧化性。也就是说,在这里空间结构比中心原子化合价对氧化性的影响更大。而在硫酸比亚硫酸的氧化性强,中心原子化合价又占主导。
这正是变化观念和平衡思想的一个体现。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
HF、HCl、HBr、HI的水溶液分别叫氢氟酸、氢氯酸(盐酸)、氢溴酸、...
次氯酸的酸性不强,却有很强的氧化性、漂白性,次氯酸的氧化...
一、HNO 3 为什么不能氧化Cl - ? 硝酸HNO 3 是强氧化剂,Cl - 氯...
氢氟酸是一弱酸(298K时,Ka=3.5×10 -4 )。与其它弱酸相同,浓度越...
卤素是很活泼的非金属元素。单质最典型的化学性质是强氧化性...
F Cl Br I ,卤素,第 Ⅶ A 族, 价电子构型 ns 2 np 5 虽然是同一族...