
|
学习小专题 |

|
学习小专题 |
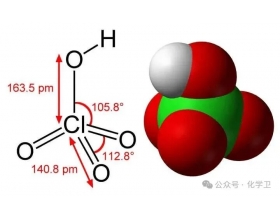 [探讨与扩展8] 次氯酸的氧化性凭什么比高氯酸的强? 作者:化学自习室 来源:未知 日期:2025-08-31 09:53:40 点击:1423 所属专题:
[探讨与扩展8] 次氯酸的氧化性凭什么比高氯酸的强? 作者:化学自习室 来源:未知 日期:2025-08-31 09:53:40 点击:1423 所属专题:
次氯酸的酸性不强,却有很强的氧化性、漂白性,次氯酸的氧化性凭什么比高氯酸的强? 我们从一下几点来分析: 1. 化合价 与原子的有效核电荷 在含氧酸中,中心原子(这里是氯原子)的化合价会影响其对电子的吸引能力,但需结合分子结构综合判断。 次氯酸中,氯为 + 1价;...
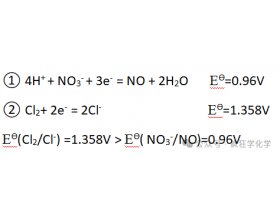 [探讨与扩展8] 硝酸为什么不能氧化氯离子?而酸性高锰酸钾却可以氧化氯离子? 作者:化学自习室 来源:未知 日期:2025-07-08 18:32:40 点击:1072 所属专题:氯离子
[探讨与扩展8] 硝酸为什么不能氧化氯离子?而酸性高锰酸钾却可以氧化氯离子? 作者:化学自习室 来源:未知 日期:2025-07-08 18:32:40 点击:1072 所属专题:氯离子
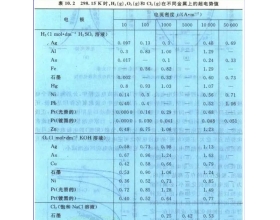
一、HNO 3 为什么不能氧化Cl - ? 硝酸HNO 3 是强氧化剂,Cl - 氯离子是还原剂,但是我们知道硝酸HNO 3 不能氧化Cl - 氯离子,可以说硝酸HNO 3 的氧化性不够强,也可以说Cl - 的还原性还不够强。那么酸性KMnO 4 为什么可以氧化Cl - ?下面我们通过电极电势来说明原...
 [探讨与扩展8] 卤素单质与金属单质的反应 作者:化学自习室 来源:未知 日期:2024-09-18 11:07:35 点击:1603 所属专题:卤素单质
[探讨与扩展8] 卤素单质与金属单质的反应 作者:化学自习室 来源:未知 日期:2024-09-18 11:07:35 点击:1603 所属专题:卤素单质
卤素是很活泼的非金属元素。单质最典型的化学性质是强氧化性,卤素单质氧化性递变规律为: F2Cl2Br2I2。 (1)卤素与金属作用 氟能与所有的金属直接作用,反应非常猛烈,生成高氧化态氟化物: 如CoF3、VF5、BiF5等。在室温或不太高的温度下,氟可以使镁、铁、镍、铜、铅...
 [探讨与扩展8] 氟离子为什么有很强的腐蚀性 作者:化学自习室 来源:未知 日期:2024-08-23 16:48:31 点击:1335 所属专题:氟化物
[探讨与扩展8] 氟离子为什么有很强的腐蚀性 作者:化学自习室 来源:未知 日期:2024-08-23 16:48:31 点击:1335 所属专题:氟化物
氢氟酸中的氟离子的半径很小,甚至小于氧离子,这导致它有很强的渗透性,致密的氧化物也不能阻止它的渗透, 氟离子(F-)具有极强的腐蚀性,主要原因如下: 高电负性 氟是所有元素中电负性最高的元素,其电负性值为3.98。高电负性使得氟离子能够强烈吸引其他原子中的电...
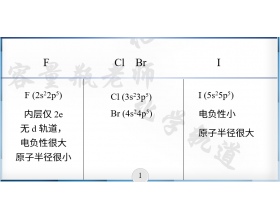 [探讨与扩展8] 氟的成键特点及特殊性 作者:化学自习室 来源:未知 日期:2024-08-19 17:28:42 点击:1527 所属专题:氟元素
[探讨与扩展8] 氟的成键特点及特殊性 作者:化学自习室 来源:未知 日期:2024-08-19 17:28:42 点击:1527 所属专题:氟元素
F Cl Br I ,卤素,第 Ⅶ A 族, 价电子构型 ns 2 np 5 虽然是同一族,价电子构型相同,都是非金属元素,最常见的 氧化数 都是 -1 但是, 还真得分开来说。 因为, F 是个特殊元素。 Cl 和 Br 更相似, I 相对它们来说也有点个性(半径大,电负性小) 今天先来说说 F 的...
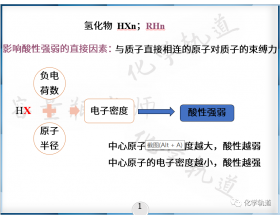 [探讨与扩展8] 非金属氢化物的酸性变化规律 作者:化学自习室 来源:未知 日期:2022-03-25 10:24:48 点击:1781 所属专题:氢化物 酸性
[探讨与扩展8] 非金属氢化物的酸性变化规律 作者:化学自习室 来源:未知 日期:2022-03-25 10:24:48 点击:1781 所属专题:氢化物 酸性
以酸碱电离理论的角度看,大多数非金属氢化物溶于水并且显酸性,例如 HCl ,也有显碱性的,例如 NH 3 ,但是像 CH 4 不溶于水, SiH 4 水解。 放 宽眼界 ,以酸碱质子理论的角度不再局限于水溶液中,能解离出质子的都是酸,所以非金属氢化物都可以看做是酸,强弱不同的...
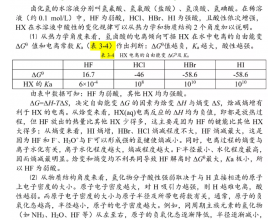 [探讨与扩展8] HF、HCl、HBr、HI水溶液的酸性为什么依次增强? 作者:岳文虹 来源:追寻化学教育的本源 日期:2021-05-25 08:17:34 点击:1415 所属专题:氢卤酸
[探讨与扩展8] HF、HCl、HBr、HI水溶液的酸性为什么依次增强? 作者:岳文虹 来源:追寻化学教育的本源 日期:2021-05-25 08:17:34 点击:1415 所属专题:氢卤酸
...
 [探讨与扩展8] 氧化性:氧和氯谁强? 作者:化学自习室 来源:未知 日期:2021-03-02 09:25:19 点击:6450 所属专题:氧化性 氯气
[探讨与扩展8] 氧化性:氧和氯谁强? 作者:化学自习室 来源:未知 日期:2021-03-02 09:25:19 点击:6450 所属专题:氧化性 氯气
这是一个老生常谈的话题,小编觉得这个问题值得拿来讲的原因有几个: 1 、题目中出现 O 2 、 Cl 2 的频率高 2 、 O 、 Cl 元素的电负性和单质的氧化性不一致 一、电负性比较 选修三 P 19 电负性数据为: O 为 3.5 , Cl 为 3.0 ,因此氧原子的氧化性大于氯原子是毋庸置...
 [探讨与扩展8] 为什么次氯酸钙与少量二氧化碳反应生成碳酸钙沉淀? 作者:化学自习室 来源:未知 日期:2021-02-25 15:20:29 点击:9141 所属专题:二氧化碳与次氯酸盐
[探讨与扩展8] 为什么次氯酸钙与少量二氧化碳反应生成碳酸钙沉淀? 作者:化学自习室 来源:未知 日期:2021-02-25 15:20:29 点击:9141 所属专题:二氧化碳与次氯酸盐
因为碳酸氢钙在水溶液中是不能高浓度存在的,浓度稍高就会分解为碳酸钙、二氧化碳和水。 如果是次氯酸钠溶液与二氧化碳的反应,主要反应确实是: NaClO + H 2 O + CO 2 = NaHCO 3 + HClO 反应生成物之一是碳酸氢钠的原因,确实是因为次氯酸的酸性强于碳酸氢根离子,这与...
 [探讨与扩展8] 次氯酸的氧化性真的比高氯酸强吗 作者:化学自习室 来源:未知 日期:2020-01-18 10:15:05 点击:4810 所属专题:次氯酸
[探讨与扩展8] 次氯酸的氧化性真的比高氯酸强吗 作者:化学自习室 来源:未知 日期:2020-01-18 10:15:05 点击:4810 所属专题:次氯酸
在现有化学类教材中一般认为次氯酸的氧化性强于高氯酸,从标准电极电势数据来看次氯酸的电极电势大于高氯酸的电极电势,然而事实真的如表面看上去一样、是毋庸置疑的吗? 为了比较的公平起见,我们假设存在两溶液(温度均为 298K):一个是 0.500mol/L的新鲜次氯酸溶液,...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
HF、HCl、HBr、HI的水溶液分别叫氢氟酸、氢氯酸(盐酸)、氢溴酸、...
次氯酸的酸性不强,却有很强的氧化性、漂白性,次氯酸的氧化...
一、HNO 3 为什么不能氧化Cl - ? 硝酸HNO 3 是强氧化剂,Cl - 氯...
氢氟酸是一弱酸(298K时,Ka=3.5×10 -4 )。与其它弱酸相同,浓度越...
卤素是很活泼的非金属元素。单质最典型的化学性质是强氧化性...
F Cl Br I ,卤素,第 Ⅶ A 族, 价电子构型 ns 2 np 5 虽然是同一族...
一、 卤素互化物 不同卤素原子之间相互形成的化合物称为卤素...
漂白粉 具有漂白作用的有效成分为次氯酸钙Ca(ClO)2的漂白剂。...