
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
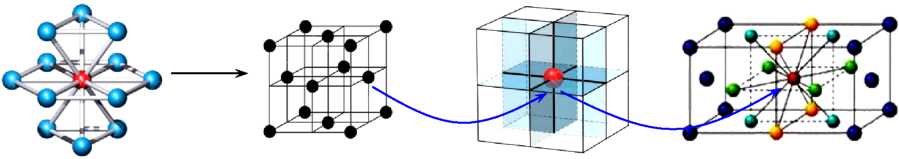
一、体心立方堆积晶胞(以CsCl为例)
⑴Cs+、Cl-的配位数均为8。
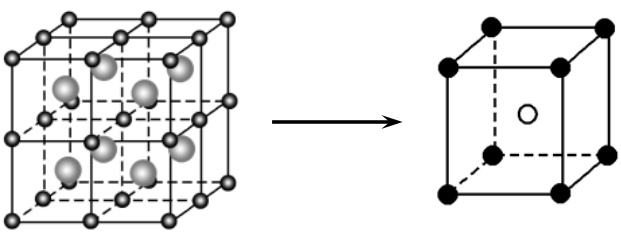
(2)白球Cs+填入黑球Cl-所形成的“立方体”空隙中。
⑶CsCl晶胞中含有1个“立方体”空隙,Cs+的填隙率为100%。
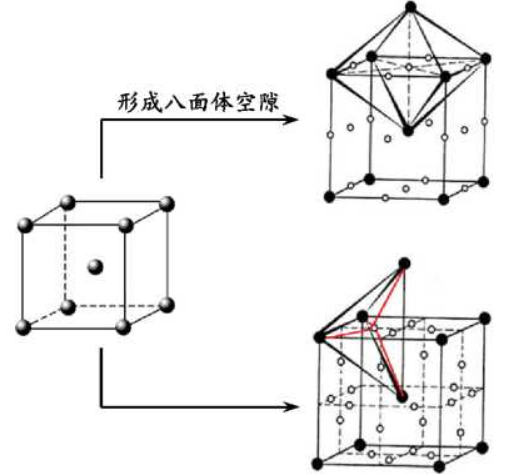
⑷体心立方堆积的原子可以形成6个“八面体”空隙。
(面心6×~=3个,棱心12×
=3个,共6个)
⑸体心立方堆积原子还可以形成12个“四面体”空隙。
二、面心立方堆积晶胞
1、以NaCl为例
(1) Na+、Cl-的配位数均为6。
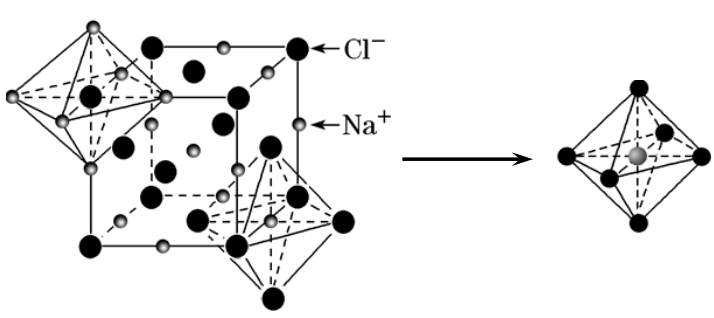
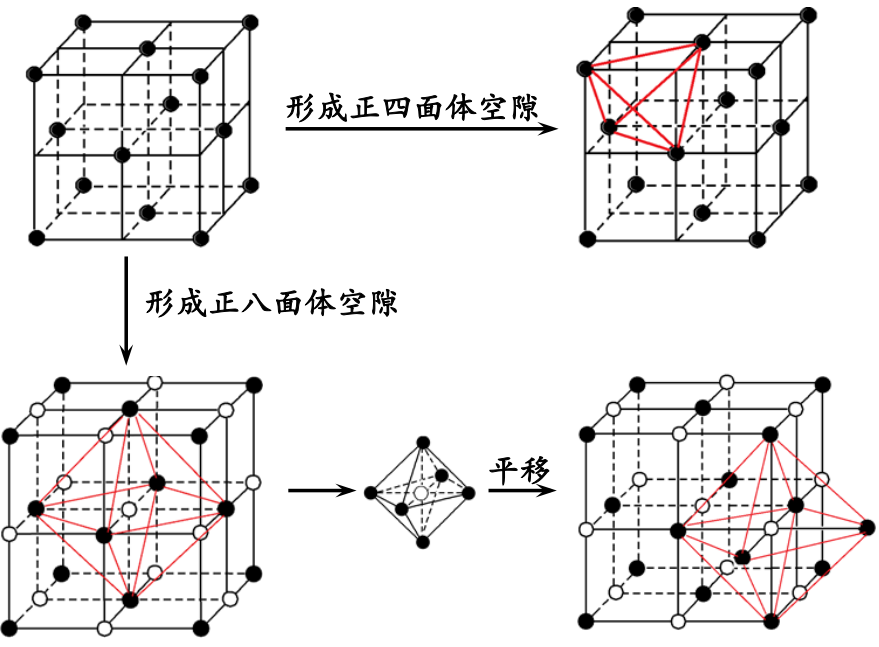
⑵黑球Cl-还可以形成“正四面体”空隙。
⑶NaCl晶胞中含有8个“正四面体”空隙, 空隙处无任何离子填充。
⑷白球Na+填入黑球Cl-所形成的“正八面体” 空隙中。
⑸NaCl晶胞中含有4个“正八面体”空隙。
(体心1个,棱心12×=3个)
⑹Na+的填隙率为100%。
⑺面心立方堆积原子的配位数为12。
2、以ZnS为例
⑴白球(Zn2+)、黑球(S2-)的配位数均为4。
⑵Zn2+填入S2-所形成“正四面体”空隙中。
⑶ZnS晶胞中含有8个“正四面体”空隙。
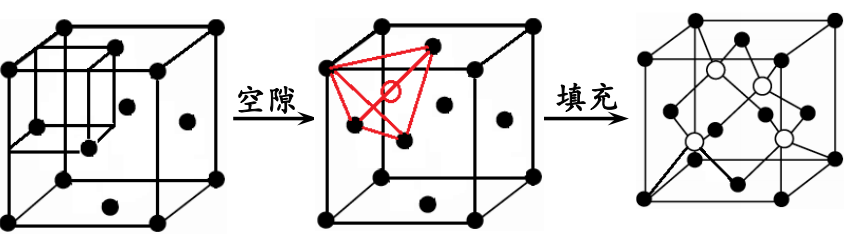
⑷Zn2+的填隙率为50%。
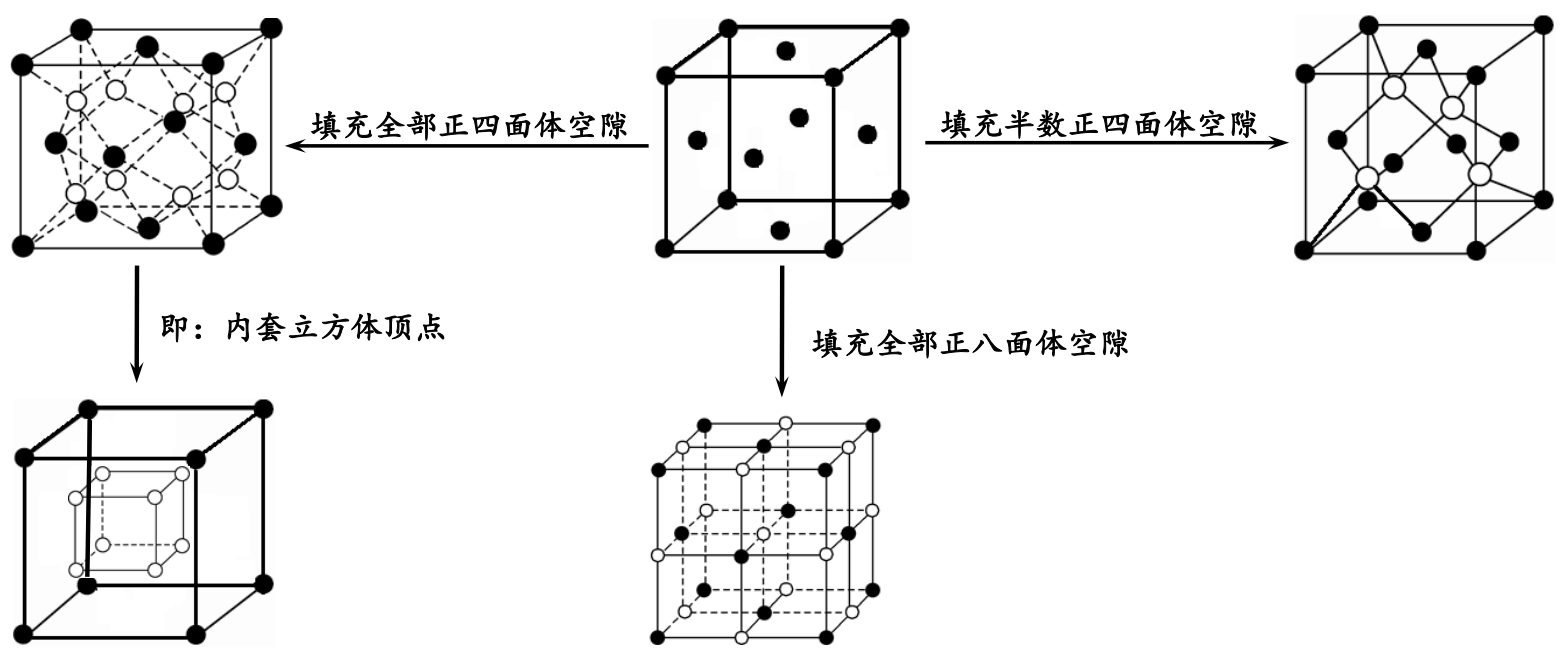
3、面心立方堆积晶胞中空隙填充情况:
三、六方最密堆积晶胞(以Mg为例)
(1)Mg原子的配位数为12
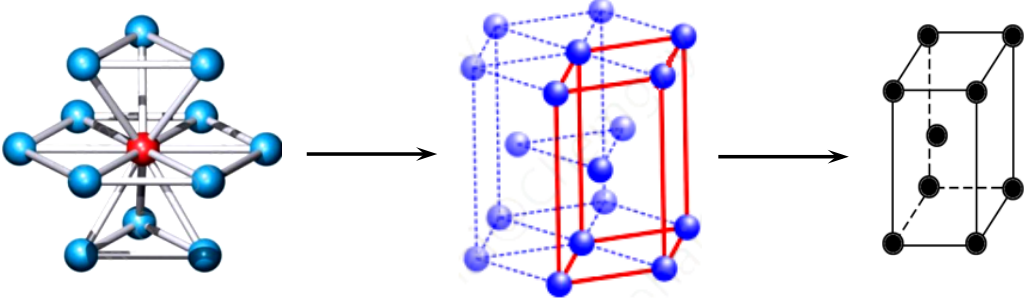
⑵Mg晶胞中含有6个“正八面体”空隙。
在晶胞的上半部有:3个;在晶胞的下半部有:3个
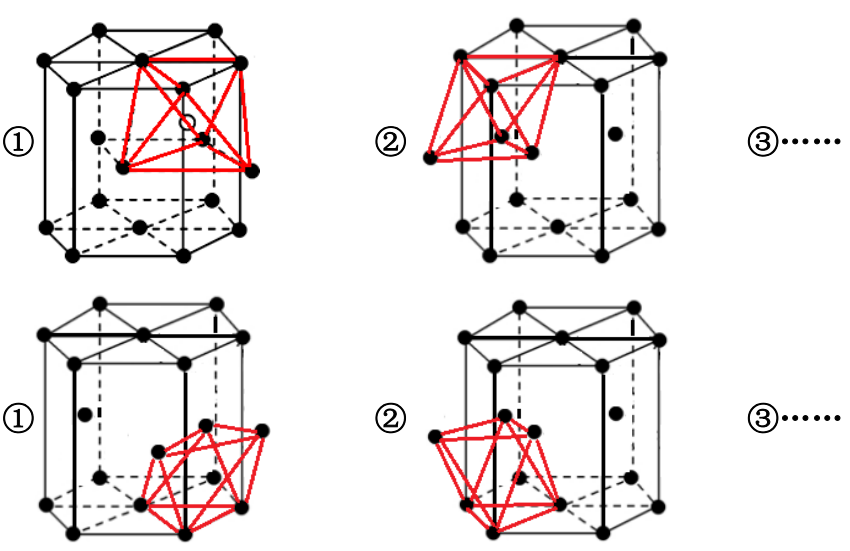
⑶Mg晶胞中含有12个“正四面体”空隙。
在晶胞的上半部有:3个;在晶胞的下半部有:3个
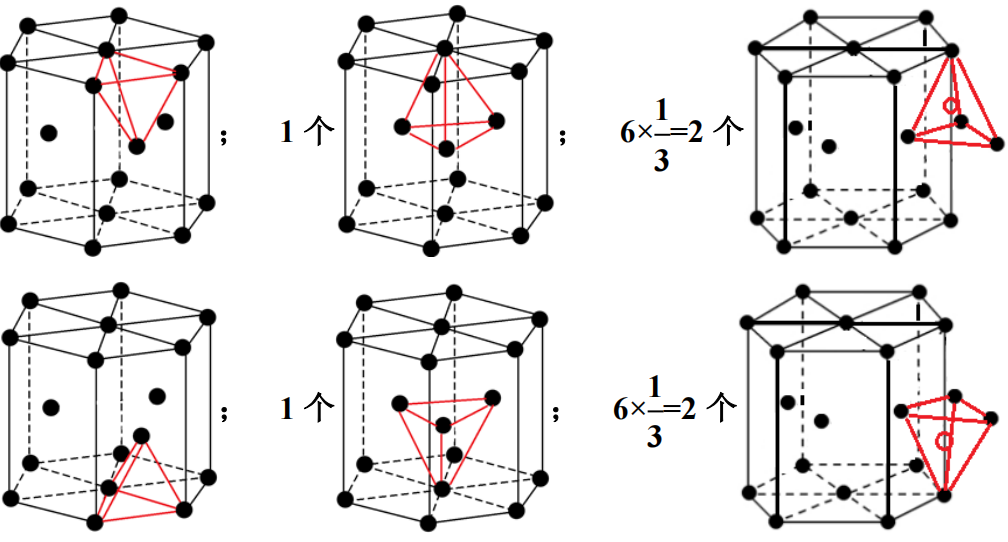
⑷Mg晶胞中含有“正四面体”空隙投影图:
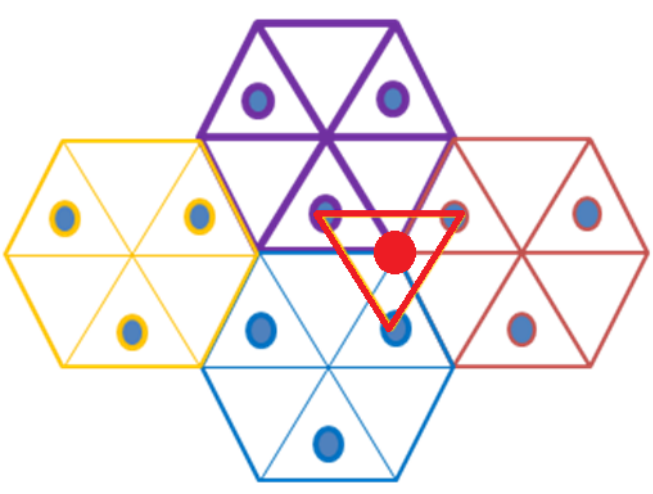
四、学以致用
1.在某种含镁、镍、碳3种元素的超导材料晶体中,镁原子和镍原子一起以立方最密堆积方式形成有序结构。结构中的两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,碳原子只填充在由镍原子构成的八面体空隙中,晶胞如图所示。
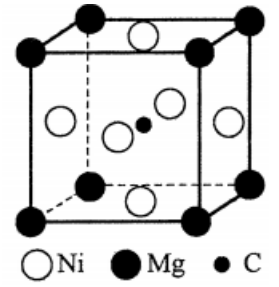
⑴组成该晶体的化学式为 。
⑵完全由镍原子构成的八面体空隙与由镍原子和镁原子共同构成的八面体空隙的数量比为
由镍原子和镁原子共同构成的八面体空隙中,镍原子和镁原子的数量比为 。
⑶若取碳原子为晶胞顶点,则镍原子位于晶胞的 位置。
【答案】⑴MgNi3C,⑵1:3, 2:1,⑶棱心
2.如图所示,Fe3O4晶体中,O2-围成正四面体空隙和正八面体空隙,Fe3O4中有一半的Fe3+填充在正四面体空隙中,Fe2+和另一半Fe3+填充在正八面体空隙中。则没有填充阳离子的正四面体空隙数与没有填充阳离子的正八面体空隙数之比为 。
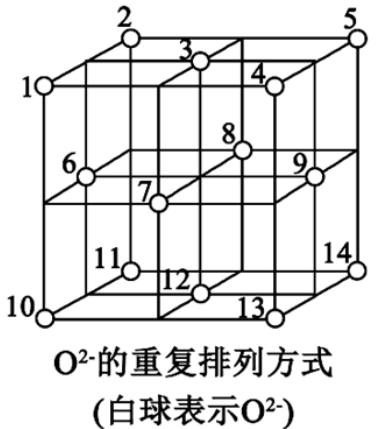
【答案】7:2
3.铬的一种氧化物的晶胞结构如图所示,其中氧离子与晶体镁的堆积方式一致,铬离子填充在其八面体空隙中,
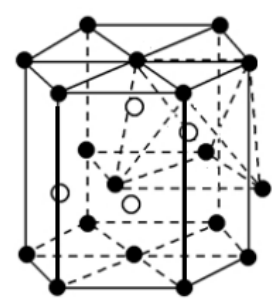
⑴该氧化物的化学式为 。
⑵该晶胞有 %八面体空隙未填充阳离子。
【答案】⑴Cr2O3,⑵33.3
4.某种磁性氮化铁的结构如图所示,
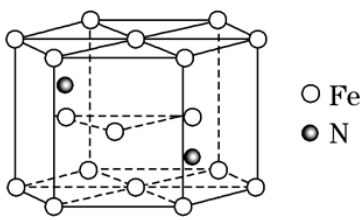
Fe为 堆积,N随机排列,在Fe构成的正四面体空隙中,空隙的占有率为,则该化合物的化学式为 ,该晶胞中含有 个正四面体空隙,其中与铁原子距离最近的铁原子的个数为
【答案】六方最密,Fe3N, 12, 12

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
晶体的形状是一定的,晶体颗粒的大小与结晶条件有关,溶质的...
一、晶体和非晶体 1.固体的分类 分类:固体分为晶体和非晶体两...
金刚石晶体有多种外形,其中正八面体是比较典型的。“从这种...
一、晶体的概念: 整块物质都由原子或分子按一定规律作周期性...
新课改后,人教版高中化学教材《物质结构与性质》第三章第一...
金红石 (TiO 2 ) 是一种重要的半导体光电转化材料,具有独特的光...