
|
学习小专题 |

|
学习小专题 |
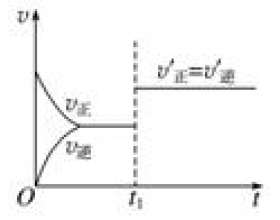 [方法与规律i] 利用图像“断点”探究外因对反应速率的影响 作者:化学自习室 来源:未知 日期:2020-02-21 10:44:55 点击:2209 所属专题:化学平衡图像
[方法与规律i] 利用图像“断点”探究外因对反应速率的影响 作者:化学自习室 来源:未知 日期:2020-02-21 10:44:55 点击:2209 所属专题:化学平衡图像
一、知识梳理 1.当可逆反应达到一种平衡后,若某一时刻外界条件发生改变,都可能使速率—时间图像的曲线出现不连续的情况,根据出现“断点”前后的速率大小,即可对外界条件的变化情况作出判断。如图: t 1 时刻改变的条件可能是使用了催化剂或增大压强(仅适用于反应前后气...
 [方法与规律i] 化学平衡图像题的解题方法 作者:化学自习室 来源:未知 日期:2020-02-21 10:21:32 点击:6507 所属专题:化学平衡图像
[方法与规律i] 化学平衡图像题的解题方法 作者:化学自习室 来源:未知 日期:2020-02-21 10:21:32 点击:6507 所属专题:化学平衡图像
化学平衡图象类试题是高考的热点题型,该类试题经常涉及到的图象类型有物质的量(浓度)、速率—时间图象,含量—时间—温度(压强)图象,恒温、恒压曲线等,图象中蕴含着丰富的信息量,具有简明、直观、形象的特点,命题形式灵活,难度不大,解题的关键是根据反应特点,明确反...
 [方法与规律i] 用假设思想解化学平衡题 作者:化学自习室 来源:未知 日期:2020-03-14 10:01:07 点击:912 所属专题:假设法
[方法与规律i] 用假设思想解化学平衡题 作者:化学自习室 来源:未知 日期:2020-03-14 10:01:07 点击:912 所属专题:假设法
一、极端假设 例1、在一密闭容器中进行反应:2SO 2 (g)+O 2 (g) 2SO 3 (g)。已知反应过程中某一时刻SO 2 、O 2 、SO 3 的浓度分别为0.2mol·L -1 、0.1mol·L -1 、0.2mol·L -1 。当反应达到平衡时,可能存在的数据是( ) A. SO 2 为0.4mol·L -1 ,O 2 为0.2mol·...
 [方法与规律i] 沉淀溶解平衡图像题的解题策略 作者:王宇竞 来源:未知 日期:2020-01-31 12:02:57 点击:1338 所属专题:溶度积曲线
[方法与规律i] 沉淀溶解平衡图像题的解题策略 作者:王宇竞 来源:未知 日期:2020-01-31 12:02:57 点击:1338 所属专题:溶度积曲线
...
 [方法与规律i] 巧用浓度商解决化学平衡中的几个疑点 作者:朱思敏 来源:未知 日期:2019-12-26 08:48:31 点击:3477 所属专题:浓度商 化学平衡常数
[方法与规律i] 巧用浓度商解决化学平衡中的几个疑点 作者:朱思敏 来源:未知 日期:2019-12-26 08:48:31 点击:3477 所属专题:浓度商 化学平衡常数
化学平衡的问题是高考化学中的重点和难点.浓度商(常用Qc表示),是指在任意时刻,生成物浓度幂之积与反应物浓度幂之积的比值.若Qc<K,平衡正向移动;若Qc>K,平衡逆向移动;若Qc=K,则为平衡状态.利用浓度商与平衡常数的比较,可以定量判断可逆反应是否达到平衡的状态或平...
 [方法与规律i] 分压平衡常数计算方法 作者:化学自习室 来源:未知 日期:2019-12-25 07:12:02 点击:75791 所属专题:分压平衡常数
[方法与规律i] 分压平衡常数计算方法 作者:化学自习室 来源:未知 日期:2019-12-25 07:12:02 点击:75791 所属专题:分压平衡常数
K p含义:在化学平衡体系中,用各气体物质的分压替代浓度计算的平衡常数叫压强平衡常数。 计算技巧: 第一步,根据“三段式”法计算平衡体系中各物质的物质的量或物质的量浓度; 第二步,计算各气体组分的物质的量分数或体积分数; 第三步,根据分压计算公式求出各气体物质...
 [方法与规律i] 利用化学反应速率常数解题的灵活变通之道 作者:李梅 来源:未知 日期:2019-12-17 22:38:39 点击:3544 所属专题:速率常数
[方法与规律i] 利用化学反应速率常数解题的灵活变通之道 作者:李梅 来源:未知 日期:2019-12-17 22:38:39 点击:3544 所属专题:速率常数
...
 [方法与规律i] 利用化学平衡常数解决勒沙特列原理压强中问题 作者:化学自习室 来源:未知 日期:2019-12-10 08:19:04 点击:1231 所属专题:化学平衡常数 勒沙特列原理盲区
[方法与规律i] 利用化学平衡常数解决勒沙特列原理压强中问题 作者:化学自习室 来源:未知 日期:2019-12-10 08:19:04 点击:1231 所属专题:化学平衡常数 勒沙特列原理盲区
在各类试题中,经常会涉及到改变一个外 界条件,要我们去分析化学平衡是否移动及结果变化的问题,很多学生都是利用勒沙特列原理来分析,却在运用的过程中总会出现一些问题,甚至得出错误的结论。 题1: 一定温度下,某真空密闭容器投入碳酸钙,发生反应CaCO 3 (s) CaO(s...
 [方法与规律i] 强酸、弱酸常见的七种判断方法 作者:化学自习室 来源:未知 日期:2019-11-06 11:21:49 点击:72505 所属专题:强酸与弱酸比较
[方法与规律i] 强酸、弱酸常见的七种判断方法 作者:化学自习室 来源:未知 日期:2019-11-06 11:21:49 点击:72505 所属专题:强酸与弱酸比较
强酸、弱酸的辨别是中学化学的重要知识 点,也是高考的考点和热点,它涉及到离子方程式的书写、离子共存、pH的求算等多方面内容, 因而必须了解强酸、弱酸常见的七种判断方法。 1、根据化学方程式判断 强酸制弱酸是复分解反应发生的条件之 一,它体现了酸性的相对强弱.如CaC...
 [方法与规律i] 判断化学平衡状态的标志口诀 作者:化学自习室 来源:未知 日期:2022-04-07 14:44:44 点击:21493 所属专题:平衡状态
[方法与规律i] 判断化学平衡状态的标志口诀 作者:化学自习室 来源:未知 日期:2022-04-07 14:44:44 点击:21493 所属专题:平衡状态
一、等的标志:(平衡的本质) 口诀:“同向”不可断, “异向”比例才可断 正反应速率:V(反应物)消耗、V(生成物)生成 逆反应速率:V(反应物)生成、V(生成物)消耗 1、同一物质表示:V(反应物)消耗= V(反应物)生成 或V(生成物)消耗= V(生成物)生成 2、不同物质表示:一种...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
虽然分压都可以用P 分 =P 总 ×( n ( 分 )/ n ( 总 ))计算,但在恒温...
...
一、公式提出的背景 19世纪末,化学家们逐渐意识到温度对化学...
假设对于反应 a A(g) + b B(g) g G(g) + h H(g) 中各物质均为理想气体,...
例:某温度、起始压强为100 kPa下,若将2mol SO 2 和1molO 2 ,通入恒...
...
什么是活化能、能垒? 1 、能垒 活化分子含有的能参加化学反应...
化学学习过程中,我们经常碰到这样一类问题,如图一,由始态...