
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑j] 实例列举法判断电解质溶液正误题 作者:张超鹏 来源:山西省壶关一中 日期:2014-05-15 09:43:16 点击:4535 所属专题:电解质溶液 是非判断
[注解与辨疑j] 实例列举法判断电解质溶液正误题 作者:张超鹏 来源:山西省壶关一中 日期:2014-05-15 09:43:16 点击:4535 所属专题:电解质溶液 是非判断
1 、强电解质溶于水,弱电解质难溶于水。 不一定。碳酸钙是强电解质,难溶于水;醋酸是弱电解质,却易溶于水。 2 、分子中键的极性越强,其物质越易电离。 不一定。例如 HF 分子中有很强的极性键,但是由于 HF 的键能大,原子之间结合得很牢固,再加上 HF 分子之间由于...
 [注解与辨疑j] 如何确定盐溶液蒸干后的固体产物 作者:刘小丹 来源:未知 日期:2013-08-09 17:36:50 点击:7351 所属专题:盐类水解应用 蒸干
[注解与辨疑j] 如何确定盐溶液蒸干后的固体产物 作者:刘小丹 来源:未知 日期:2013-08-09 17:36:50 点击:7351 所属专题:盐类水解应用 蒸干
将盐溶液蒸干,是在敞开的容器中进行的,在实验室里,是在蒸发皿中进行的。在蒸发过程中,水不断汽化,在常压下,在蒸干以前,溶液的温度保持在100摄氏度左右。盐溶液蒸干后,固体产物是不是原来的盐呢?不一定。这是因为有些盐在蒸发浓缩过程中会发生化学反应。 分解温...
 [注解与辨疑j] 如何由FeCl3溶液制取氯化铁晶体? 作者:王兵 来源:未知 日期:2013-05-19 09:47:00 点击:14806 所属专题:氯化铁 盐类水解应用
[注解与辨疑j] 如何由FeCl3溶液制取氯化铁晶体? 作者:王兵 来源:未知 日期:2013-05-19 09:47:00 点击:14806 所属专题:氯化铁 盐类水解应用
通过对FeCl 3 溶液加热浓缩、冷却结晶、过滤,在此过程需要向FeCl 3 溶液中加入过量的盐酸,以防止Fe 3+ + 3H 2 O Fe(OH) 3 + 3H + 这一反应的发生而产生氢氧化铁。由于铁盐水解产生氢氧化铁胶体,所以铁盐可用作净水剂。由FeCl 3 晶体制取FeCl 3 固体时加热失水的过程应在H...
 [注解与辨疑j] Kw与温度的关系 作者:古盛兰 来源:未知 日期:2013-04-15 15:45:05 点击:11130 所属专题:水的离子积常数
[注解与辨疑j] Kw与温度的关系 作者:古盛兰 来源:未知 日期:2013-04-15 15:45:05 点击:11130 所属专题:水的离子积常数
在稀溶液中,KW不随离子浓度的变化而改变,不论溶液是酸性、碱性或中性,溶液中的c(H + )和c(OH - )的乘积在一定温度下为一常数。 K w 随温度的变化而改变,温度升高,K w 明显地增大 ,见下表。 K w 跟温度变化的关系表 温度/℃ K w 温度/℃ K w 0 1.13810 -15 40 2.91...
 [注解与辨疑j] 酸的强弱比较表 作者:武群 来源:未知 日期:2013-04-12 09:16:34 点击:3273 所属专题:强酸与弱酸比较
[注解与辨疑j] 酸的强弱比较表 作者:武群 来源:未知 日期:2013-04-12 09:16:34 点击:3273 所属专题:强酸与弱酸比较
注意: ①强酸是强电解质。中强酸和弱酸属于弱电解质,其电离方程式写可逆符号,在离子方程式中写分子式。②由H 2 SO 3 >H 3 PO 4 ,且NaH 2 PO 4 的水溶液显酸性可知,KHSO 3 和NaHSO 3 的水溶液也应显酸性。③强电解质是全部电离,之所以有强弱,是因为表观电离度所致。...
 [注解与辨疑j] 常用酸碱指示剂的变色范围 作者:张修鹏 来源:未知 日期:2013-04-12 08:51:58 点击:9542 所属专题:酸碱指示剂
[注解与辨疑j] 常用酸碱指示剂的变色范围 作者:张修鹏 来源:未知 日期:2013-04-12 08:51:58 点击:9542 所属专题:酸碱指示剂
碱指示剂 变色范围 PKHin 颜色 浓度 用量 酸色 碱色 (滴/10mL试液) 百里酚蓝 (麝香草酚蓝) 1.2~2.8 1.65 红 黄 0.1%的20%酒精溶液 1~2 甲基黄 2.9~4.0 3.3 红 黄 0.1%的90%酒精溶液 1 甲基橙 3.1~4.4 3.40 红 黄 0.05%的水溶液 1 溴酚蓝 3.0~4.6 3.85 黄 蓝紫 0.1%的...
 [注解与辨疑j] 同离子效应与盐效应 作者:翟娜 来源:未知 日期:2013-04-11 10:34:05 点击:11109 所属专题:同离子效应 盐效应
[注解与辨疑j] 同离子效应与盐效应 作者:翟娜 来源:未知 日期:2013-04-11 10:34:05 点击:11109 所属专题:同离子效应 盐效应
若在难溶电解质溶液中,加入一种与难溶电解质无共同离子的电解质,将使难溶电解质的溶解度增大。这种由于加入了易溶的强电解质而增大难溶电解质溶解度的现象称作盐效应。例如BaSO 在KNO 溶液中的溶解度就比在纯水中稍大,并且KNO 浓度越大,BaSO 的溶解度也变得越大。这...
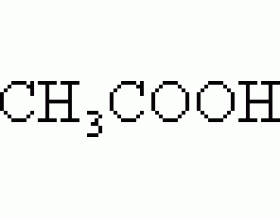 [注解与辨疑j] 电离度解析 作者:刘学超 来源:未知 日期:2013-04-10 08:32:20 点击:5099 所属专题:电离度
[注解与辨疑j] 电离度解析 作者:刘学超 来源:未知 日期:2013-04-10 08:32:20 点击:5099 所属专题:电离度
弱酸、弱碱等弱电解质在水溶液中存在电离平衡。例如: 当达到电离平衡时,弱电解质溶液里的离子浓度保持一定,可用此时离子浓度的高低衡量弱电解质的相对强弱。本节的电离度就是定量描述弱电解质强弱的重要概念。 1 .准确理解电离度的概念 当弱电解质在溶液里达到电离平衡...
 [注解与辨疑j] Ksp中s及p的含义 作者:张澳 来源:未知 日期:2013-03-28 09:10:28 点击:4648 所属专题:溶度积
[注解与辨疑j] Ksp中s及p的含义 作者:张澳 来源:未知 日期:2013-03-28 09:10:28 点击:4648 所属专题:溶度积
Ksp中sp即solubility product,solubility(可溶物),product(乘积),solubility product(溶度积)。类似的Kw中的w是water(水)。...
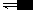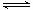 [注解与辨疑j] 应用盐类水解知识解释的几个问题 作者:张扬 来源:未知 日期:2020-01-30 14:08:15 点击:8020 所属专题:盐类水解应用
[注解与辨疑j] 应用盐类水解知识解释的几个问题 作者:张扬 来源:未知 日期:2020-01-30 14:08:15 点击:8020 所属专题:盐类水解应用
1 . 化学实验中的盐类水解问题 ⑴ 为什么实验室中配制 FeCl 3 溶液时要在其中加入少量浓盐酸? 目的是为了防止 FeCl3 溶液的水解,因为在 FeCl3 溶液中存在下列水解方程式, FeCl 3 + 3H 2 O Fe(OH) 3 ↓+ 3HCl,当在溶液中加入浓盐酸时,该水解方程式向左进行,从而...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1、 碳酸氢钠溶液pH计算公式的推导 注意: 值得注意的是,最后推导的公式从表面上看c(...
溶解度和溶度积换算 溶解度和溶度积均可以定量表示难溶物质的溶解性。 溶解度与溶度积...
...
酸碱滴定法 强酸滴定强碱的反应 强酸滴定弱碱的反应 混合碱的滴定(双指示剂法+滴定突...
【学生疑问】 教材上有两个实验,一个是 AgI 转化为 Ag 2 S,一个是 Mg(OH) 2 转化为 ...
25 ℃ 时, K a1 (H 2 S)=1.1 × 10 -7 ; K a2 (H 2 S)=1.3 × 10 -13 . (高等教育...
沉淀转化是沉淀溶解平衡的应用之一。 对于溶度积较大的沉淀转为溶度积较小的沉淀这类...
1.实例 常温下,用0.100 0 mol・L -1 NaOH溶液滴定20.00 mL 0.100 0 mol・L -1 CH 3...