
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
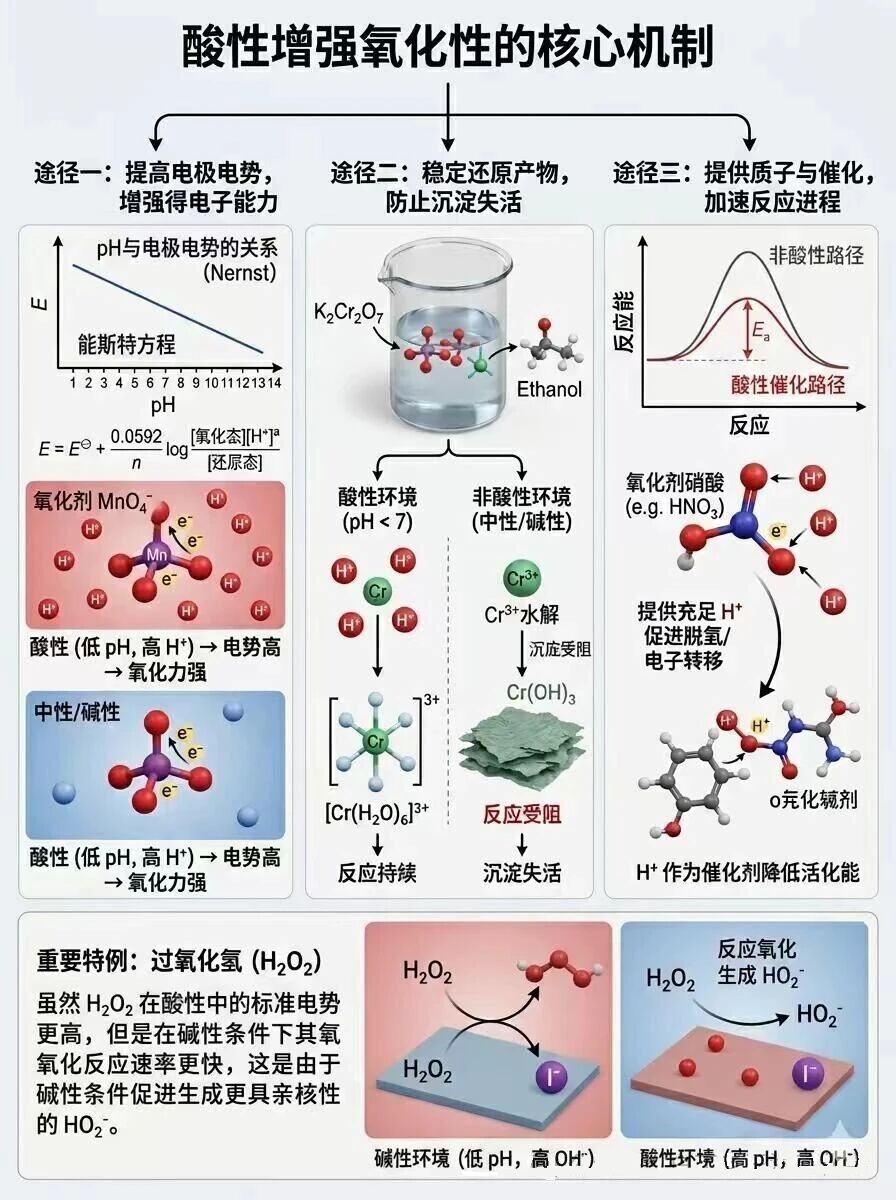
酸性环境主要通过影响电极电位、提升产物稳定性、参与反应机制三大途径增强氧化剂的氧化性,是氧化还原反应中的关键影响因素,以下为核心原理拆解:
1. 电化学本质:提升电极电势,强化氧化能力
氧化剂的氧化能力由标准电极电势决定,涉及H+的氧化还原半反应,电势受pH值直接影响(能斯特方程)。
酸性增强→c(H+)↑→电极电势显著升高→氧化剂得电子能力大幅提升,氧化能力远强于中性、碱性环境(含氧酸根类氧化剂此效应最显著)。
2. 产物稳定性:抑制水解,推动反应正向进行
多数氧化剂的还原产物(如金属离子)在酸性环境中更稳定,避免因水解阻碍反应:
例:重铬酸钾氧化乙醇,还原产物Cr3+在中性、碱性下水解生成Cr(OH)3沉淀,覆盖反应物阻断反应;
酸性下Cr3+以稳定水合离子[Cr(H2O)6]3+存在,保持溶解状态,让氧化还原电对正常工作,反应持续进行到底。
3. 反应机制:提供质子,降低活化能加速反应
氧化反应多为脱氢/电子转移伴随质子转移的过程,酸性环境的作用体现在两点:
提供充足H+,助力完成脱氢、电子转移核心步骤(如浓硝酸、浓硫酸氧化有机物时,H+配合实现脱水、酸化,让被氧化物更易失电子、氢原子);
H+可作为催化剂,活化氧化剂/被氧化物质,降低反应活化能,直接加速氧化过程。
重要特例:过氧化氢H2O2
H2O2的氧化性与常规规律相反:碱性环境中氧化反应速率更快(虽酸性下标准电位略高)。
原因:碱性条件促进H2O2生成更具亲核进攻能力的HO2-,能更快氧化碘离子、亚铬离子等物质。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
酸性环境主要通过影响电极电位、提升产物稳定性、参与反应机...
在金属催化偶联反应中中,钯催化剂最为常用,但钯有各种价态...
...
在氧化还原反应中,氧化剂得电子被还原生成还原产物,还原剂...
溶液的酸碱性对氧化还原反应具有显著且多方面的影响,主要体...
在氧化还原反应中,“档次” 本质是氧化性 / 还原性的强弱等级...