
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【导读】有机物水解均为取代反应,卤代烃、酯、油脂、糖类、蛋白质、酸酐均可发生水解反应。
卤代烃需 NaOH 水溶液加热,酯与油脂酸性可逆、碱性完全水解,糖和蛋白质以酸和酶水解为主。产物规律:卤代烃得醇、酯得酸与醇、多糖得单糖、蛋白质得氨基酸,碱性水解更彻底。
一、卤代烃的水解
反应本质:取代反应,NaOH水溶液、加热,生成醇
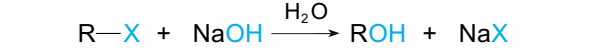

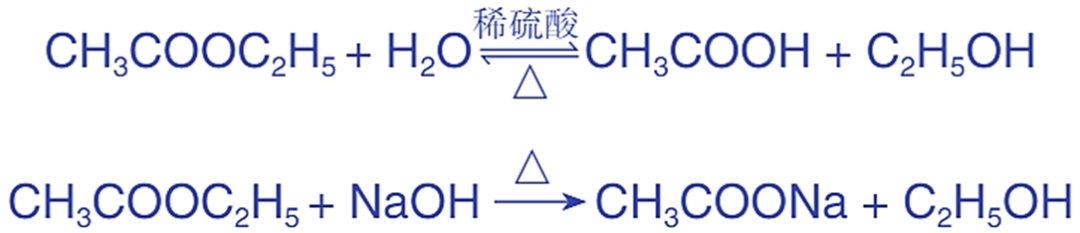
二、酯类的水解
反应本质:取代反应,稀硫酸加热(可逆);NaOH加热(完全)。
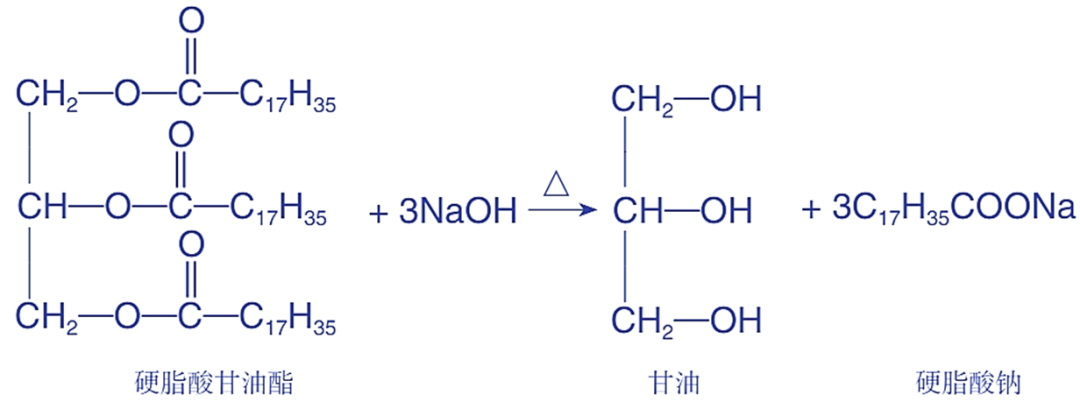
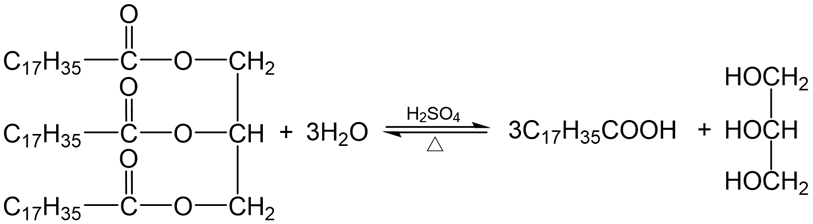
三、油脂的水解
反应本质:高级脂肪酸甘油酯水解,酸性得脂肪酸+甘油;碱性得脂肪酸盐+甘油,是皂化反应。
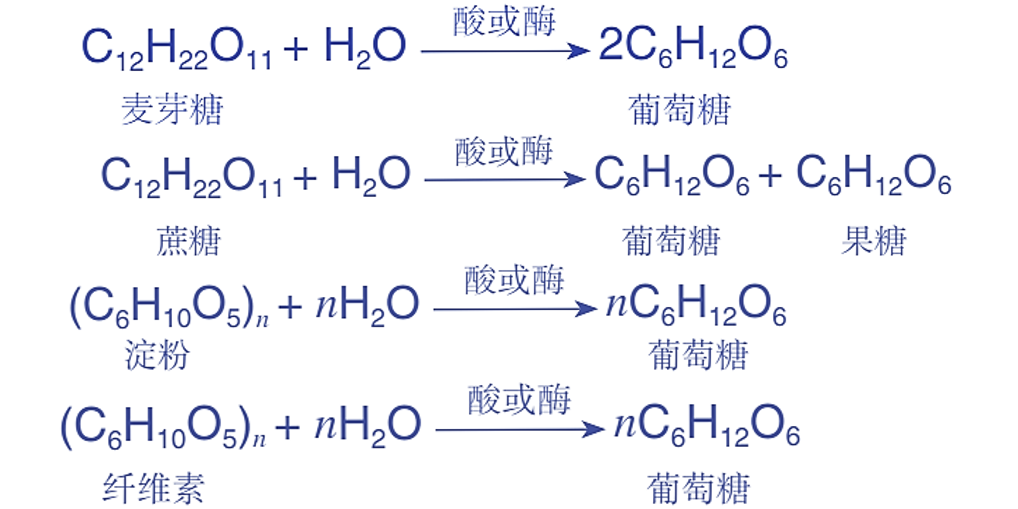
四、糖类的水解
反应本质:多糖、二糖在稀酸、酶作用下断裂苷键,生成单糖
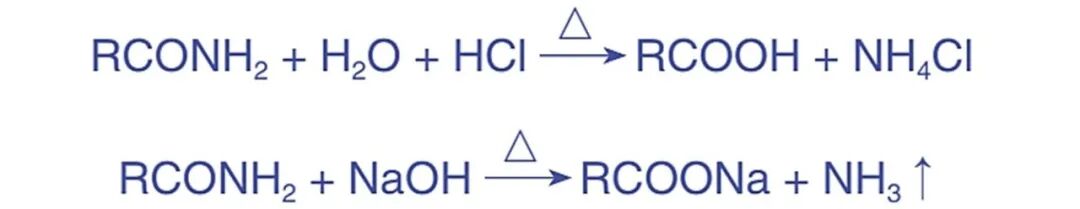
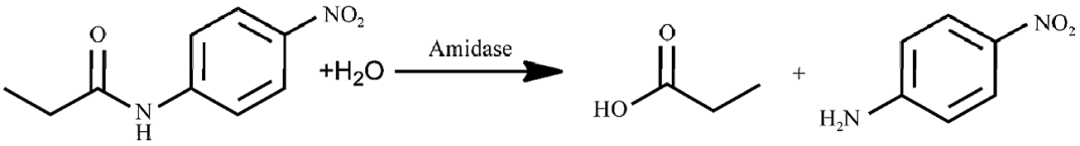
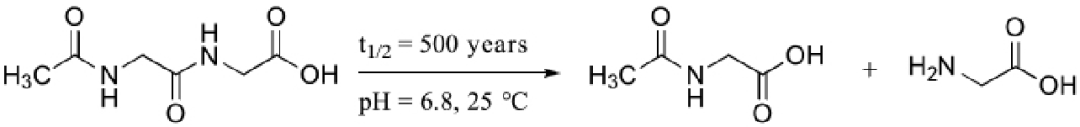
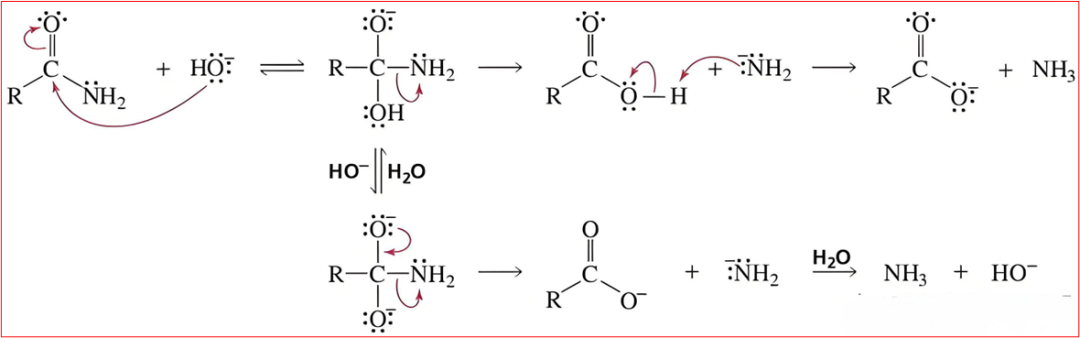
五、酰胺、肽键、蛋白质的水解
反应本质:酰胺、肽键断裂,酸、碱或酶条件生成对应的羧酸和胺、氨;蛋白质水解最终生成氨基酸。
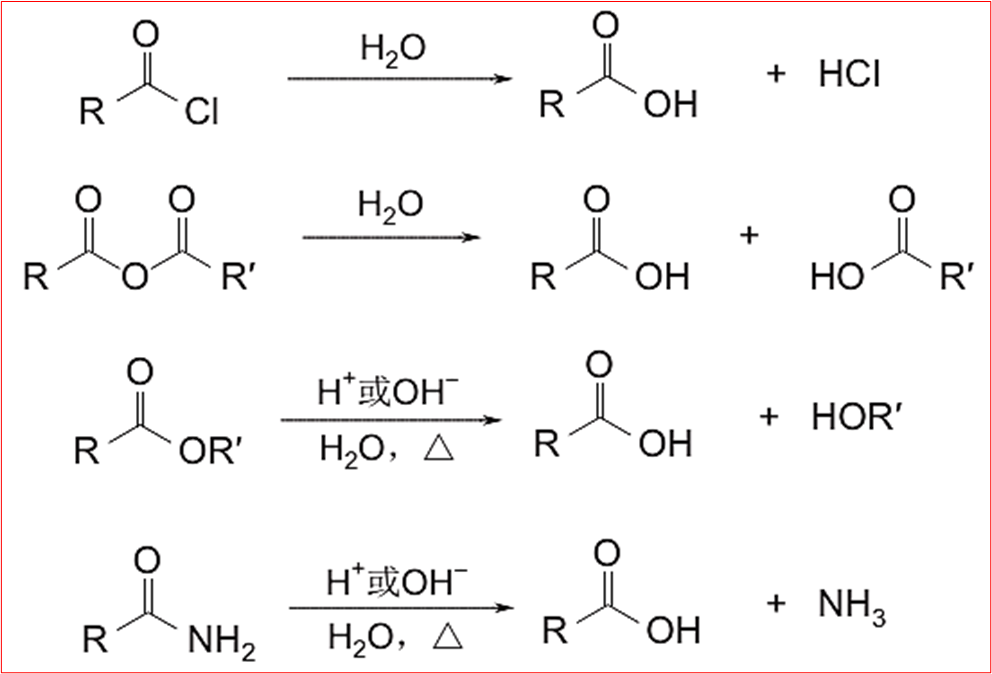
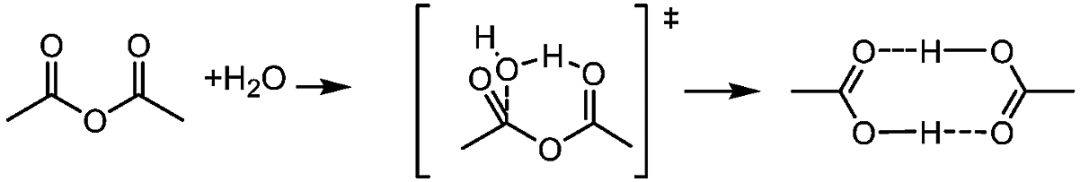
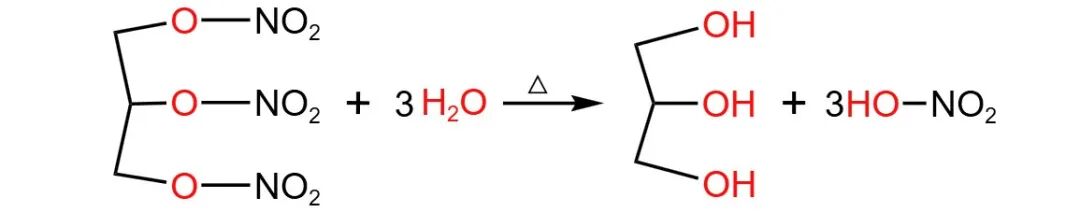
六、有机酸酐及无机酸酯的水解
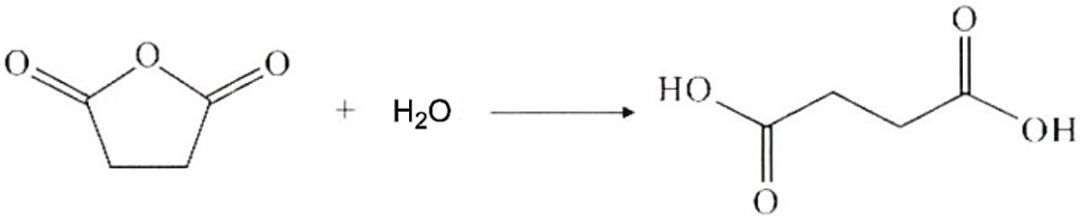
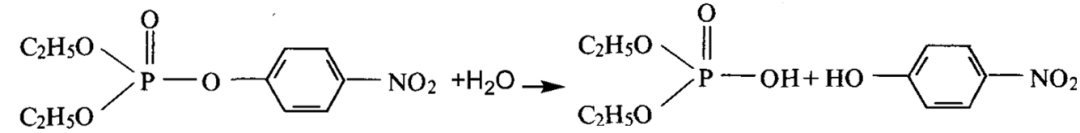
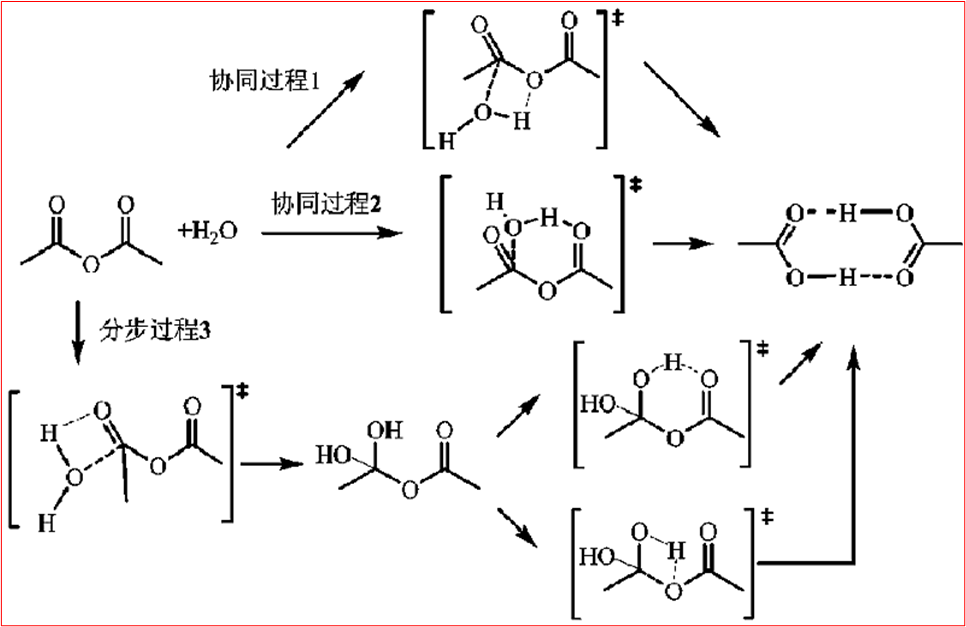
七、有机物水解反应规律总结
1.反应类型
全部属于取代反应,有进有出,原子团交换。
2.通用反应通式
R−X+H−OH→R−OH+H−X
R−COOR'+H−OH→R−COOH+R'−OH
R−CONHR'+H−OH→R−COOH+R'−NH₂
遵循“电荷匹配”规则,正电性的基团结合-OH,负电性的基团结合-H。
3.条件规律
卤代烃:NaOH水溶液、加热
酯、油脂:稀H₂SO₄加热(可逆);NaOH加热(完全)
糖类、蛋白质:稀酸或酶,温和条件
4.结构要求
含可断裂极性键:C-X、酯基、苷键、肽键;羧基一般不水解。
5.产物规律
卤代烃+NaOH→醇+卤化钠
酯+H₂O→羧酸+醇(酸性水解)
油脂+H₂O→高级脂肪酸+甘油(酸性水解)
二糖+H₂O→两分子单糖
多糖+nH₂O→n单糖
酰胺基+H₂O+无机酸→羧酸+铵盐(酸性水解)
蛋白质→氨基酸
6.可逆性
酸性水解:可逆
碱性水解:不可逆(中和酸,推动反应完全)

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
中学的有机化学知识系统性强,用归纳和演绎的方法很容易掌握...
【导读】有机物水解均为取代反应,卤代烃、酯、油脂、糖类、...
在高考题中,有机物的命名是我们的重要考点。而含有多官能团...
一、最容易丢分的10个易错点(必看) 1.最长碳链选错 不是“横...
高中有机化学的核心,就是「官能团决定性质」!不管是选择题...
一、什么是取代反应? 一句话:有机物里某个原子/原子团,被...