
|
学习小专题 |

|
学习小专题 |
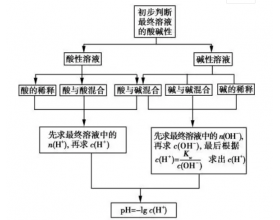 [方法与规律j] pH的计算方法与规律 作者:化学自习室 来源:未知 日期:2020-02-16 11:14:48 点击:12760 所属专题:pH计算
[方法与规律j] pH的计算方法与规律 作者:化学自习室 来源:未知 日期:2020-02-16 11:14:48 点击:12760 所属专题:pH计算
一.溶液pH的计算 1、基本思路 2、类型方法 ①单一溶液 溶液类型 相关计算 强酸(HnA) 设HnA的浓度为cmol/L,则c(H + )=ncmol/L,pH=lgc(H + )=lgnc 强碱[B(OH)n] 设B(OH)n的浓度为cmol/L,则c(OH)=ncmol/L,c(H + )=mol/L,pH=lgc(H + )=14+lgnc ②混合溶液 二.酸...
 [方法与规律j] 化学平衡题常用的几种解法 作者:化学自习室 来源:未知 日期:2020-02-16 10:42:59 点击:899 所属专题:化学平衡解题思维
[方法与规律j] 化学平衡题常用的几种解法 作者:化学自习室 来源:未知 日期:2020-02-16 10:42:59 点击:899 所属专题:化学平衡解题思维
一、特征法 对题干和选择支的特点进行分析,发现隐含信息,得出正确判断的方法。 例1.在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g) 2c(g);△H0x(g)+3y(g) 2z(g);△H0,进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是 A.等压时,通入惰...
 [方法与规律j] 双组分混合电解质溶液质子守恒表达式书写 作者:淮畔化学 来源:未知 日期:2020-02-15 11:34:02 点击:1244 所属专题:质子守恒
[方法与规律j] 双组分混合电解质溶液质子守恒表达式书写 作者:淮畔化学 来源:未知 日期:2020-02-15 11:34:02 点击:1244 所属专题:质子守恒
...
 [方法与规律j] 难溶电解质溶解平衡的图像题集锦 作者:化学自习室 来源:未知 日期:2020-02-14 15:02:06 点击:966 所属专题:溶解平衡图像
[方法与规律j] 难溶电解质溶解平衡的图像题集锦 作者:化学自习室 来源:未知 日期:2020-02-14 15:02:06 点击:966 所属专题:溶解平衡图像
...
 [方法与规律j] 酸碱溶液混合常见典型问题例谈 作者:杨明生 来源:未知 日期:2020-02-14 15:23:16 点击:2241 所属专题:酸碱中和
[方法与规律j] 酸碱溶液混合常见典型问题例谈 作者:杨明生 来源:未知 日期:2020-02-14 15:23:16 点击:2241 所属专题:酸碱中和
酸碱溶液混合的有关问题是中学化学一类常见的典型问题。强酸与强碱溶液混合情况比较简单,恰好完全发生反应时,溶液呈中性,混合溶液的PH=7;酸过量时溶液显酸性, 混合溶液的PH7;碱过量时溶液呈碱性,混合溶液的PH7。但弱酸与强碱溶液混合或强 酸与弱碱溶液混合,以及弱...
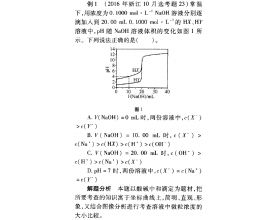 [方法与规律j] 用好“四点”突破图像类溶液中微粒浓度比较 作者:霍金花 来源:未知 日期:2020-02-14 13:33:54 点击:870 所属专题:电解质溶液图像 离子浓度大小比较
[方法与规律j] 用好“四点”突破图像类溶液中微粒浓度比较 作者:霍金花 来源:未知 日期:2020-02-14 13:33:54 点击:870 所属专题:电解质溶液图像 离子浓度大小比较
...
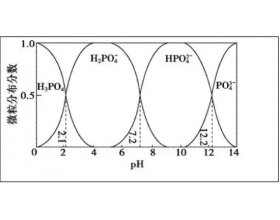 [方法与规律j] 曲线段段清 微粒个个明―电解质溶液图像题精析 作者:胡嘉谋 来源:未知 日期:2020-02-14 12:39:31 点击:1650 所属专题:电解质溶液图像
[方法与规律j] 曲线段段清 微粒个个明―电解质溶液图像题精析 作者:胡嘉谋 来源:未知 日期:2020-02-14 12:39:31 点击:1650 所属专题:电解质溶液图像
电解质溶液中离子浓度大小比较问题,是高考热点中的热点。此类题主要考查弱电解质的电离平衡、盐类水解平衡等离子平衡、电荷守恒、物料守恒、质子守恒、pH及离子浓度计算等,目前常出现多元酸与强碱反应体系中微粒分布分数图或微粒浓度分布图的试题,其解题思维关键:要认真...
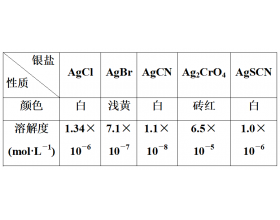 [方法与规律j] 中和滴定的迁移与应用 作者:化学自习室 来源:未知 日期:2020-01-31 14:49:38 点击:4031 所属专题:滴定法
[方法与规律j] 中和滴定的迁移与应用 作者:化学自习室 来源:未知 日期:2020-01-31 14:49:38 点击:4031 所属专题:滴定法
中和滴定的拓展应用是近几年高考试题的创新题型,主要类型有沉淀滴定和氧化还原滴定。考查角度主要有:①滴定管的使用问题、②滴定指示剂的选择、③滴定终点的现象判断、④定量计算问题、⑤滴定误差分析。 1、沉淀滴定法 (1)概念:沉淀滴定法是利用沉淀反应进行滴定、测量分...
 [方法与规律j] 溶度积Ksp在计算中的应用 作者:叶虹 来源:未知 日期:2020-01-31 12:16:30 点击:936 所属专题:溶度积计算
[方法与规律j] 溶度积Ksp在计算中的应用 作者:叶虹 来源:未知 日期:2020-01-31 12:16:30 点击:936 所属专题:溶度积计算
...
 [方法与规律j] 形形色色的粒子浓度之比 作者:化学自习室 来源:未知 日期:2020-01-22 20:41:10 点击:954 所属专题:粒子浓度之比
[方法与规律j] 形形色色的粒子浓度之比 作者:化学自习室 来源:未知 日期:2020-01-22 20:41:10 点击:954 所属专题:粒子浓度之比
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。弱酸也可以制备强酸!!! 比如向 CuSO 4 溶液中加入 H 2 S 溶液生成 CuS 黑色沉淀和 ...
氧化还原滴定法: 1.特点: 氧化还原滴定法在药物分析中应用广泛,用于测定具有氧化性...
问题1: 在酸溶液中,H + 和OH - 的来源分别是什么?举例说明怎样计算由水电离产生...
电离平衡常数是高考中一个重要的必考考点,常考查电离平衡常数的计算、弱酸的相对强弱...
...
一、原理:影响水的电离平衡因素 H 2 O H + +OH - 1.25 ℃, → c (H + ) H2O = ...
...
电解质溶液中有关离子浓度的判断是近年化学高考的重要题型之一。解此类型题的关键是掌...