
|
学习小专题 |

|
学习小专题 |
 [方法与规律j] 双水解反应方程式的配平技巧口诀 作者:化学自习室 来源:未知 日期:2022-08-07 08:19:19 点击:829 所属专题:盐类水解方程式 双水解反应
[方法与规律j] 双水解反应方程式的配平技巧口诀 作者:化学自习室 来源:未知 日期:2022-08-07 08:19:19 点击:829 所属专题:盐类水解方程式 双水解反应
谁弱选谁切记清,添加系数电荷等。 反应式中常加水,质量守恒即配平。 说明:双水解反应,是指由一种强酸弱碱盐与另一种强碱弱酸盐作用,由于相互促进,从而使水解反应进行到底的反应。如:Al 2 (SO 4 ) 3 和Na 2 CO 3 反应。该法的特点是可以直接写系数, 可在瞬间完成配平...
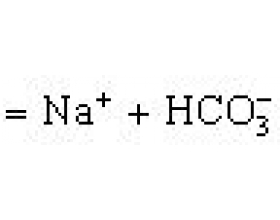 [方法与规律j] 定性与定量来分析比较离子浓度大小 作者:化学自习室 来源:未知 日期:2022-08-04 17:22:38 点击:734 所属专题:离子浓度大小比较
[方法与规律j] 定性与定量来分析比较离子浓度大小 作者:化学自习室 来源:未知 日期:2022-08-04 17:22:38 点击:734 所属专题:离子浓度大小比较
一、离子间的定性关系分析溶液中离子间的定性关系,我们首先应从宏观上把握,即确定溶液的酸碱性:其次应认清电离和水解反应程度的相对大小,在书写方程式时应按电离程度由大到小的顺序进行书写;再次,若离子关系比较复杂,应赋予离子具体的物质的量,以便进行离子或分...
 [方法与规律j] 难溶电解质的溶解平衡及其三个应用 作者:化学自习室 来源:未知 日期:2022-08-03 15:19:00 点击:356 所属专题:溶解平衡
[方法与规律j] 难溶电解质的溶解平衡及其三个应用 作者:化学自习室 来源:未知 日期:2022-08-03 15:19:00 点击:356 所属专题:溶解平衡
...
 [方法与规律j] 高考中常考的电解质溶液图像 作者:化学自习室 来源:未知 日期:2022-05-31 10:17:50 点击:579 所属专题:电解质溶液图像
[方法与规律j] 高考中常考的电解质溶液图像 作者:化学自习室 来源:未知 日期:2022-05-31 10:17:50 点击:579 所属专题:电解质溶液图像
...
 [方法与规律j] 水溶液中离子平衡中对数图像分析 作者:化学自习室 来源:未知 日期:2022-05-31 10:09:46 点击:578 所属专题:对数曲线
[方法与规律j] 水溶液中离子平衡中对数图像分析 作者:化学自习室 来源:未知 日期:2022-05-31 10:09:46 点击:578 所属专题:对数曲线
一、对数图像分析...
 [方法与规律j] 如何证明HA是弱酸的方法 作者:化学自习室 来源:未知 日期:2022-02-22 15:03:29 点击:1729 所属专题:弱酸实验判断
[方法与规律j] 如何证明HA是弱酸的方法 作者:化学自习室 来源:未知 日期:2022-02-22 15:03:29 点击:1729 所属专题:弱酸实验判断
1、相同温度,相同浓度的HA与HCl溶液,HA的导电性较弱。 2、0.lmol/L的HA与0.1mol/L的HCl溶液加水稀释相同倍数,HCl的导电性变化大,降低得更快。 3、0.lmol/L的HA, pHl。 4、升高温度,0.lmol/L的HA的pH值明显减小 5、0.lmol/L 的HA 稀释 10 倍,ΔpHl 6、0.lmol/L 的 HA...
 [方法与规律j] 高考化学各种酸碱滴定曲线图的突破 作者:化学自习室 来源:未知 日期:2022-08-06 10:17:52 点击:1163 所属专题:中和滴定曲线
[方法与规律j] 高考化学各种酸碱滴定曲线图的突破 作者:化学自习室 来源:未知 日期:2022-08-06 10:17:52 点击:1163 所属专题:中和滴定曲线
高考频繁出现酸碱中和滴定的图象题,此类题试题综合性强,难度较大,不仅考查定性与定量结合分析问题的思想,而且考查数形结合识图用图的能力,还要求学生能深入微观世界认识各种化学过程来解决比较微粒浓度大小问题。但万变不离其中,离不开指示剂的选择,离不开滴定曲线的...
 [方法与规律j] 定量分析碳酸氢钠溶液中微粒浓度大小 作者:化学自习室 来源:未知 日期:2021-12-08 15:27:05 点击:558 所属专题:碳酸氢钠01 离子浓度大小比较
[方法与规律j] 定量分析碳酸氢钠溶液中微粒浓度大小 作者:化学自习室 来源:未知 日期:2021-12-08 15:27:05 点击:558 所属专题:碳酸氢钠01 离子浓度大小比较
...
 [方法与规律j] 巧解沉淀滴定问题 作者:化学自习室 来源:未知 日期:2021-11-25 14:49:39 点击:867 所属专题:沉淀滴定
[方法与规律j] 巧解沉淀滴定问题 作者:化学自习室 来源:未知 日期:2021-11-25 14:49:39 点击:867 所属专题:沉淀滴定
沉淀滴定成为了近年来考试的热点问题。比如2018年全国新课标Ⅲ,第六题就考查了这部分内容。今天我就给大家讲解一下这部分知识。 一、沉淀滴定: 1.概念 沉淀滴定是利用沉淀反应进行滴定、测量分析的方法。生成沉淀的反应很多,但符合条件的却很少,实际上应用最多的是...
 [方法与规律j] 溶度积常数及其应用 作者:化学自习室 来源:未知 日期:2021-11-23 14:32:09 点击:4835 所属专题:溶度积
[方法与规律j] 溶度积常数及其应用 作者:化学自习室 来源:未知 日期:2021-11-23 14:32:09 点击:4835 所属专题:溶度积
一、沉淀溶解平衡中的常数( K sp )――溶度积 1.定义:在一定温度下,难溶电解质的饱和溶液中,存在沉淀溶解平衡,其平衡常数叫做溶度积常数(或溶度积) 2.表示方法:以 M m A n (s) mM n+ (aq) + nA m- (aq)为例(固体物质不列入平衡常数), K sp =[ c (M n+ )] m ・[...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。弱酸也可以制备强酸!!! 比如向 CuSO 4 溶液中加入 H 2 S 溶液生成 CuS 黑色沉淀和 ...
氧化还原滴定法: 1.特点: 氧化还原滴定法在药物分析中应用广泛,用于测定具有氧化性...
问题1: 在酸溶液中,H + 和OH - 的来源分别是什么?举例说明怎样计算由水电离产生...
电离平衡常数是高考中一个重要的必考考点,常考查电离平衡常数的计算、弱酸的相对强弱...
...
一、原理:影响水的电离平衡因素 H 2 O H + +OH - 1.25 ℃, → c (H + ) H2O = ...
...
电解质溶液中有关离子浓度的判断是近年化学高考的重要题型之一。解此类型题的关键是掌...