
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
1.聚集状态
(1) 烃:碳原子数小于5的烃都是气体。(新戊烷是气体,沸点:9.5℃)
烷烃:C1 —C4为气体,C5 —C16为液体,C17以上为固体。
烯烃:C2 —C4为气体,C5 —C18为液体,C19以上为固体。
苯的同系物多数为液体,和苯一样有特殊的香味,其蒸气有毒。但对二甲苯为固体。
环丙烷、环丁烷为气体,环戊烷为液体,高级同系物为固体。
|
物质 |
正戊烷 |
异戊烷 |
新戊烷 |
对二甲苯 |
邻二甲苯 |
间二甲苯 |
环已烷 |
苯 |
甲苯 |
乙苯 |
|
熔点 |
-130 |
-159.9 |
-16.5 |
13.3 |
-25.2 |
-47.9 |
6.55 |
80.1 |
110.6 |
136 |
|
沸点 |
36.1 |
27.8 |
9.5 |
138.3 |
144.4 |
139.1 |
80.74 |
|
|
|
|
比重 |
0.6262 |
0.6201 |
0.6135 |
0.8611 |
0.8802 |
0.8642 |
0.7786 |
|
|
|
(2) 烃的衍生物:CH3Cl、CH2=CHCl、C2H5Cl、HCHO、CH3Br等为气体。
饱和一元醇中,C1 —C4为酒味液体,C17以上为固体。
饱和一元羧酸中,C1 —C3为具有强烈酸味和刺激性的流动液体,C4 —C9为具有无色无臭的油状液体,C10以上为石蜡状固体。
硝基化合物中,一硝基化合物为高沸点液体,其余为结晶固体。
酚类、饱和高级脂肪酸、二元羧酸、芳香酸、脂肪、糖类、氨基酸及萘等为固体。
不饱和脂肪酸(如油酸)为液体。
2.一些有机物的沸点:
|
有机物 |
溴甲烷 |
氯乙烷 |
乙醛 |
溴乙烷 |
|
|
沸点 / ℃ |
3.6 |
12.3 |
20.8 |
34.5 |
38.4 |
|
有机物 |
丙醚 |
乙酸乙酯 |
乙醇 |
乙酸 |
溴苯 |
|
沸点 / ℃ |
56.2 |
77 |
78 |
118 |
158 |
3.溶解性
(1) 难溶于水:烃类、卤代烃、酯、硝基化合物、高级脂肪酸、多糖、高分子化合物等。
(2) 低级醇、醛、羧酸、单糖、二糖、氨基酸、丙酮、某些蛋白质溶于水。
(3) 乙炔、乙醚微溶于水。常温下,苯酚微溶于水,70℃以上与水互溶。
(4) 难溶于水,且比水轻:烷烃、烯烃、炔烃、CnHn+1Cl、汽油、乙醚、苯(0.8765 g / cm3)、甲苯(0.8669 g / cm3)、二甲苯、环己烷、乙酸乙酯(0.9003 g / cm3)、油酸及低级酯类、油。
(5) 难溶于水,且比水重:溴甲烷(1.6755 g / cm3)、溴乙烷(1.4604 g / cm3)、溴苯(1.495 g / cm3)、CCl4、硝基苯、多氯代烃、溴代烃等。
4.最简式相同的
(1) CH:乙炔(C2H2)、(C4H4)、苯(C6H6)、立方烷(C8H8)
CH2:烯烃(C2H4)、环烷烃(CnH2n)
CH2O:甲醛(CH2O)。乙酸和甲酸甲酯(C2H4O2)、乳酸(C3H6O3)、葡萄糖和果糖(C6H10O6)
C6H10O5(葡萄糖单元):淀粉和纤维素[(C6H10O5)n]
(2) 最简式相同的,所含元素的百分含量不变。
(3) 最简式相同的有机物,当组成混合物时,只要质量一定,无论以任何配比混合,完全燃烧后,生成CO2的量一定,耗O2量相同。
(4) 等质量的最简式相同的化合物燃烧时耗氧量相同。
5.(单)烯烃的特点
(1) 最简式相同:CH2
(2) C、H元素的百分含量一定。
(3) 燃烧后生成的CO2和H2O(g)的物质的量、气体体积或压强相等。
2CnH2n+3nO2 ® 2nCO2+2nH2O
(4) 等质量的不同烯烃耗氧量同。
6.烃中
(1) 氢原子数必为偶数。
(2) 含氢量w(H):烷烃>烯烃>炔烃>芳烃
烷烃中:M,w(H) ¯
烯烃中:w(H)不变,都是14.3%
炔烃和芳香烃中,M ,w(H)
CH4的w(H)最大,为25%;C2H2和C6H6的w(H)最小,为7.7%
(3) 含碳量w(C):芳烃>炔烃>烯烃>烷烃
烷烃中:M, w(C)
烯烃中:w(C)不变,都是85.7%
炔烃和芳香烃中,M ,w(C) ¯
CH4的w(C)最小,为75%;C2H2和C6H6的w(H)最大,为92.3%
7.求烯烃分子中的双键数
双键数=![]()
8.一个碳原子上有两个羟基就不稳定,一个碳原子上连有双键和羟基(如稀醇)的有机物也不稳定。
9.羟基多了可能产生甜味。
(1) 分子结构中含有多个羟基,且具有甜味的物质有:蔗糖、果糖、葡萄糖、麦牙糖(木糖、木糖醇);(不能食用的)甘油、乙二醇。
(2) 分子结构中含有多个羟基,但不具有甜味的物质有:淀粉、纤维素(部分纤维素不能食用)。
以上十种物质中,甘油、乙二醇、木糖醇是醇,其余属糖类。
(3) 有甜味但不属于糖类的是,可食用的是糖精(邻磺酸苯酰亚胺),不要食用的是乙烯、乙醚、氯仿。
10.有机物的酸性
(1) 羧酸是一类有机物,其中甲酸最强,除此以外的一般规律是:芳香酸和二元酸都强于一元酸,饱和一元羧酸中,随相对分子质量的增加,酸强度减弱。
饱和一元羧酸中,甲酸、乙酸和丙酸能与水混溶。随着相对分子质量的增加,饱和一元羧酸在水中的溶解度迅速减小,最后趋近于零。
(2) 酚类具有酸性,但苯酚(石炭酸)比碳酸还弱,它不能使酸碱指示剂褪色。
11.高分子化合物
(1) 高分子化合物是由组成(链节)相同,但相对分子质量不等的同种高分子组成的混合物。
(2) 平均相对分子质量链节质量×平均聚合度
加聚高分子:![]() =M(单体)×平均聚合度
=M(单体)×平均聚合度
缩聚高分子:![]() <M(单体)×平均聚合度
<M(单体)×平均聚合度
(3) 乙烯类高分子: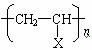
当X为H,即聚乙烯 ![]()
当X为CH3,即聚丙烯 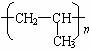
当X为Cl,即聚氯乙烯 ![]()
当X为OH,即聚乙烯醇 ![]()
当X为CN,即聚丙烯腈 ![]()
当X为COOR,即聚丙烯酸酯 ![]()
当X为C6H5,即聚苯乙烯 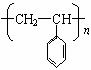
12.发生卤代反应,只能生成一种一卤代物的
(1) 甲烷CH4、乙烯CH2=CH2、乙炔、乙烷CH3—CH3、丙二烯CH2=C=CH2、新戊烷、2,2,3,3—四甲基丁烷
(2) 无支链的环烷烃:环丙烷、环丁烷、环戊烷、环己烷等。
(3) 苯及(指环上)对二甲苯、间三甲苯。
13.端头碳上连有羟基的醇(伯醇)可氧化成醛,仲醇氧化为酮。酮加氢为仲醇,醛加氢还原为伯醇。
14.有机物使溴水褪色的
(1) 不发生化学反应,由于萃取使溴水层褪色,有机层颜色加深的有:苯、甲苯、二甲苯、环己烷、乙酸乙酯、CCl4、直馏汽油等。
(2) 发生取代反应使溴水褪色的有:苯酚。
(3) 发生氧化还原反应使溴水褪色的有:SO2、H2S。但KI溶液与溴水反应生成碘水,颜色加深。
15.颜色反应或显色反应
(1) 淀粉+碘 ® 蓝色。
(2) 苯酚+FeCl3溶液 ® 紫色。
(3) 蛋白质(分子内含苯环)+浓硝酸 ® 黄色。
(4) 乙二醇、甘油、葡萄糖等多羟基化合物加入新制的Cu(OH)悬浊液生成绛蓝色溶液。
16.有机物与有关试剂的反应
(1) 溴水:遇烯、炔等不饱和烃褪色,遇苯酚溶液产生白色沉淀。
(2) 纯溴:与饱和烃和芳香烃发生取代反应。
(3) 酸性高锰酸钾溶液:遇烯、炔等不饱和烃褪色,遇苯的同系物反应褪色。能氧化醇、醛、还原性糖等。
(4) 金属钠:能与羟基化合物(醇、酚、羧酸、甘油)反应放出氢气。
(5) 新制Cu(OH)2悬浊液:常温下遇多元醇、葡萄糖等均能反应,生成绛蓝色溶液;与醛、葡萄糖、甲酸、甲酸酯、甲酰胺和果糖在加热条件下均能反应,生成砖红色沉淀;能与乙酸发生中和反应。
(6) 银氨溶液:与醛、葡萄糖、甲酸、甲酸酯、甲酰胺和果糖在加热条件下均能发和银镜反应,
(7) 氢氧化钠溶液:与羧酸、石炭酸反应。卤代烃、酯可在碱溶液中加热发生水解反应。
(8) 碘水:遇淀粉变蓝。
(9) 石蕊(甲基橙)试液:低级酸溶液可使之变红。
(10) FeCl3溶液:遇苯酚溶液变紫色。
17.有机物与有关试剂的反应
(1) 溴水:遇烯、炔等不饱和烃褪色,遇苯酚溶液产生白色沉淀。
(2) 纯溴:与饱和烃和芳香烃发生取代反应。
(3) 酸性高锰酸钾溶液:遇烯、炔等不饱和烃褪色,遇苯的同系物反应褪色。能氧化醇、醛、还原性糖等。
(4) 金属钠:能与羟基化合物(醇、酚、羧酸、甘油)反应放出氢气。
(5) 新制Cu(OH)2悬浊液:常温下遇多元醇、葡萄糖等均能反应,生成绛蓝色溶液;与醛、葡萄糖、甲酸、甲酸酯、甲酰胺和果糖在加热条件下均能反应,生成砖红色沉淀;能与乙酸发生中和反应。
(6) 银氨溶液:与醛、葡萄糖、甲酸、甲酸酯、甲酰胺和果糖在加热条件下均能发和银镜反应,
(7) 氢氧化钠溶液:与羧酸、石炭酸反应。卤代烃、酯可在碱溶液中加热发生水解反应。
(8) 碘水:遇淀粉变蓝。
(9) 石蕊(甲基橙)试液:低级酸溶液可使之变红。
(10) FeCl3溶液:遇苯酚溶液变紫色。
18.有机物的俗名
沼气、坑气——甲烷 电石气——乙炔 酒精——乙醇 木醇——甲醇 甘油——丙三醇 蚁醛——甲醛
福尔马林——35%—40%甲醛水溶液 石炭酸——苯酚 蚁酸——甲酸 草酸——乙二酸 安息香酸——苯甲酸
硬脂酸——十八碳酸 软脂酸——十六碳酸 油酸——十八碳烯酸 油脂——高级脂肪酸的甘油酯 肥皂——硬脂酸钠
硬化油——人造脂肪 TNT——2,4,6—三硝基甲苯 苦味酸——2,4,6—三硝基苯酚 硝化甘油——三硝酸甘油酯
尿素——碳酰胺

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
备战高考有机化学,多数同学紧盯高频常见有机物,却常常忽略...
易错01:有机概念易错知识点 (1)有机物中一定含碳元素,含碳...
近期在有机物的命名方面总是存在疑惑,许多资料书与参考资料...
中学的有机化学知识系统性强,用归纳和演绎的方法很容易掌握...
【导读】有机物水解均为取代反应,卤代烃、酯、油脂、糖类、...
在高考题中,有机物的命名是我们的重要考点。而含有多官能团...