
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、诱导效应
在有机化合物分子中,由于电负性不同的取代基(原子或原子团)的影响,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应,叫诱导效应。由极性键所表现出的诱导效应称做静态诱导效应,而在化学反应过程中由于外电场(如试剂、溶剂)的影响所产生的极化键所表现出的诱导效应称做动态诱导效应。诱导效应只改变键内电子云密度分布,而不改变键的本性。
诱导效应的特征是是沿着碳链传递,并随着距离的增加其作用迅速减弱。实际上到了第四个碳原子以后这种影响就可以忽略不计了。诱导效应是一种静电作用,是永久性的,属于电子效应的一种。
由于氯的电负性较大,吸引电子的能力较强,电子向氯偏移,使氯带部分负电荷(δ-)、碳带部分正电荷(δ+)。带部分正电荷的碳又吸引相邻碳上的电子,使其发生偏移。
静态诱导效应:由于分子内极性共价键的存在(内在电场)而导致的,静态分子固有的性质。对化合物反应活性的影响具有两面性,在一定条件下可增加反应活性,也可能会降低反应活性。
动态诱导效应:是发生在化学反应时,由于外界电场的出现而发生的。通常只是在进行化学反应的瞬间才表现出来,所起的作用大都是加速反应的进行。
取代基的诱导效应强弱有如下规律:
1、同族元素中,原子序数越大,吸电子诱导效应越弱;同周期元素中,原子序数越大,吸电子诱导效应越强。
2、基团不饱和程度越大,吸电子诱导效应越强。这是由于各杂化态中S轨道成分不同而引起的,S成分越高,吸电子能力越强。
3、正电荷基团和含配位键(直接相连)的基团具吸电子诱导效应,负电荷基团具给电子诱导效应。
4、烷基具给电子诱导效应和给电子超共轭效应。
吸电子基团:—NO2>—CN>F>Cl>Br>I>—C≡CH>—OCH3>—C6H5>—CH=CH2>H。
斥电子基团:(CH3)3C—>(CH3)2CH—>CH3CH2—>CH3—>H。
诱导效应对有机酸的酸性强弱影响很大。凡是能引起羰基碳原子上电子云密度降低的诱导效应都能使酸性增强,能引起羰基碳原子上电子云密度升高的诱导效应时酸性减弱。这种影响越大,酸性强弱的变化就越大。
例如,氯原子取代乙酸的α-H后,生成氯乙酸,由于氯的-I效应通过碳链传递,使羧基中O—H键极性增加,氢更容易以质子形式解离下去,从而酸性增强,致使ClCH2COOH的酸性强于CH3COOH的酸性。
诱导效应是一种静电诱导作用,其作用随所经距离的增大而迅速减弱。诱导效应在一个σ键体系中传递时,一般认为每经过一个链上原子,即降低为原来的约三分之一。通常以ε或1/α来表示递降率。经过n个原子后,其诱导效应只有原来的(1+α)n。一般认为,经过三个原子后诱导作用可忽略。
二、共轭效应
共轭效应(Conjugated Effect) ,又称离域效应,是指共轭体系中由于原子间的相互影响而使体系内的π电子(或P电子)分布发生变化的一种电子效应。凡共轭体系上的取代基能降低体系的π电子云密度,则这些基团有吸电子共轭效应,用-C表示,如-COOH,-CHO,-COR;凡共轭体系上的取代基能增高共轭体系的π电子云密度,则这些基团有给电子共轭效应,用+C表示,如-NH2,-R、-OH。
H2C=CH2,π键的两个π电子的运动范围局限在两个碳原子之间,这叫做定域运动。
CH2=CH-CH=CH2 中,可以看作两个孤立的双键重合在一起,π电子的运动范围不再局限在两个碳原子之间,而是扩充到四个碳原子之间,这叫做离域现象。
共轭分子中任何一个原子受到外界试剂的作用,其它部分可以马上受到影响。这种电子通过共轭体系的传递方式,叫做共轭效应。沿共轭体系传递不受距离的限制。
共轭效应,由于形成共轭π键而引起的分子性质的改变叫做共轭效应。共轭效应主要表现在两个方面。
①共轭能:形成共轭π键的结果使体系的能量降低,分子稳定。例如CH2=CH—CH=CH2共轭分子,由于π键与π键的相互作用,使分子的总能量降低了,也就是说,CH2=CH—CH=CH2分子的能量比两个不共轭的CH2=CH2分子的能量总和要低。所低的数值叫做共轭能。
②键长:从电子云的观点来看,在给定的原子间,电子云重叠得越多,电子云密度越大,两个原子结合得就越牢固,键长也就越短,共轭π键的生成使得电子云的分布趋向平均化,导致共轭分子中单键的键长缩短,双键的键长加长。
共轭效应是电子效应的一种。组成共轭体系的原子处于同一平面,共轭体系的P 电子,不只局限于两个原子之间运动,而是发生离域作用,使共轭体系的分子产生一系列特征,如分子内能低、稳定性高、键长趋于平均化,以及在外电场影响下共轭分子链发生极性交替现象和引起分子其他某些性质的变化,这些变化通常称为共轭效应。共轭效应是指在共轭体系中电子离域的一种效应是有机化学中一种重要的电子效应。它能使分子中电子云密度的分布发生改变(共平面化、趋于平均),内能减少,键长趋于平均化,折射率升高,整个分子更趋稳定。
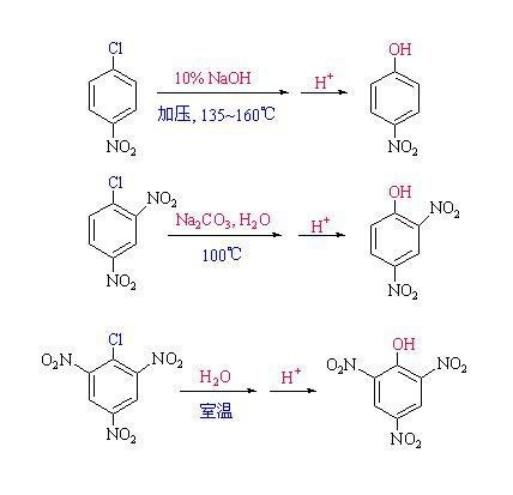
正常共轭效应
又称π-π共轭。是指两个以上双键(或叁键)以单键相联结时所发生的π电子的离位作用。C.K.英戈尔德称这种效应为中介效应,并且认为,共轭体系中这种电子的位移是由有关各原子的电负性和p轨道的大小(或主量子数)决定的。Y原子的电负性和它的P轨道半径愈大,则它吸引π电子的能力也愈大,愈有利于基团-X=Y从基准双键A=B-吸引π电子的共轭效应(如同右边的箭头所示)。与此相反,如果A原子的电负性和它的P轨道半径愈大,则它释放π电子使其向y原子移动的能力愈小,愈不利于向-X=Y基团方向给电子的共轭效应。中间原子B和X的特性也与共轭效应直接相关。多电子共轭效应又称p-π共轭。在简单的多电子共轭体系中,Z为一个带有P电子对(或称N 电子)的原子或基团。这样的共轭体系中,除z能形成d-π共轭情况外,都有向基准双键A=B-方向给电子的共轭效应。Z原子的一对P电子的作用,类似正常共轭体系中的-X=Y基团。
超共轭效应
其中一种为σ-π共轭。它是由一个烷基的C-H键的σ键电子与相邻的半满或全空的P轨道互相重叠而产生的一种共轭现象。依照多电子共轭的理论,一个C-H键或整个CH3基团可作为一个假原子来看待。超共轭效应存在于烷基连接在不饱和键上的化合物中,超共轭效应的大小由烷基中α-H原子的数目多少而定,甲基最强,第三丁基最弱。超共轭效应比一般正常共轭效应和多电子共轭效应弱得多。
同共轭效应
又称p轨道与p轨道的σ型重叠。甲基以上的烷基,除有超共轭效应外,还可能产生同共轭效应。所有同共轭效应,原是指β碳原子上的C-H键与邻近的π键间的相互作用。大量的化学活性和电子光谱的数据表明,在丙烯基离子和类似的烯羰基中,存在一种特殊的P-π或π-π共轭现象,即所谓同共轭效应:
在丙烯基离子中是烯碳原子上的p轨道,与正碳离子(β)上的空P轨道,作σ型的部分重叠;而在类似的烯羰基中,则是羰基碳原子的p轨道与烯碳原子(β)的p轨道作σ型的部分重叠:这种共轭效应的影响比超共轭效应还小。烷基与烯链间的整个共轭效应,应包括超共轭效应和同共轭效应。
d-p共轭
又称d轨道接受共轭。是指一个原子的p轨道与另一个原子的d轨道重叠而产生的一种共轭现象,例如有机硅化合物结构中的d-p共轭;在这里,苯环上的一部分π电子云进入硅的3d轨道,形成d-p共轭,使硅原子与苯环结合得更牢。此外,共轭效应还分静态和动态两类。静态共轭效应存在于未反应的共轭分子中,它是共轭分子中π电子的高度活动性和π电子发生位移的结果。动态共轭效应指在起化学反应的一瞬间,由于进攻试剂的作用,使共轭体系中π电子密度重新分布所引起的一种共轭现象。
三、诱导效应与共轭效应的异同
(1)不同之处
诱导效应:存在σ键中;通过原子间电负性的差异而导致键的极性改变使整个分子电子云发生移动;是短距离效应,一般有3个碳原子后基本消失;极化变化是单一方向。
共轭效应:存在于共轭体系中;通过π电子的运动,沿着共轭链传递;强度一般不因共轭链的长度而受影响,属长距离电子效应;极性交替出现。
(2)相同之处
两者都存在吸电子效应和斥电子效应。
通常在讨论诱导效应和共轭效应时,一般是分别讨论,但有时在一个分子中既有诱导效应,还存在共轭效应,它们相互影响,相互制约。
共轭效应的强弱判断为:
1、原子电负性的影响。原子电负性越大,吸电子能力越强,从而给电子的共轭效应越弱。
2、不饱和度的影响体系的不饱和度越大,共轭体系越大,从而共轭效应也越大。
3、取代基所带电荷的影响。负电荷越多,给电子的共轭效应越强;正电荷越多,吸电子的共轭效应越强;通常负电荷给电子的共轭效应大于中性分子。
4、原子能级差异的影响。原子能级差异越小,共轭效应越强。
竞争关系
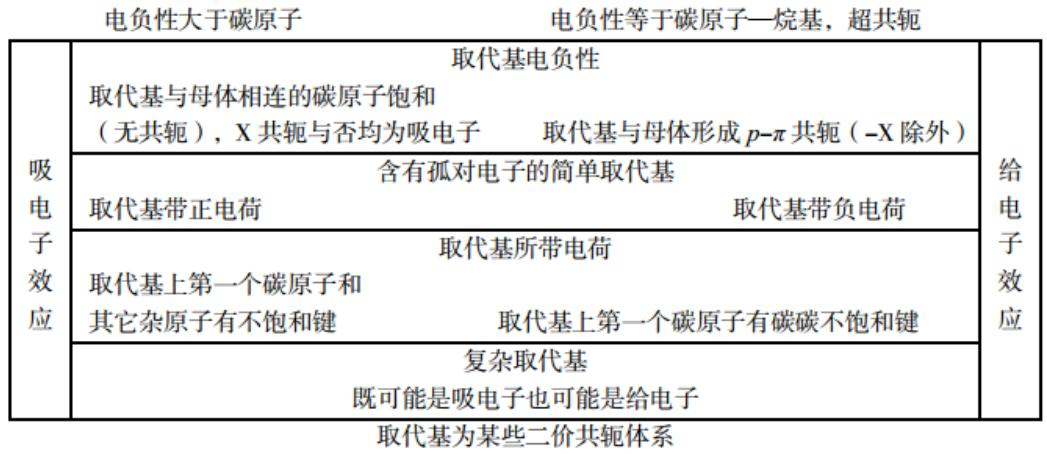
通过对诱导效应和共轭效应的分析,总结出便于区分二者的竞争关系由图3可见,从左边看,结果为吸电子效应,有以下几种情况:
(1)仅有诱导效应而无共轭效应。此类取代基电负性大于碳,且母体中与取代基相连的第一个碳原子饱和。
(2)取代基为给电子的共轭效应小于吸电子的诱导效应的基团(+C<-I)。若卤素取代基的邻碳链或环尚未饱和,则卤素的吸电子的诱导效应大于供电子的共轭效应,总体表现为吸电子效应。
(3)取代基为既有吸电子的共轭效应又有吸电子的诱导效应的基团(-C+ -I)。此类基团通常为带正电荷的基团或取代基第一个碳和非碳原子有不饱和键的基团。
从右边看,结果为给电子效应。
(1)仅有共轭效应而无诱导效应。这就是超共轭效应,其大小排列顺序为:(CH3)3C->(CH3)2CH->CH3CH2-。
(2)取代基为能产生р-π共轭的除卤素外的其它端基有孤对电子的简单基团。此类取代基多为有孤对电子的基团或负离子,如氨基、烷氧基、氧负离子和碳负离子等。
(3)取代基为能产生р-π共轭的某些复杂基团此类取代基大多比较复杂,基团中一般包含有孤对电子的原子以及碳碳不饱和键,形成р-π共轭。既可能是吸电子效应也可能是给电子效应。通常为某些二价共轭体系基团
四、应用
一般来说:
1、体系越缺电子,酸性越强;体系越富电子,碱性越强。
2、缺电子的体系使其电子越多越稳定,给电子基团能使该体系更稳定;富电子的体系使其电子越少越稳定,吸电子基团能使该体系更稳定。
3、越稳定的物质越容易生成。反应过程中,稳定中间体的生成量最多,反应速率也最快,有些物质可能会通过重排生成更稳定的中间体;反应的最终产物以最稳定的物质为主。
举例:比较下列化合物的酸性并排序。
(A)间硝基苯甲酸;(B)对硝基苯甲酸;
(C)邻硝基苯甲酸;(D)苯甲酸。
答案:C>B>A>D
解析:芳环羧酸的邻位异构体的酸性是最强的,原因为:
(1)诱导效应。邻位取代时,羧基和硝基的距离太近,导致羧基碳氧双键上的π电子难以和苯环上的π电子较好地共轭,故以诱导为主。取代基吸引羧基上的电子云,从而增大了酸的解离;
(2)共轭效应。间位和对位的诱导效应很弱,以共轭效应为主,且间位共轭效应大于对位。共轭效应使得羰基上的电子云密度增大,对羧基的吸引力减小,故而使得所示的酸性解离减弱。
五、空阻效应
空间位阻效应又称立体效应。空间位阻效应主要指分子中某些原子或基团彼此接近而引起的空间阻碍作用。如酶反应中空间位阻会降低其催化活性。
在配位化合物中,当向一个配体引入某些较大基团后,由于产生空间位阻,影响它与中心原子形成配位化合物。空间产生影响的事实,每个原子在分子中占有一定的空间。如果原子是太接近了,两个相邻的原子就会形成重叠的电子云(表现为斥力),这可能会影响分子和首选形状(构)的反应。
因分子中靠近反应中心的原子或基团占有一定的空间位置,而影响分子反应活性的效应。降低分子反应活性的空间效应称“空间阻碍”。例如,邻位双取代的苯甲酸的酯化反应要比没有取代的苯甲酸困难得多。同样,邻位双取代的苯甲酸酯也较难水解。这是由于邻位上的基团占据了较大的空间位置,阻碍了试剂(水、醇等)对羧基碳原子的进攻。
相反,反应物转变为活性中间体的过程中,如降低反应物的空间拥挤程度,则能提高反应速度。这种空间效应称“空间助效”。例如,叔丁基正离子比甲基正离子容易形成,这是因为在形成叔丁基正离子的反应中,空间拥挤程度降低得多一些,而在形成甲基正离子的反应中,空间拥挤程度相对降低得少一些。空间效应是影响有机反应历程的重要因素。
空间位阻效应又称立体效应。主要是指分子中某些原子或基团彼此接近而引起的空间阻碍和偏离正常键角而引起的分子内的张力。如酶反应中空间位阻会降低其催化活性。在配位化合物中,当向一个配体引入某些较大基团后,由于产生空间位阻,影响它与中心原子形成配位化合物。
空间阻碍一般会降低反应速率,例如,在溴代烷的双分子亲核取代反应中,由于烷基体积的增大,引起空间阻碍,使反应速率变小。
然而在有些反应中,立体效应有可能增加反应速率,例如,在单分子亲核取代反应中,三烷基取代卤代烷的烷基增大时,由于取代基之间的空间斥力,引起碳卤键的异裂,导致碳正离子的形成,从而提高了反应速率。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、诱导效应 在有机化合物分子中,由于电负性不同的取代基...
在中学化学的几种炔烃的物理常数表中,记载有乙炔的熔点(...
在高考中考查: 近几年新高考中最早出现非苯环芳香烃相关考查...
立体结构差异 椅式环己烷结构中,碳原子构成的环近似于一个三...
电子效应,在大多数反应中,由于取代基(与氢原子相比)倾向...
一、芳香烃的定义 具有芳香性的烃称为芳香烃,一般是指分子中...