
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
铜的化合物有硫酸铜(CuSO4)、醋酸铜[(CH3COO)2Cu]、氧化铜(CuO)和氧化亚铜(Cu2O)、氯化铜(CuCl2)和氯化亚铜(CuCl)、硝酸铜[Cu(NO3)2]、氰化铜[Cu(CN)2]、脂肪酸铜、环烷酸铜(C22H14CuO4)等。
铜(I)
铜(I)通常称为亚铜,氯化亚铜(CuCl)、氧化亚铜(Cu2O)、硫化亚铜(Cu2S)都是常见的一价铜化合物。[Cu(NH3)2]+是亚铜和氨的配离子,无色,易被氧化,在酸性溶液中自行歧化,生成Cu(II)和Cu单质。
以氯化亚铜为例:在热的浓盐酸中,CuCl2可被单质铜还原为无色的铜氯络合离子,稀释后可得难溶于水的白色沉淀(CuCl)。此外,还原剂氯化锡
(SnCl2)亦可将氯化铜还原为氯化亚铜。
Cu2++Cu+4Cl-→2[CuCl2]-
2[CuCl2]-→2CuCl↓+2Cl-
Cu2++Cu+2Cl-→2CuCl↓
SnCl2+2CuCl2→2CuCl↓+SnCl4
铜(II)
铜(II)是铜最常见的价态,它可以和绝大部分常见的阴离子形成盐,如众所周知的硫酸铜,存在白色的无水物和蓝色的五水合物;碱式碳酸铜,又称铜绿,有好几种组成形式,而氯化铜和硝酸铜亦是重要的铜盐。
铜(II)可以形成一系列的配离子,如[Cu(H2O)6]2+(蓝色)、[CuCl4]2-(黄绿)、[Cu(NH3)4]2+(深蓝)等,它们的颜色也不尽相同。
在Cu(Ⅱ)的卤化物中,最重要的是氯化铜,无水氯化铜为棕黄色固体,可由单质铜与氯气化合而成,为共价化合物,结构是CuCl4平面组成的长链。
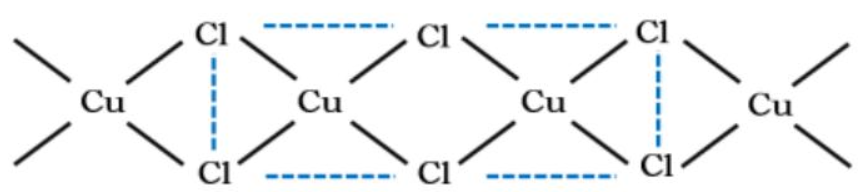
氯化铜不仅易溶于水,还能溶于乙醇、丙酮等有机物。高浓度的氯化铜溶液常因形成配离子而呈黄色。
Cu2++4Cl-→[CuCl4]2-
此外,氯化铜还具有一定的氧化性,可发生氧化还原反应。
CuCl2 + H2 → Cu +2HCl(加热)
CuCl2 + Zn→ ZnCl2+Cu(置换反应)
CuCl2(盐酸酸化) + Cu →2CuCl(白色结晶)
2CuCl2 +2KI→2CuCl↓+2KCl+I2↓
2CuCl2 + FeS→Cu2Cl2+FeCl2+S↓
2CuCl2 +Cu2S→Cu2Cl2+S↓
铜(III)
Cu(III)有8个3d 电子,它们排列为高自旋(两个未成对电子)或低自旋(抗磁性)两种构型,前一种较少见,六氟合铜(III)酸钾(K3CuF6)是唯一的顺磁性铜(III)配合物(μ= 2.8b M),是呈淡绿色的固体,在250 ℃时,由氟与氯化钾和氯化铜3:1混合物反应制备,该化合物易水解并放出氧。在1 atm的氧气气氛中加热过氧化钾与氧化铜的混合物至400-450℃24小时,可制得高铜酸钾KCuO2,它是一种晶状浅蓝色反磁性化合物。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
铜的化合物有硫酸铜(CuSO 4 )、醋酸铜[(CH 3 COO) 2 Cu]、氧化铜(CuO...
你是否还记得中学课本里的分类:碱性氧化物是能与酸反应生成...
...
一、建立轴线:形态随pH切换 中间: Al(OH) 3 (沉淀态) 左侧(强酸...
钛(化学符号 Ti,原子序数 22)是一种具有优异综合性能的过渡...
就高考备考中,尤其关于镁的知识给同学们列出以下复习提纲:...