
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
共价键就是俩原子凑一对电子,八隅体是铁律,氢只能连1个原子——直到乙硼烷这个叛逆分子跳出来,直接把这套规则掀了个底朝天。
硼的价电子只有3个,氢1个,乙硼烷总价电子仅12个。而和它只差一个字母的乙烷,总价电子14个,刚好凑够7根正常共价键(二原子二电子)(2c—2e)按老规则,乙硼烷要复刻乙烷结构,硬生生差2个电子。
为了解释这个“电子赤字”,化学家吵了快30年,直到电子衍射技术拍出了它的“高清身份证”——所有人都傻了:它根本不是乙烷的平面结构,而是长了两个“氢桥”的奇葩桥式结构。
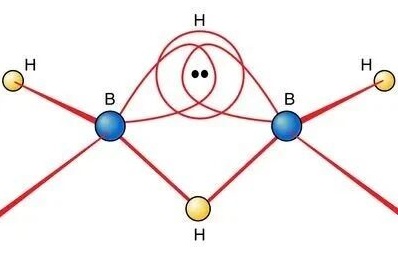
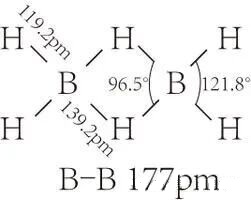
两个硼原子都做了sp3杂化,先各拿2个杂化轨道,和4个氢原子形成正常的sigma键,刚好用掉8个电子。
而剩下的4个电子、2个硼的剩余轨道、2个氢原子,乙硼烷直接玩了波化学界的「共享经济」:两个硼原子+一个氢原子,三个轨道肩并肩重叠,3个原子共用2个电子,形成了神奇的三中心两电子(3c—2e)氢桥键。
两个氢桥键刚好用完剩下的4个电子,12个电子完美分配,直接把缺电子的死局盘活了,同时,两个氢桥键所在的平面,和4个端基氢的平面完全垂直,对称性拉满。
这根奇怪的键,它直接颠覆了化学家对共价键的固有认知,催生了全新的缺电子多中心键化学,研究者利普斯科姆也靠着对硼烷的系统研究,拿下了1976年诺贝尔化学奖。
值得一提的是,氢桥键比普通共价键弱得多,也让乙硼烷成了实打实的“暴脾气”:空气中能自燃,遇水会爆炸,但同时也是有机合成里超好用的还原剂。
说到底,乙硼烷最迷人的地方,从来都不是复杂的结构,而是它告诉我们:化学从来没有一成不变的铁律。能把缺电子的劣势,玩成独一份的成键绝活,这种不走寻常路的智慧让人不 禁感慨自然界的鬼斧神工。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
共价键就是俩原子凑一对电子,八隅体是铁律,氢只能连1个原子...
d 轨道杂化是原子轨道杂化的重要类型,以中心原子价层中的 ...
一般来说,同主族元素形成的R-R键键能从上至下,键长逐渐增大...
离子极化与影响元素 离子极化理论是离子键理论的重要补充。...
原子之间形成共价键时,若共用电子对只是由一方原子提供电子...
p区元素化学的学习中我们常常发现,很多非金属含氧酸的游离酸...