
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
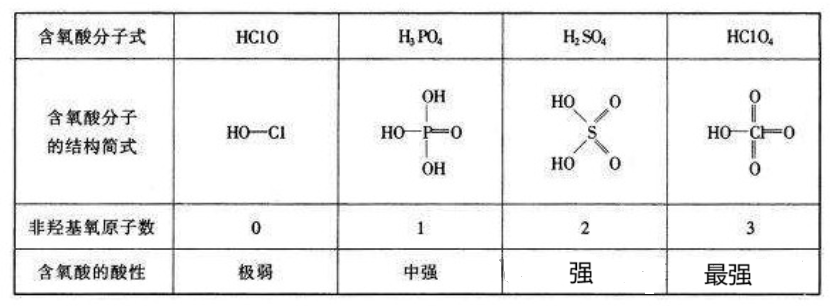
鲍林在研究含氧酸时,将其化学式一般写作 HₘROₙ,其中 R 代表中心原子,羟基(–OH)与非羟基氧原子共存。鲍林发现,含氧酸的酸性主要取决于分子中非羟基氧原子(n)的数量。当 n 增加时,R 原子的氧化态提高,其电负性增强,从而对羟基氧起到较强的电子拉吸作用,使 O–H 键极化加剧,H⁺ 更容易离解。简言之,非羟基氧原子越多,酸性越强。例如:
硅酸(H₄SiO₄)
中心原子硅的氧化态较低(n = 0),酸性非常弱;
磷酸(H₃PO₄)
含有 1 个非羟基氧(n = 1),酸性中等;
硫酸(H₂SO₄)
含有 2 个非羟基氧(n = 2),酸性强;
高氯酸(HClO₄)
含有 3 个非羟基氧(n = 3),属于极强酸。
鲍林对强弱酸的划定
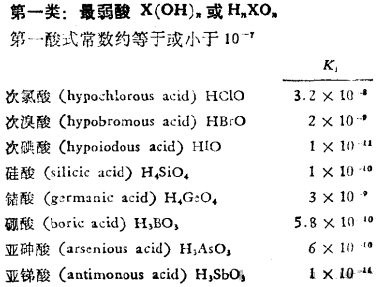
按上述规则,鲍林的划分如下:
最弱酸:
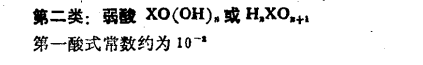



例外的酸:


 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。1.皓矾: ZnSO 4 ·7H 2 O 2.钡餐,重晶石: BaSO 4 3.绿矾,皂矾,青矾: FeSO 4 ·7...
少量、适量、足量和过量,这几个词是化学实验和计算中的核心定量描述,区别主要在于反...
一、基础概念:从 “温度强度” 看五者的核心差异 首先需明确:这五种操作本质都是 “...
【导读】“强酸制弱酸”是复分解反应的常见规律,其本质是强酸电离出的H更易与弱酸根...
在高中化学中,很多同学从初中就学习了复分解反应, 都知道复分解反应中“强酸制弱酸...
1.水银:汞Hg 2.过氧一硫酸:过氧硫酸过硫酸 H 2 SO 5 3.白金:主要成分铂 Pt 4.苯:C...