
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
通过初中化学的学习,我们已经知道三大强酸为盐酸(HCl)、硫酸(H2SO4)、硝酸(HNO3),在高中的化学学习中,又有三种酸也加入强酸行列,分别是高氯酸(HClO4)、氢溴酸(HBr)、氢碘酸(HI),其中高氯酸的酸性为所有无机酸中最强,而氢溴酸、氢碘酸的酸性则比盐酸还要强。下面我们就一起具体地认识一下这六大强酸及应用!
1、盐酸 HCl
简介:
1、盐酸是氢氯酸的俗称,是氯化氢(HCl)气体的水溶液,为无色透明的一元强酸;工业上用的盐酸常因含有FeCl3等杂质而略带黄色。有刺激性气味、有酸味。常用的浓盐酸中的质量分数为37%~38%,密度为1.19g/cm3,物质的量浓度约为12.0mol•L-1。
注意:浓盐酸易挥发,敞口放置溶质HCl氯化氢质量减小,溶剂质量不变,溶液溶质质量分数变小。浓硫酸具有吸水性,敞口放置吸收空气中的水,溶剂质量增加,溶液溶质质量分数变小。
2、盐酸的首次发现:公元800年的一个信奉伊斯兰教,名为贾比尔·伊本·哈扬的阿拉伯化学家/炼金师,将氯化钠和硫酸混合从而第一次制取了盐酸。
3、盐酸是一种重要的化工产品,用于金属除锈、制造药物(如盐酸麻黄素、氯化锌)等。人体胃液中也含有少量的盐酸,帮助消化。
4、盐酸的特性
(1)浓盐酸具有挥发性。打开浓盐酸的试剂瓶,会观察到瓶口有白雾出现,那是因为从浓盐酸瓶中挥发出的氯化氢气体与空气中的水蒸气接触,形成盐酸小液滴,故在开启的瓶口处形成白雾,不是白烟。在化学中“烟”是指细小的固体颗粒,“雾”是指液态的小液滴。
(2)浓盐酸具有强烈的腐蚀性。使用时要注意安全。
(3)盐酸的通性:①使指示剂变色;②与金属反应制取氢气;③与金属氧化物反应生成相应的盐和水;④与盐反应,生成另一种酸和另一种盐。
(4)还原性
①4HCl(浓)+MnO2![]() MnCl2+2H2O+Cl2↑(实验室制取氯气)
MnCl2+2H2O+Cl2↑(实验室制取氯气)
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
③NaClO+2HCl=NaCl+Cl2↑+H2O(氯元素的归中反应)
(5)强酸制弱酸:CH3COONa+HCl=CH3COOH+NaCl
5、工业制盐酸:H2+Cl2 2HCl然后用水吸收,在合成塔内完成。
2HCl然后用水吸收,在合成塔内完成。
6、实验室制盐酸:2NaCl(s)+H2SO4(浓)=Na2SO4+2HCl↑
7、离子反应中的拆与不拆:浓盐酸浓度为37%~38%,溶液中主要以离子形式存在,所以在书写离子方程式时浓盐酸要拆开。如浓盐酸与共热制氯气4HCl(浓)+MnO2![]() MnCl2+2H2O+Cl2↑的离子方程式为4H++ 2Cl-+ MnO2
MnCl2+2H2O+Cl2↑的离子方程式为4H++ 2Cl-+ MnO2![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
2 、H2SO4硫酸
简介:
1、无水硫酸为无色粘稠的油状液体,为二元无机强酸。有酸味,实验室常用浓硫酸的溶质质量分数为98%,密度为1.84g/cm3,物质的量浓度约为18.4mol•L-1。
2、浓硫酸在打开瓶盖后瓶口上方无明显现象。
3、硫酸的首次发现:硫酸发现于公元8世纪,阿拉伯炼丹家贾比尔通过干馏硫酸亚铁晶体得到硫酸。
4、硫酸是一种重要的化工原料,用于生产化肥、农药、火药、染料、冶炼金属、精炼石油和金属除锈等。利用浓硫酸的吸水性,实验室中常用它做干燥剂。
5、浓硫酸的特性及应用
(1)浓硫酸具有吸水性,可做干燥剂。如果浓硫酸长期露置在空气中,会吸收空气中的水蒸气,使浓硫酸的溶质质量分数变小。浓硫酸能够干燥不和它反应的气体,如O2、H2、CO2、等,但不能干燥能和它反应的NH3.
(2)浓硫酸具有脱水性。它能夺取纸张、木材、皮肤(都由碳、氢、氧等元素的化合物组成)里的水分,生成黑色的炭。所以使用浓硫酸时要格外小心,如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量和水冲洗,然后涂上3%~5%的碳酸氢钠溶液。
C12H22O11==12C+11H2O ;C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(3)浓硫酸具有强烈的腐蚀性。使用时要注意安全。
(4)浓硫酸的稀释:浓硫酸溶于水时会放出大量的热,这是因为硫酸与水结合成水合物的过程中放出的热量大于其分子扩散过程中吸收的热量。所以在稀释浓硫酸时绝对不可将水倒入浓硫酸中,而是要把浓硫酸沿器壁慢慢注入水里,并用玻璃棒不断搅拌,使产生的大量的热迅速扩散。
注意:在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢倒入水中,并不断搅拌。切不可将水倒进浓硫酸中,可简单的记为十二字真言“酸入水,沿器壁,缓慢倒,不断搅”。如果水倒进浓硫酸中,由于水的密度小,浮在硫酸的上面,硫酸溶解时放出的热量不易散失,使水暴沸,带着酸向四处飞溅,有可能发生意外。
(5)常温下浓硫酸能使铁、铝等金属钝化。
(6)浓硫酸的强氧化性和酸性
①加热时,浓硫酸可以与除金、铂之外的所有金属反应,生成高价金属硫酸盐,本身一般被还原成二氧化硫。
Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
在上述反应中,硫酸表现出了强氧化性和酸性。
②热的浓硫酸可将碳、硫、磷等非金属单质氧化到其高价态的氧化物或含氧酸,本身被还原为二氧化硫。
C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O ;
CO2↑+2SO2↑+2H2O ;
S+H2SO4(浓) ![]() 2SO2↑+2H2O
2SO2↑+2H2O
2P+5H2SO4(浓)=2H3PO4+5SO2↑+2H2O
在这类反应中,浓硫酸只表现出氧化性。
③与其他还原性物质反应
浓硫酸具有强氧化性,实验室制取硫化氢、溴化氢、碘化氢等还原性气体不能选用浓硫酸。
H2S+H2SO4(浓)=S↓+SO2↑+2H2O 2HBr+H2SO4(浓)=Br2↑+SO2↑+2H2O 2HI+H2SO4(浓)=I2↓+SO2↑+2H2O
(7)作催化剂
①制取乙烯时作催化剂 原理:
CH3CH2OH C2H4↑+H2O
C2H4↑+H2O
生成副产品乙醚: 2CH3CH2OH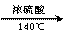 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
净化:杂质为CO2、SO2、H2O,可用NaOH溶液除去CO2、SO2,再用浓硫酸干燥。
【小窍门:要除去中性气体中的酸性气体,用强碱溶液或碱石灰吸收。如:C2H4中的混有的CO2、SO2用NaOH溶液吸收除去。还可用CuSO4或Pb(NO3)2等溶液除去。】
收集:用排水法收集
检验:溴水或酸性KMnO4溶液(褪色)。
②制取乙酸乙酯时作催化剂: CH3COOH + C2H5OH CH3COOC2H5+H2O
CH3COOC2H5+H2O
浓硫酸做催化剂和脱水剂。
③甲苯与浓硝酸在浓硫酸、加热的条件下生成炸药TNT:
④酯类的水解,稀硫酸作催化剂 CH3COOCH2CH3+H2O CH3COOH+ CH3CH2OH
CH3COOH+ CH3CH2OH
(8)铅蓄电池(浓硫酸做电解质溶液)
(负极—Pb,正极—PbO2,电解液—浓硫酸)
总反应:PbO2+Pb + 2H2SO4=2PbSO4+2H2O
放电:
负极:Pb + SO42--2e-=PbSO4
正极:PbO2+4H++ SO42-+ 2e-=PbSO4+2H2O
【放电时二氧化铅电极上发生还原反应,铅电极上发生氧化反应。充电时,二氧化铅电极上发生氧化反应,铅电极上发生还原反应。】
充电:阴极:PbSO4+2H++2e-= Pb+H2SO4
阳极:PbSO4+2H2O-2e-= PbO2+H2SO4+2H+
5、工业制硫酸:
①制取二氧化硫(沸腾炉):24FeS2+11O2 8SO2+2Fe2O3
8SO2+2Fe2O3
②将二氧化硫溶于水变成亚硫酸(接触室):2SO2+O2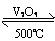 2SO3
2SO3
③亚硫酸氧化得硫酸(吸收塔):SO3+H2O=H2SO4。
6、离子反应中的拆与不拆:浓硫酸、浓磷酸与固体的反应不能写成离子方程式。
如浓硫酸与铜片共热不能写成:Cu+4H++SO42-=CuSO4+SO2↑+2H2O,浓硫酸不拆,应该是:Cu+2H2SO4(浓)=CuSO4+SO2↑+2H2O。
解释:浓硫酸中的水很少,不能电离,以分子的形式存在;该反应生成的水被浓硫酸吸收,所以生成的CuSO4不能也电离。
3、 硝酸 HNO3
简介:
1、硝酸为无色、易挥发、具有刺激性气味的液体,易溶于水。浓硝酸常因为溶解有NO2而呈黄色。质量分数为69%的硝酸为常用浓硝酸。98%以上的硝酸称之为发烟硝酸。
2、硝酸的首次发现:公元八世纪,阿拉伯炼金术士贾比尔·伊本·哈扬(Jabir ibn Hayyan)在干馏硝石的时候发现并制得了硝酸。同时,他也是盐酸、硫酸和王水的发现者。
3、浓硝酸的特性及应用:
(1)浓硝酸不稳定,受热或光照易分解
4HNO3 O2↑+ 4NO2↑+ 2H2O
O2↑+ 4NO2↑+ 2H2O
(2)强氧化性
①3FeO+10HNO3(稀)=3Fe(NO3)3+NO↑+5H2O
硝酸表现出了强氧化性和酸性。
②金属与HNO3反应
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
注意:浓硝酸与Cu反应时,若Cu过量,反应开始时浓硝酸的还原产物为NO2,但随着反应的进行,硝酸变稀,其还原产物将为NO,最终应得到NO2与NO的混合气体,可利用氧化还原反应过程中化合价升降总数相等的守恒规律求解有关Cu、HNO3和混合气体之间的量的关系。
③非金属与HNO3反应
C+4HNO3(浓) =CO2↑+4NO2↑+2H2O,
S+6HNO3(浓) =H2SO4+6NO2↑+2H2O。
(3)钝化
常温时,冷的浓硝酸、浓硫酸可使铝、铁表面生成致密的氧化膜,阻止酸与金属的进一步反应,这种现象叫钝化。钝化其实也是硝酸强氧化性的表现,利用金属Al和Fe的这种性质,我们可以用Al或Fe制的容器来盛装浓硫酸或浓硝酸。
(4)铁与稀硝酸的反应
稀硝酸与少量铁反应:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O
稀硝酸与过量铁反应:3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O
(5)硝基苯
(6)蛋白质的变色反应 浓HNO3只能使含有苯环的蛋白质变黄色。
(7)硝酸酯 硝酸可以与醇发生酯化反应生成对应的硝酸酯。
(8)甲苯与浓硝酸在浓硫酸、加热的条件下生成炸药TNT:
(10)硝酸与纤维素反应生成硝化纤维。
以浓硫酸作催化剂,纤维素与硝酸反应制得纤维素硝酸酯:
5、工业制硝酸
4NH3+5O2 4NO+6H2O (反应条件:800度高温,催化剂铂铑合金作用下)
4NO+6H2O (反应条件:800度高温,催化剂铂铑合金作用下)
2NO+O2=2NO2
3NO2+H2O=2HNO3+NO
6、离子反应中的拆与不拆:浓硝酸,应拆开。
如浓硝酸与铜的反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,写成离子方程式为:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O。
7、离子共存问题
在水溶液中,NO3-本无氧化性,但当水溶液中有大量H+存在时,NO3-就表现出强氧化性,如在有H+、NO3-存在的溶液中不能与Fe2+、S2-、I-、SO32-、Br-等还原性离子共存。
8、关于硝酸的计算 可利用电子得失守恒进行计算。
4 、高氯酸 HClO4
简介:
高氯酸又名过氯酸,化学式为HClO4,无水物为无色透明的发烟液体。高氯酸是一种强酸,有强烈的腐蚀性、刺激性,酸酐为Cl2O7。高氯酸在无机含氧酸中酸性最强。高氯酸是强氧化剂,与有机物、还原剂、易燃物(如硫、磷等)接触或混合时有引起燃烧爆炸的危险。
5、 氢溴酸 HBr
1、氢溴酸(化学式:HBr)是溴化氢的水溶液,微发烟,有刺激性酸味。见光、露置空气或久贮逐渐变黄成棕色。有强还原性。有很强烈腐蚀性。
2、离子反应中的拆与不拆:氢溴酸是强酸,酸性比盐酸还要强,在水中完全电离,所以需拆开。
6、 氢碘酸 HI
简介:
1、氢碘酸(化学式:HI)是碘化氢的水溶液,是种非氧化性酸。氢碘酸是一种强酸,还原性强,还原性大于盐酸和氢溴酸。有强腐蚀性,能灼伤皮肤。
2、离子反应中的拆与不拆:氢碘酸是强酸,酸性比盐酸还要强,在水中完全电离,所以需拆开。
(1)氢碘酸与氢氧化铁反应
化学方程式:6HI + 2Fe(OH)3= 2FeI2+6H2O + I2
离子方程式:6H++ 2I-+ 2Fe(OH)3= 2Fe2++ 6H2O + I2
解释:原因:H+先溶解氢氧化铁;I-有还原性,产物Fe3+有较强氧化性,I-可将Fe3+还原成Fe2+.
(2)氧化铁溶于足量的氢碘酸
Fe2O3+6H++ 2I-= 2Fe2++ I2+3H2O
(3)硝酸铁溶液中加入氢碘酸
①HI过量:
Fe(NO3)3+12HI=FeI2+3NO↑+4H2O+5I2
Fe3++3NO3-+12H++10I-=Fe2++5I2+3NO↑+6H2O
②HI少量:
2Fe(NO3)3+8HI=2Fe(NO3)2+2NO↑+ 4H2O+ 4I2
2Fe3++2NO3-+8H+ + 8I-==2Fe2++2NO↑ +4H2O +4I2

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
锰(Mn)是元素周期表第四周期第 ⅦB 族的过渡金属元素,原子...
镁(Mg,原子序数 12,第 ⅡA 族碱土金属元素)是典型的活泼金...
在第ⅡA族(碱土金属)元素家族中,铍(Be)以其极致的轻金属特性、...
1.皓矾: ZnSO 4 ·7H 2 O 2.钡餐,重晶石: BaSO 4 3.绿矾,皂矾,青矾...
少量、适量、足量和过量,这几个词是化学实验和计算中的核心...
一、基础概念:从 “温度强度” 看五者的核心差异 首先需明确...