
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
[例]现有1L 含SO3为30%的发烟硫酸(密度为1.95g/cm3),要把它稀释成为95%的浓硫酸。求需要往其中加入水的体积。
[分析]学生对“含SO3为30%的发烟硫酸”的意义不太明确。同时,水的密度为1g/cm3,也是隐含的条件,1L 中单位“L”与密度中的单位“cm3”不一致,要换算。没有提示时,很多学生以为30%为SO3,70%为水,结果当然错误;当提示含SO3为30%的发烟硫酸是30%的是SO3,70%的为纯硫酸后,全班也只有10%的同学能解答。为了讲清楚此题,我先用分步计算法讲解,再用稀释规律讲解。从多个角度解析。讲解后90%的同学能够听懂,收到了较好的效果。
[解法一]分步计算法
设发烟硫酸中30%的三氧化硫转化为硫酸时需要水的质量为X,同时生成硫酸的质量为Y。则
SO3+H2O==H2SO4
801898
1000×1.95×30% x y
解得:x=132g,y=717g
30%的三氧化硫转化为硫酸时,纯硫酸的质量共为1950+132=2082g
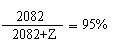
再设还需加水的质量z时,纯硫酸可变为95%的浓硫酸,则有z=110g
故共加水132+110=242g,因为水的密度为1g/cm3,即加入水的体积为242mL
[解法二]稀释规律法
设加水的质量为x,根据稀释前后硫酸的质量不变,则有
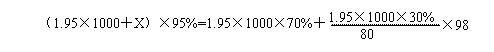
解得:x=242(g),即加入水的体积为242mL。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
硝酸与金属的反应计算,是高考化学氧化还原板块的必考难点,...
由于硝酸具有强氧化性,能与金属活动顺序表中除Pt、Au以外的所...
H 2 O、OH - 或其他含-2价O的化合物常常是氧化还原反应方程式...
[ 例 ] 现有 1L 含 SO 3 为 30% 的发烟硫酸(密度为 1.95g/cm 3 ),要...
一、硫化物 的颜色及溶解性规律: 硫化银 (Ag 2 S) :灰黑色,微溶...
例题 1、 在某100ml的混合液中,硝酸和硫酸的物质量浓度分别是...