
|
学习小专题 |
 次氯酸盐与酸的反应实验探究
日期:2022-08-11 15:55:52
点击:21917
好评:0
次氯酸盐与酸的反应实验探究
日期:2022-08-11 15:55:52
点击:21917
好评:0
一、次氯酸盐与酸的反应 次氯酸是一种酸性很弱,氧化性很强的酸。当次氯酸钙或次氯酸钠的溶液与稀硫酸反应时,能生成次氯酸。其离子方程式是: C1O - + H + = HC1O (1) 该反应的平衡常数K 1 等于次氯酸的电离常数(2.9510 -8 )的倒数,其值为3.3910 7 。 次氯酸钙或...
 弱酸与弱酸盐的反应规律及产物的确定
日期:2021-12-16 08:12:26
点击:15287
好评:0
弱酸与弱酸盐的反应规律及产物的确定
日期:2021-12-16 08:12:26
点击:15287
好评:0
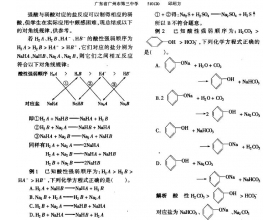
[规律1]根据强置换弱的反应规律和一元弱酸的电离度(或电离常数)可得出如下弱酸的强弱顺序:HNO 2 >HF>HCOOH>C 6 H 5 COOH>CH 3 COOH>HClO>HCN>C 6 H 5 OH>HAlO 2 。依此可判断一元弱酸与一元弱酸盐是否发生反应及其反应的产物。 [规律2]在确定弱酸与多元弱酸...
 强酸制弱酸方程式书写技巧
日期:2020-03-05 18:44:36
点击:4283
好评:1
强酸制弱酸方程式书写技巧
日期:2020-03-05 18:44:36
点击:4283
好评:1
...
 强酸制弱酸的对角线规律(强烈推荐)
日期:2017-09-11 17:08:24
点击:4617
好评:1
强酸制弱酸的对角线规律(强烈推荐)
日期:2017-09-11 17:08:24
点击:4617
好评:1
...
 弱酸制强酸经典赏析
日期:2016-12-28 10:51:48
点击:4101
好评:0
弱酸制强酸经典赏析
日期:2016-12-28 10:51:48
点击:4101
好评:0
1、氢硫酸制硫酸 1.方程式:CuSO 4 +H 2 S== CuS + H 2 SO 4 2.平衡常数K=7.143×10 14 3.显然能发生反应,原因也很简单,Cu离子的存在,促进了氢硫酸的电离,得到强酸(硫酸) 2、醋酸制亚硝酸 1.已知电离常数K(CHCOOH)=1.76×10 -5 ,K(HNO 2 )=4.6×10 -4 2.方程式...
 二氧化碳通入盐或碱溶液中生成何种盐?
日期:2016-11-09 09:08:54
点击:4358
好评:0
二氧化碳通入盐或碱溶液中生成何种盐?
日期:2016-11-09 09:08:54
点击:4358
好评:0
案例1.将少量或过量的CO 2 气体分别通入次氯酸钙溶液中,为什么前者生成正盐CaCO 3 ,后者生成酸式盐Ca(HCO 3 ) 2 ? 反应本质: 少量CO 2 气体:CO 2 +H 2 O+Ca(ClO) 2 ==CaCO 3 ↓+2HClO 过量CO 2 气体:2CO 2 +2H 2 O+Ca(ClO) 2 ==Ca(HCO 3 ) 2 +2HClO 定性分...
 酸的强弱规律及其应用
日期:2015-12-23 11:15:05
点击:22986
好评:0
酸的强弱规律及其应用
日期:2015-12-23 11:15:05
点击:22986
好评:0
酸是化学中的一类重要物质,很多化学反应都与酸有关,常见酸的酸性强弱关系是学习中必须掌握的一个基本知识点。本文将总结中学化学中常见酸的强弱变化规律,并结合具体事例谈谈这些规律的应用。 一、常见酸按酸性强弱的分类 习惯上,按照酸的电离能力的大小,可将酸大致...
 关于苯酚钠溶液与二氧化碳反应的几个疑问
日期:2015-01-13 09:26:58
点击:8354
好评:0
关于苯酚钠溶液与二氧化碳反应的几个疑问
日期:2015-01-13 09:26:58
点击:8354
好评:0
1、为什么苯酚钠溶液中通入CO 2 生成的是NaHCO 3 而不是Na 2 CO 3 ? 答:假设生成碳酸钠和苯酚,则此两者不共存(一个显碱性,一个显酸性),假设不成立. 故苯酚钠溶液中通入CO 2 不生成碳酸钠。(注:假设法是较为有效的学习方法)。实际上若生成碳酸钠,必然是由于苯酚钠与碳酸...
 酸强弱知识的应用
日期:2007-07-15 10:07:18
点击:7987
好评:0
酸强弱知识的应用
日期:2007-07-15 10:07:18
点击:7987
好评:0
常见强酸有 HClO 4 、 HNO 3 、 HCl 、 H 2 SO 4 ,中强酸有 H 2 SO 3 、 H 3 PO 4 ,弱酸有 HF 、 HCOOH 、 CH 3 COOH 、 H 2 CO 3 、 H 2 S 、 HClO 、 C 6 H 5 OH 等,酸碱质子理论认为,能电离出 H + 即是酸,那么广义地讲, NaHCO 3 、 Na 2 HPO 4 、 NaH 2 PO 4...
 强酸制取弱酸的原理及其应用
日期:2007-05-14 14:21:18
点击:26948
好评:2
强酸制取弱酸的原理及其应用
日期:2007-05-14 14:21:18
点击:26948
好评:2
强酸制取弱酸,指的是较强酸(可以是强酸或弱酸)可生成较弱酸。即: 强酸+弱酸盐弱酸+强酸盐 中学化学通常以 H 2 CO 3 、 的酸性作为比较标准,要求掌握常见弱酸酸性强弱顺序: 强酸制弱酸原理的应用主要体现在以下几个方面: 1. 实验室制取某些弱酸 2. 解释现象 漂...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。