
|
学习小专题 |
 “隔线法”分析较强酸制取较弱酸
日期:2023-04-07 10:59:41
点击:276
好评:0
“隔线法”分析较强酸制取较弱酸
日期:2023-04-07 10:59:41
点击:276
好评:0
“隔线法”分析较强酸制取较弱酸。...
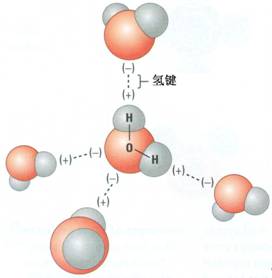 高考讲座:弱酸与盐反应方程式的书写
日期:2023-02-15 11:07:48
点击:89
好评:0
高考讲座:弱酸与盐反应方程式的书写
日期:2023-02-15 11:07:48
点击:89
好评:0
高考讲座:弱酸与盐反应方程式的书写。...
 新课程实验演示:强酸制弱酸
日期:2022-02-18 09:19:14
点击:286
好评:0
新课程实验演示:强酸制弱酸
日期:2022-02-18 09:19:14
点击:286
好评:0
...
 利用“交叉”规律分析“强酸制取弱酸”原理
日期:2021-12-16 09:15:22
点击:3975
好评:0
利用“交叉”规律分析“强酸制取弱酸”原理
日期:2021-12-16 09:15:22
点击:3975
好评:0
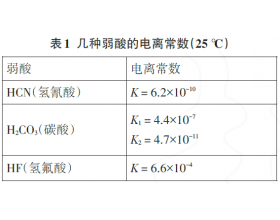
学生对强酸制取弱酸规律并不陌生,可当给定反应物酸“过量”或“少量”时,学生往往对于生成的盐是“正盐”还是“酸式盐”搞不清楚. 例2 (1)向Na 2 CO 3 溶液中加入少量HF溶液,反应离子方程式为 (数据参照表1 ,下同);若加入过量HF溶液,反应离子方程式为 ; (2)向NaC...
 强酸制弱酸的原理及其应用
日期:2021-03-29 10:52:36
点击:20283
好评:0
强酸制弱酸的原理及其应用
日期:2021-03-29 10:52:36
点击:20283
好评:0
在中学化学中,我们经常听到这样的一种说法强酸制弱酸。那么强酸制弱酸到底是什么原理呢?怎么用? 我们先来看一道题,向氯化钡溶液中通入二氧化硫,会有白色沉淀产生吗?有相当多的一部分同学会认为发生如下反应:SO 2 +H 2 O+BaCl 2 =BaSO 3 ↓+2HCl 很多同学觉得这个...
 在强酸制弱酸中感受质子争夺战,体会化学思维
日期:2020-03-25 10:17:41
点击:391
好评:0
在强酸制弱酸中感受质子争夺战,体会化学思维
日期:2020-03-25 10:17:41
点击:391
好评:0
在强酸制弱酸中感受质子争夺战,体会化学思维。...
 二氧化碳通入溶液中,少量与过量是否一样?
日期:2019-05-30 20:58:34
点击:4512
好评:0
二氧化碳通入溶液中,少量与过量是否一样?
日期:2019-05-30 20:58:34
点击:4512
好评:0
一、少量、过量不一样 1、二氧化碳通入偏铝酸钠溶液 H 2 CO 3 >Al(OH) 3 >HC O 3 - 现象:都是产生白色沉淀 少量:2 NaAlO 2 +CO 2 +3 H 2 O = 2Al(OH) 3 ↓ + Na 2 CO 3 过量:NaAlO 2 +CO 2 +2 H 2 O = Al(OH) 3 ↓+ NaHCO 3 2、二氧化碳通入次氯酸钙溶液中 少量...
 利用酸轴分析化学反应规律
日期:2019-01-08 15:58:08
点击:1199
好评:0
利用酸轴分析化学反应规律
日期:2019-01-08 15:58:08
点击:1199
好评:0
铝轴:H + —Al 3+ —Al(OH) 3 —Al O 2 - —OH - 硫轴:H 2 S—S—SO 2 ——H 2 SO 4 酸轴:H + —CH 3 COOH—H 2 CO 3 —(HClO)C 6 H 5 OH— (CH 3 COO - )HC O 3 - —(ClO - )C 6 H 5 O - —C O 3 2 - —OH - 相邻没戏。比如Al O 2 - 与OH - 、SO 2 与H 2 S...
 化学小论文:弱酸真的不能制强酸吗?
日期:2017-09-18 17:29:28
点击:353
好评:0
化学小论文:弱酸真的不能制强酸吗?
日期:2017-09-18 17:29:28
点击:353
好评:0
弱酸真的不能制强酸吗?溶度积常数的应用研究。...
 强酸制弱酸信息题的应对策略
日期:2017-09-14 09:23:47
点击:1294
好评:0
强酸制弱酸信息题的应对策略
日期:2017-09-14 09:23:47
点击:1294
好评:0
...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。