
|
ѧϰСר�� |

|
ѧϰСר�� |
 [ע�������d] �Ժ�����ӵ��˶�״̬���� ����:��˫�� ��Դ:δ֪ ���ڣ�2021-12-17 09:12:18 �����19184 ����ר�⣺��������˶�״̬
[ע�������d] �Ժ�����ӵ��˶�״̬���� ����:��˫�� ��Դ:δ֪ ���ڣ�2021-12-17 09:12:18 �����19184 ����ר�⣺��������˶�״̬
������ԭ�Ӻ�����˶�״̬���൱���ӵģ��������������ĵ��Ӳ㡢�����Dz㡢�����ƵĿռ���չ���������״̬�ĸ���������������ˣ�������Ҫ˵��һ�����ӵ��˶�״̬ʱ������ͬʱָ������������һ�����Ӳ㣬��һ�������Dz㣬���ĵ���������һ�ֿռ���չ����������һ����...
 [ע�������d] �ܼ����� ����:���� ��Դ:δ֪ ���ڣ�2020-12-07 09:47:52 �����5586 ����ר�⣺�ܼ�09����
[ע�������d] �ܼ����� ����:���� ��Դ:δ֪ ���ڣ�2020-12-07 09:47:52 �����5586 ����ר�⣺�ܼ�09����
�ܼ����� ָ���Ӳ����ϴ��ijЩ��������������ڵ��Ӳ�����С��ijЩ���������������4s������3d������С��������ʱӦ�ȳ���4s���������3d���������Ԫ���ֵ��������Ų�Ϊ4s 2 3d 1 ��ʧȥ����ʱ�����ܼ�����Ӧ��ʧȥ3d���ӣ���Ϊ4s 2 3d 0 ������ԭ�ӹ���ʵ���...
 [ע�������d] �����ʾʽ ����:���� ��Դ:δ֪ ���ڣ�2016-01-30 12:24:06 �����10028 ����ר�⣺�����ʾʽ
[ע�������d] �����ʾʽ ����:���� ��Դ:δ֪ ���ڣ�2016-01-30 12:24:06 �����10028 ����ר�⣺�����ʾʽ
�����ʾʽ���÷���ͼ�ͷ������������Ų���ʽ�ӡ�ÿһ�����ʾһ�������������Ų�ʽ�Աȣ������й���ϵ�������������ڳɼ�ʱ���ӱ仯�������ص㣬�����鷳Щ����дʱ��дԪ�ط��ţ��ٸ����������ԭ��������������ԭ���ͺ��ع�����д����̼ԭ�ӻ�̬�ͼ���̬�ĵ���...
 [̽������չa] ���������� ����:�ܹ� ��Դ:δ֪ ���ڣ�2012-12-03 10:16:42 �����2165 ����ר�⣺����������
[̽������չa] ���������� ����:�ܹ� ��Դ:δ֪ ���ڣ�2012-12-03 10:16:42 �����2165 ����ר�⣺����������
ijЩ�����ܷ���������������ߣ���Щ���ʽ������������ʡ����Ƿ�����������Ц����ߡ����������������֡�...
 [̽������չa] ������Ԫ�� ����:��� ��Դ:δ֪ ���ڣ�2021-12-29 13:45:11 �����4534 ����ר�⣺������Ԫ��
[̽������չa] ������Ԫ�� ����:��� ��Դ:δ֪ ���ڣ�2021-12-29 13:45:11 �����4534 ����ר�⣺������Ԫ��
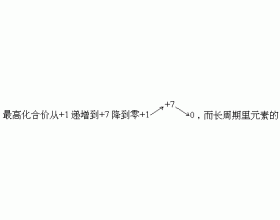
���壺 �ɺ˵������ͬ�ķ�����ͬλ����ɵ�Ԫ�ؽз�����Ԫ�ء� ˵���� �ٴ�ԭ�Ӻ��Է��ط�������ߣ��������ʽ��������ԡ��з����Ե���Ȼͬλ�ؽ���Ȼ������Ԫ�ء��������ǣ�Po����뱣�Ru�����գ�Fr�����أ�Ra����﹣�Ac�����ʣ�Th�����䣨Pa�����ˣ�U���� ���˹��ϳ�...
 [ע�������d] ��������������������ԭ�� ����:�º� ��Դ:δ֪ ���ڣ�2016-01-30 12:25:52 �����29912 ����ר�⣺����ԭ�� ����������ԭ��
[ע�������d] ��������������������ԭ�� ����:�º� ��Դ:δ֪ ���ڣ�2016-01-30 12:25:52 �����29912 ����ר�⣺����ԭ�� ����������ԭ��
һ����������ƽ���� ������20���ͽܳ�����������ѧ��֮һ�����ִ���ѧ�Ŀ�����֮һ������������ѧ�����ӵ綯��ѧ��������������ۺͻ������������������в���ĥ��Ĺ��ס��Բ������������ʽ��͵IJ�������д��������Ϊ������ѧ���������Ŀ�ѧ���С�������������һλ...
 [ע�������a] dz̸�������ӵ����� ����:���� ��Դ:δ֪ ���ڣ�2016-01-24 19:30:19 �����15239 ����ר�⣺�������� �۵���
[ע�������a] dz̸�������ӵ����� ����:���� ��Դ:δ֪ ���ڣ�2016-01-24 19:30:19 �����15239 ����ר�⣺�������� �۵���
һ���������ӿ���ȷ�����ʵĻ�ѧ������ һ��˵������������������4��ԭ��������������С��4��ԭ�ӱ˴˼�����ʧ�����γ��������ӣ����Ӽ��Ծ������������ö��γ����Ӽ�����NaCl�����������������ڻ����4��ԭ�Ӽ������õ��ӶԶ��γɹ��ۼ�����N��N��C-C����...
 [̽������չa] ����Ԫ�� ����:���ܾ� ��Դ:δ֪ ���ڣ�2021-12-29 13:43:51 �����15471 ����ר�⣺����Ԫ��
[̽������չa] ����Ԫ�� ����:���ܾ� ��Դ:δ֪ ���ڣ�2021-12-29 13:43:51 �����15471 ����ר�⣺����Ԫ��
����Ԫ��֮һ Ԫ�����ڱ�����ʽ���дӢ�B�嵽��B��10�����У�������ϵ���ϵԪ��ϰ���ϰ����ǽ�������Ԫ�أ���ЩԪ�������ڱ����λ���ǽ��ڵ��ͽ����͵��ͷǽ���֮��ģ���ʾ�ɽ�������ǽ����Թ��ɵ���˼�� ����Ԫ��֮�� ����Ԫ�صĺ������˵����һ���ɷ����������...
 [ע�������d] 3d�����4s������ĸ���������� ����:������ ��Դ:δ֪ ���ڣ�2012-11-29 12:57:41 �����15083 ����ר�⣺�ܼ�09
[ע�������d] 3d�����4s������ĸ���������� ����:������ ��Դ:δ֪ ���ڣ�2012-11-29 12:57:41 �����15083 ����ר�⣺�ܼ�09
��3d���û�е������ʱ,3d�������������4s�������(����Naԭ�Ӻ� Caԭ��);��3d�����������ϵ���ʱ,4s�������������3d���������(����Tiԭ�Ӻ�Vԭ��)����Ϊ3d���������е���ʱ,�������� 4s���Ӳ�����������,ʹ4s��������������ߵĽ��....
 [̽������չa] ��ѧ�ϵĶԽ��߹��� ����:��� ��Դ:δ֪ ���ڣ�2013-04-15 10:43:31 �����27199 ����ר�⣺�Խ��߹���
[̽������չa] ��ѧ�ϵĶԽ��߹��� ����:��� ��Դ:δ֪ ���ڣ�2013-04-15 10:43:31 �����27199 ����ר�⣺�Խ��߹���
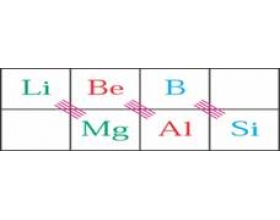
1.�Խ��߹��� �Ա�����ϵ��Ԫ������,����: ���ϡ�����,�Խ���Ԫ���������Ʃ����Խ��߹��� ����ϵ����������Ԫ�ضԽǹ�ϵ���ԡ� �Խ��߹�����Ҫ�Ǵ������ܽ�����ľ������,�ɴ����Ӽ���������Խ��͡� 2.�Խ�Ԫ�����ʵ������� ����B��Si��һ��Ԫ��Ϊ���о�����: ���� B ...
 ��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ�
��ӭ������վ��̬���ֻ�ɨһɨ�Ϳ��ԡ� ��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء�
��ӭʹ�û�ѧ��ϰ��APP��ɨ��Ϳ����ء������ԭ���У��ڿ���ij������ʱ�������������Ӷ����ų����ÿ���������ԭ�Ӻ˶�����...
1.������ӹ��м����ܲ�? �ܲ���Ӳ�,������ԭ�Ӻ�Զ���IJ�ͬ,��������ɷ�Ϊ��һ����...
1��һ�����ӵ��˶�״̬Ҫ���ļ������������� ��Ӧ����������������ܲ�(���Ӳ�)�ǵ�...
...
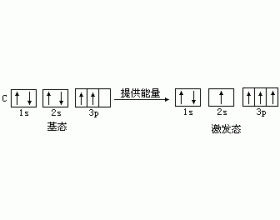
��̬�ͼ���̬ ʲô�ǹ��ף� ���ף���ͬԪ�ص�ԭ�ӷ���ԾǨʱ�� ���� �� ��̬������̬ ...
���ֵ��ܼ�ͼֻ�Ǹ����Ƶ��ܼ�ͼ���ǰ�������������ӵ������̡� ������������...
��������Ų��Ƿdz�����˼�ġ��ڿ�ʼ��ʱ������ֵ���֮��֪��������ԭ��������...
�����Ʋ����ƣ��Ǹ��ʷֲ�ͼ �������ǵ�����ԭ�Ӻ���ռ���ֵĸ����ܶȷֲ�ͼ������...