
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑d] 基态与激发态,构造原理与电子排布式解读 作者:化学自习室 来源:未知 日期:2023-10-07 09:16:16 点击:2048 所属专题:构造原理
[注解与辨疑d] 基态与激发态,构造原理与电子排布式解读 作者:化学自习室 来源:未知 日期:2023-10-07 09:16:16 点击:2048 所属专题:构造原理
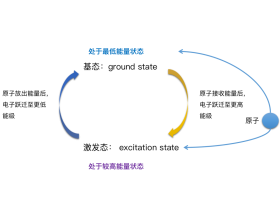
基态和激发态 什么是光谱? 光谱:不同元素的原子发生跃迁时会 吸收 ( 基态→激发态 )或 释放 ( 激发态→基态 )不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱或发射光谱, 总称原子光谱 。 光谱分析:在现代化学中,常利用原子光谱上的 特征谱 线来 鉴定元素...
 [注解与辨疑d] 泡利原理与洪特规则解读 作者:化学自习室 来源:未知 日期:2023-10-07 09:11:46 点击:1887 所属专题:泡利原理 洪特规则
[注解与辨疑d] 泡利原理与洪特规则解读 作者:化学自习室 来源:未知 日期:2023-10-07 09:11:46 点击:1887 所属专题:泡利原理 洪特规则
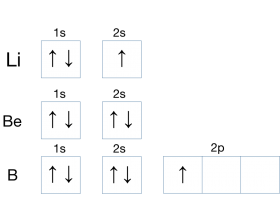
能量最低原则: 在构建 基态原子 时,电子将 尽可能地占领 能量最低的原子轨道 ,使整个原子的 能量最低 。 泡利不相容原理( Pauli exclusion principle) 又称泡利原理,不相容原理,是 微观粒子 运动的基本规律之一。 内容是:在一个原子轨道里,不能有两个或两个以上...
 [注解与辨疑d] 关于核外电子排布通俗解读 作者:化学自习室 来源:未知 日期:2023-04-26 07:55:43 点击:732 所属专题:核外电子排布
[注解与辨疑d] 关于核外电子排布通俗解读 作者:化学自习室 来源:未知 日期:2023-04-26 07:55:43 点击:732 所属专题:核外电子排布
核外电子排布是非常有意思的。在开始的时候,人类发现电子之后不知道电子在原子里面怎么样存在。于是人们提出了各种各样的模型来解释。比较出名的就是J. J. 汤姆逊(电子的发现者)提出的葡萄干面包模型:电子像是葡萄干嵌在面包里一样嵌在原子里。但是这个模型被一个著...
 [注解与辨疑d] 概念辨析:泡利不相容原理及洪特规则 作者:化学自习室 来源:未知 日期:2023-01-02 15:56:43 点击:22193 所属专题:洪特规则
[注解与辨疑d] 概念辨析:泡利不相容原理及洪特规则 作者:化学自习室 来源:未知 日期:2023-01-02 15:56:43 点击:22193 所属专题:洪特规则
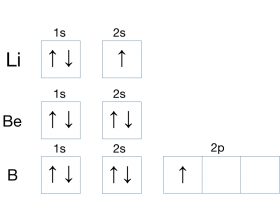
能量最低原则: 在构建 基态原子 时,电子将 尽可能地占领 能量最低的原子轨道 ,使整个原子的 能量最低 。 泡利不相容原理( Pauli exclusion principle) 又称泡利原理,不相容原理,是 微观粒子 运动的基本规律之一。 内容是:在一个原子轨道里,不能有两个或两个以上...
 [注解与辨疑d] 概念辨析:能层和能级 作者:化学自习室 来源:未知 日期:2023-01-02 15:50:56 点击:6029 所属专题:能层 能级
[注解与辨疑d] 概念辨析:能层和能级 作者:化学自习室 来源:未知 日期:2023-01-02 15:50:56 点击:6029 所属专题:能层 能级
能层 :按照电子能量的差异,将核外电子分成不同的能层。距离原子核的远近是结果,能量不同才是导致排布远近不同的动力因。 1层 2层 3层 4层 5层 6层 7层 K层 L层 M层 N层 O层 P层 Q层 能级 :同一能层中,能量不同的电子,分成不同的能级。同一能层的电子,能量可以不同,...
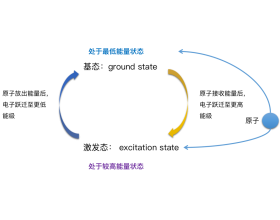 [注解与辨疑d] 概念辨析:基态与激发态及构造原理与电子排布式 作者:化学自习室 来源:未知 日期:2023-01-02 15:47:00 点击:3155 所属专题:构造原理 电子排布式
[注解与辨疑d] 概念辨析:基态与激发态及构造原理与电子排布式 作者:化学自习室 来源:未知 日期:2023-01-02 15:47:00 点击:3155 所属专题:构造原理 电子排布式
基态和激发态 什么是光谱? 光谱:不同元素的原子发生跃迁时会吸收(基态→激发态)或释放(激发态→基态)不同的光,可以用光谱仪摄取各种元素的电子的吸收光谱或发射光谱,总称原子光谱。 光谱分析:在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分...
 [注解与辨疑d] 概念辨析:电子云及原子轨道 作者:化学自习室 来源:未知 日期:2023-03-21 16:48:13 点击:20980 所属专题:电子云 原子轨道
[注解与辨疑d] 概念辨析:电子云及原子轨道 作者:化学自习室 来源:未知 日期:2023-03-21 16:48:13 点击:20980 所属专题:电子云 原子轨道
电子云不是云,是概率分布图 电子云是电子在原子核外空间出现的概率密度分布图。它不是实际的电子,可以理解为电子可能出现的概率轨迹。 电子云轮廓图 电子在原子核外空间出现概率为90% 的空间圈出来,即电子云轮廓图。实际是指,电子大概率会出现的空间区域。我们只能...
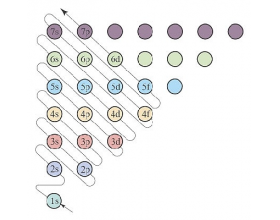 [注解与辨疑d] 构造原理图及元素周期表分区 作者:化学自习室 来源:未知 日期:2022-10-11 19:27:27 点击:11171 所属专题:构造原理 元素分区
[注解与辨疑d] 构造原理图及元素周期表分区 作者:化学自习室 来源:未知 日期:2022-10-11 19:27:27 点击:11171 所属专题:构造原理 元素分区
1869 年俄国化学家门捷列夫发现了元素周期律; 1913 年丹麦科学家玻尔基于氢光谱线状光谱实验,提出氢原子模型、玻尔理论,成功解释了氢原子光谱的线状光谱现象;在此基础上, 1920 年玻尔提出构造原理,即从氢元素开始,随元素原子序数增加,其核电荷数递增,新增电子...
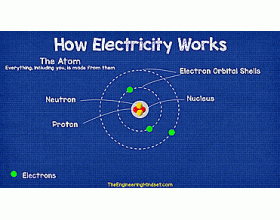 [注解与辨疑d] 全文解读原子结构 作者:化学自习室 来源:未知 日期:2022-09-16 15:11:40 点击:3676 所属专题:原子结构03
[注解与辨疑d] 全文解读原子结构 作者:化学自习室 来源:未知 日期:2022-09-16 15:11:40 点击:3676 所属专题:原子结构03
原子是构成物质的基本单元,原子结构影响原子间的结合方式,而原子间结合的方式决定了材料的种类,不同材料有着不同的性能,同一材料经过不同的加工工艺后也会有不同的性能,这些都归结于内部结构的不同,本文重讲一下原子结构(Atomic Structure)的相关知识。 01 原子...
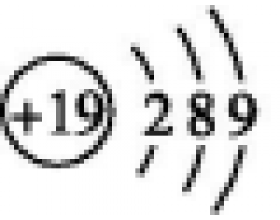 [注解与辨疑d] 原子结构与性质疑难剖析 作者:化学自习室 来源:未知 日期:2022-08-06 09:56:10 点击:19462 所属专题:原子结构03与性质
[注解与辨疑d] 原子结构与性质疑难剖析 作者:化学自习室 来源:未知 日期:2022-08-06 09:56:10 点击:19462 所属专题:原子结构03与性质
2022 年普通高等学校招生全国统一考试 ( 全国乙卷 ) 化学 【2022全国乙卷】1. 生活中处处有化学,下列叙述正确的是 A. HB 铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂 C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧 【答案】 B 【解析】 【详解...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
原子核外电子的真实运动状态是我们肉眼看不到的,但是可以通...
铜原子(Cu)的基态电子排布为[Ar] 3d4s,失去一个电子形成亚铜...
先让大家看看高中和大学电负性的数值图:下面的人教版高中化...
在元素周期表中,除了同周期从左到右、同主族从上到下的性质...
电负性是描述原子在化合物中吸引成键电子能力的核心物理量,...
【导读】第一电离能(I)和第一电子亲和能(E)从能量变化的角度描...
电离能和电子亲和能都是研究元素游离态的原子的性质。电离能...