
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑j] 弱酸酸性强弱顺序及应用举例 作者:王利平 来源:未知 日期:2016-02-02 10:12:01 点击:1933 所属专题:酸性 盐类水解应用
[注解与辨疑j] 弱酸酸性强弱顺序及应用举例 作者:王利平 来源:未知 日期:2016-02-02 10:12:01 点击:1933 所属专题:酸性 盐类水解应用
...
 [注解与辨疑j] 溶度积、溶解度、浓度概念辨析及其关系 作者:黄勇 来源:未知 日期:2019-06-28 10:18:42 点击:12348 所属专题:溶度积与溶解度 物质的量浓度
[注解与辨疑j] 溶度积、溶解度、浓度概念辨析及其关系 作者:黄勇 来源:未知 日期:2019-06-28 10:18:42 点击:12348 所属专题:溶度积与溶解度 物质的量浓度
一.溶度积: 【注】溶度积 K sp 实际上就是沉淀的“解离常数”;溶度积 K sp 与生成沉淀的常数K(生成沉淀)互为倒数。 二.溶解度的几种表示: 1.固体溶解度: 固体溶解度是指在一定的温度下,某固体物质在100克溶剂里(通常为水)达到饱和状态时所能溶解的质量(在一定温度...
 [注解与辨疑j] 水解平衡常数的计算 作者:王金玉 来源: 日期:2019-11-24 16:15:21 点击:134124 所属专题:水解平衡常数 盐类水解
[注解与辨疑j] 水解平衡常数的计算 作者:王金玉 来源: 日期:2019-11-24 16:15:21 点击:134124 所属专题:水解平衡常数 盐类水解
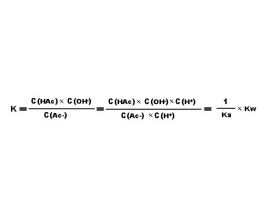
一.醋酸钠溶液的水解(强碱弱酸盐水解) Ac - +H 2 O HAc+OH - 平衡常数 : (Kw 是水的离子积, Ka 是醋酸的电离常数 ) 二.氯化铵溶液的水解(强酸弱碱盐水解) NH4++H2ONH3.H2O+H+ 平衡常数 : (Kw 是水的离子积, Kb 是氨水的电离常数 ) 三.醋酸铵溶液的水解(弱酸弱...
 [注解与辨疑j] 沉淀转化疑难解答 作者:黄叶 来源:未知 日期:2019-06-11 16:32:23 点击:1416 所属专题:沉淀转化 溶度积
[注解与辨疑j] 沉淀转化疑难解答 作者:黄叶 来源:未知 日期:2019-06-11 16:32:23 点击:1416 所属专题:沉淀转化 溶度积
...
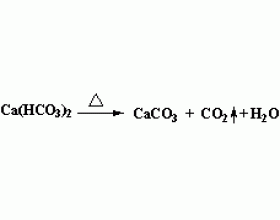 [注解与辨疑j] 蒸干盐溶液所得物质的判断方法 作者:李萍 来源:未知 日期:2015-04-23 09:18:48 点击:2434 所属专题:盐类水解应用 蒸干
[注解与辨疑j] 蒸干盐溶液所得物质的判断方法 作者:李萍 来源:未知 日期:2015-04-23 09:18:48 点击:2434 所属专题:盐类水解应用 蒸干
蒸发盐溶液时最终能否得到溶质,与溶质的稳定性、水解性、还原性有关: 1.判断盐的稳定性。判断该盐是否稳定。有些盐不稳定,加热蒸干后会发生分解,检查盐加热后是否会分解如: Ca(HCO 3 ) 2 由于不稳定加热蒸干后,分解为 CO 2 和水蒸气( H 2 O ) 挥发后剩下的物质是 CaCO...
 [注解与辨疑j] 醋酸和醋酸钠混合溶液中,醋酸电离大于醋酸钠水解吗? 作者:李留记 来源:未知 日期:2015-03-15 11:21:43 点击:2691 所属专题:盐类水解应用 酸碱性判断
[注解与辨疑j] 醋酸和醋酸钠混合溶液中,醋酸电离大于醋酸钠水解吗? 作者:李留记 来源:未知 日期:2015-03-15 11:21:43 点击:2691 所属专题:盐类水解应用 酸碱性判断
请问各位同仁,醋酸和醋酸钠同时存在,醋酸电离大于醋酸钠水解吗?为什么?不一定。要看他们的浓度。根据Ka Kw Kc 可计算其浓度比和PH 的关系。 醋酸和醋酸钠浓度之比为1:176时,为中性;大于1:176时,酸的电离为主;小于1:176时,以水解为主。...
 [注解与辨疑j] 为什么碱溶液混合求pH必须要先求C(OH-)? 作者:张县 来源:未知 日期:2015-02-12 19:37:14 点击:2194 所属专题:ph计算
[注解与辨疑j] 为什么碱溶液混合求pH必须要先求C(OH-)? 作者:张县 来源:未知 日期:2015-02-12 19:37:14 点击:2194 所属专题:ph计算
我们知道任何水溶液中H + 、OH - 都是共存的,而 c (H + ) c (OH - )= K w , 在常温 时 K w =1×10 -14 , 在酸溶液 c (H + )> c ( OH - ),例如:在pH=5的盐酸溶液 c (H + )=10 -5 mol/L, c ( OH - )=10 -9 mol/L,显然前者浓度的远远大于后者的浓度。...
 [注解与辨疑j] 同浓度同体积的NaCl和NaF溶液的离子数多少的比较。 作者:张楠 来源:未知 日期:2015-02-03 10:26:12 点击:1031 所属专题:盐类水解应用
[注解与辨疑j] 同浓度同体积的NaCl和NaF溶液的离子数多少的比较。 作者:张楠 来源:未知 日期:2015-02-03 10:26:12 点击:1031 所属专题:盐类水解应用
1.同浓度同体积的NaCl和NaF溶液的离子数多少的比较。 2.同浓度同体积的NaOH和NaF溶液的离子数多少的比较。 3.同浓度同体积的HCl和NH 4 Cl溶液的离子数多少的比较。 4.同浓度同体积的NaCl和NH 4 Cl溶液的离子数多少的比较。 1.根据电荷守恒 C(Na + )+ c (H + )= c (Cl - )...
 [注解与辨疑j] 酸式盐的水解与电离比较 作者:耿艳 来源:未知 日期:2015-02-01 15:28:41 点击:6529 所属专题:酸式盐 酸碱性判断
[注解与辨疑j] 酸式盐的水解与电离比较 作者:耿艳 来源:未知 日期:2015-02-01 15:28:41 点击:6529 所属专题:酸式盐 酸碱性判断
盐类的水解中,什么时候水解大于电离,什么时候电离大于水解?高中都需要掌握那些盐? 1. 常见的电离大于水解的酸式盐有:亚硫酸氢盐,磷酸二氢盐,草酸氢盐等大多数酸式盐(溶液呈酸性)。 2.常见的水解大于电离的酸式盐有:磷酸一氢盐,碳酸氢盐,硫氢化物等少数酸式盐(...
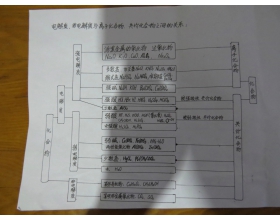 [注解与辨疑3] 离子化合物、共价化合物与电解质、非电解质之间的关系总结 作者:陈万 来源:未知 日期:2016-01-17 16:32:51 点击:6749 所属专题:离子化合物 共价化合物 电解质判断 非电解质
[注解与辨疑3] 离子化合物、共价化合物与电解质、非电解质之间的关系总结 作者:陈万 来源:未知 日期:2016-01-17 16:32:51 点击:6749 所属专题:离子化合物 共价化合物 电解质判断 非电解质
【补充】(1)少数气态氢化物也是非电解质。如氨气。(2)活泼金属氢化物才是电解质。如氢化钠。 大致规律: 离子化合物包括铵盐、强碱、活泼金属化合物,其他的不活泼的金属化合物和只由非金属组成的化合物都是共价化合物。 除了离子化合物都是共价化合物。 通常认为: 电负...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。问:为什么强酸在冰醋酸中可以比较出其酸性强弱? 想要回答这个问题,还是得回到酸电...
计算0.01mol ZnS溶于1.0L 盐酸中,所需盐酸的最低浓度? 查表可知: K sp (Zns)=2.0×...
水的离子积常数 K w 是一个温度的函数,言外之意就是只和温度有关,只要温度不变,溶...
氢氟酸在溶于水的时候,先解离成氢离子和氟离子,这个过程需要吸收热量。 氢离子和氟...
...
HI 10 11 HBr 10 9 HCl 10 7 HClO 4 10 7 HClO 3 10 3 H 2 SO 4 10 2 HNO 3 20 H 3 O ...
一、 强、弱电解质概念上的四大区别 强电解质在水溶液中全部电离,电离不可逆,不存在...
几种酸碱指示剂变色的pH范围:①甲基橙3.1~4.4、②甲基红4.4~6.2③酚酞8.2~10,现用0....