
|
学习小专题 |

|
学习小专题 |
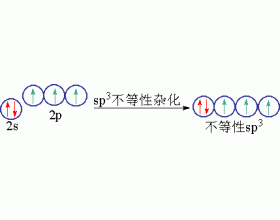 [注解与辨疑e] 不等性杂化轨道 作者:张扬 来源:未知 日期:2021-05-13 16:13:46 点击:7946 所属专题:杂化轨道类型
[注解与辨疑e] 不等性杂化轨道 作者:张扬 来源:未知 日期:2021-05-13 16:13:46 点击:7946 所属专题:杂化轨道类型
有些分子的成键,表面来看与CH 4 分子的成键差别很大。比如NH 3 分子的成键似乎与BF 3 分子类似,中心原子也将采取sp 2 杂化的方式成键,键角也应为120,但实测结果键角却为10718,与10928更为接近些。又譬如H 2 O分子的成键似乎与BeCl 2 分子类似,中心原子也将采取sp...
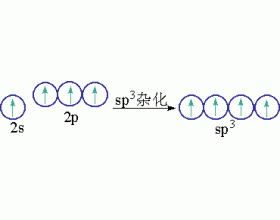 [注解与辨疑e] sp3杂化轨道 作者:刘洪林 来源:未知 日期:2013-04-13 18:51:50 点击:8382 所属专题:杂化轨道类型
[注解与辨疑e] sp3杂化轨道 作者:刘洪林 来源:未知 日期:2013-04-13 18:51:50 点击:8382 所属专题:杂化轨道类型
同一原子内由一个ns轨道和三个np轨道发生的杂化,称为sp 3 杂化,杂化后组成的轨道称为sp 3 杂化轨道。sp 3 杂化可以而且只能得到四个sp 3 杂化轨道。 CH 4 分子的结构经实验测知为正四面体结构,四个C-H键均等同,键角为10928,杂化轨道理论认为,激发态C原子(2s 1 2...
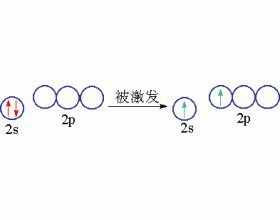 [注解与辨疑e] sp杂化轨道 作者:程波 来源:未知 日期:2013-04-13 18:06:20 点击:10689 所属专题:杂化轨道类型
[注解与辨疑e] sp杂化轨道 作者:程波 来源:未知 日期:2013-04-13 18:06:20 点击:10689 所属专题:杂化轨道类型
同一原子内由一个ns轨道和一个np轨道发生的杂化,称为sp杂化。杂化后组成的轨道称为sp杂化轨道。sp杂化可以而且只能得到两个sp杂化轨道。 实验测知,气态BeCl 2 是一个直线型的共价分子。Be原子位于两个Cl原子的中间,键角180,两个Be-Cl键的键长和键能都相等: Cl-Be-Cl...
 [注解与辨疑e] sp2杂化轨道 作者:罗翊轩 来源:未知 日期:2013-04-13 18:00:10 点击:12502 所属专题:杂化轨道类型
[注解与辨疑e] sp2杂化轨道 作者:罗翊轩 来源:未知 日期:2013-04-13 18:00:10 点击:12502 所属专题:杂化轨道类型
同一原子内由一个ns轨道和二个np轨道发生的杂化,称为sp 2 杂化。杂化后组成的轨道称为sp 2 杂化轨道。实验测知,气态氟化硼(BF 3 )具有平面三角形的结构。B原子位于三角形的中心,三个B-F键是等同的,键角为120。 基态B原子的价层电子构型为2s 2 2p 1 ,表面看来似乎只...
 [注解与辨疑e] 配位键和配位数 作者:黄勇 来源:未知 日期:2022-04-06 17:34:54 点击:28429 所属专题:配位键 配合物配位数
[注解与辨疑e] 配位键和配位数 作者:黄勇 来源:未知 日期:2022-04-06 17:34:54 点击:28429 所属专题:配位键 配合物配位数
配位键 定义:成键电子由成键原子一方单独提供形成的共价键,叫做配位键(曾用名:配价键)。 说明 1.配位键是特殊的共价键。常用L→M符号表示。其中L提供孤对电子,叫做电子对给予体。M原子有空轨道,可以接受孤对电子,叫做电子对接受体。 2.一方有孤对电子,而另一方...
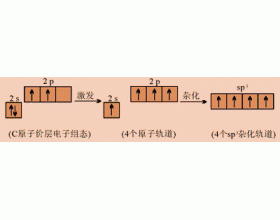 [注解与辨疑e] CCl4分子的空间构型 作者:丁萍 来源:未知 日期:2022-03-18 17:00:16 点击:23352 所属专题:四氯化碳 分子结构模型
[注解与辨疑e] CCl4分子的空间构型 作者:丁萍 来源:未知 日期:2022-03-18 17:00:16 点击:23352 所属专题:四氯化碳 分子结构模型
实验测定表明,CCl 4 分子的空间构型为正四面体。其形成过程可表示为示为 CCl 4 分子的空间构型和sp 3 杂化轨道 中心原子C以夹角均为109°28′的4个完全等同的sp 3 杂化轨道分别与4个H原子的1s轨道重叠后,形成4个sp 3 s的σ键。故CCl 4 分子的空间构型为正四面体。...
 [注解与辨疑e] 杂化轨道类型与分子空间构型的关系 作者:董啸 来源:未知 日期:2013-04-03 10:13:44 点击:38776 所属专题:杂化类型判断 分子立体结构判断
[注解与辨疑e] 杂化轨道类型与分子空间构型的关系 作者:董啸 来源:未知 日期:2013-04-03 10:13:44 点击:38776 所属专题:杂化类型判断 分子立体结构判断
一、sp 3 杂化――分子的空间构型为(正)四面体 以CH 4 为例 C原子外层电子构型(基态)C原子(激发态)C原子(杂化态) sp 3 杂化轨道的特点:sp 3 轨道夹角为109度28分,以正四面体结构排列,4个sp 3 轨道等同。 不等性sp 3 杂化――分子的空间构型为三角锥形或V型 以NH...
 [注解与辨疑e] 关于氢键的问题集 作者:胡中宇 来源:未知 日期:2013-03-27 16:14:11 点击:8205 所属专题:氢键02
[注解与辨疑e] 关于氢键的问题集 作者:胡中宇 来源:未知 日期:2013-03-27 16:14:11 点击:8205 所属专题:氢键02
问题1:究竟氢键是属于分子间作用力呢?还是化学键呢? 答:氢键的作用力强度与分子间力的强度是同一个数量级,比共价键的强度小得多。一些物质在熔化、气化的物理变化过程中,氢键受到破坏。因此,氢键应归入分子间作用力来讨论。 但是,氢键的成键方式与分子间力差别很大...
 [注解与辨疑e] 含氧酸的元数 作者:赵双燕 来源:未知 日期:2012-11-25 19:03:00 点击:11197 所属专题:含氧酸
[注解与辨疑e] 含氧酸的元数 作者:赵双燕 来源:未知 日期:2012-11-25 19:03:00 点击:11197 所属专题:含氧酸
在初中,我们学习酸时,通常会对酸进行分类,有一种分类方法,是按照酸是否含有氧分:含氧酸,如亚硫酸H 2 SO 3 、偏磷酸HPO 3 、甲酸HCOOH等;无氧酸,如氢硫酸H 2 S、氢溴酸HBr等。我们在此只讨论含氧酸的元数。 还有一种分类方法,是按照酸的元数分:一元酸、二元酸、及...
 [注解与辨疑e] 价层电子对互斥理论预测分子空间构型步骤 作者:刘丽颖 来源:未知 日期:2020-01-02 08:39:11 点击:16062 所属专题:价层电子对互斥理论 分子立体结构判断
[注解与辨疑e] 价层电子对互斥理论预测分子空间构型步骤 作者:刘丽颖 来源:未知 日期:2020-01-02 08:39:11 点击:16062 所属专题:价层电子对互斥理论 分子立体结构判断
价键理论可解释原子采用什么样的空间轨道去形成共价键,但不易预测分子的空间结构。价层电子对互斥理论可相当成功地简便地判断许多共价型分子的几何构型。 该理论认为,在多原子共价型分子中,中心原子周围的配体(原子、离子或原子团)的相对几何位置,决定于中心原子的...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。[2025湖北新八校2月卷] 8 . 从微观视角探析物质结构及性质是学习化学的有效方法。下列...
含氮(N)的杂化化合物是指氮原子通过轨道杂化形成化学键的化合物。氮原子的电子构型...
在化学中均裂和异裂是共价键的断裂的两种主要方式,其决定因素不同:均裂主要由键能决...
通常而言,同主族元素形成的X-X键,自上而下,键长逐渐增大,键能逐渐降低。 根据元素...
无机化学实验是一门与无机化学理论课密切配合的课程。实验用化学事实充实了理论课的学...
能否形成氢键的“视点”:一看有无电负性...
1mol 氨中氢键数量分析 一、氢键形成机制 NH分子结构 H原子作为氢键供体(需与高电负性...
二氧化氮(NO)中氮原子的杂化类型为 sp杂化,具体分析如下: 1.计算 n (的价层电子对数...