
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
同一原子内由一个ns轨道和一个np轨道发生的杂化,称为sp杂化。杂化后组成的轨道称为sp杂化轨道。sp杂化可以而且只能得到两个sp杂化轨道。
实验测知,气态BeCl2是一个直线型的共价分子。Be原子位于两个Cl原子的中间,键角180°,两个Be-Cl键的键长和键能都相等:
Cl-Be-Cl
基态Be原子的价层电子构型为2s2,表面看来似乎是不能形成共价键的。但杂化理论认为,成键时Be原子中的一个2s电子可以被激发到2p空轨道上去,使基态Be原子转变为激发态Be原子(2s12p1):

与此同时,Be原子的2s轨道和一个刚跃进的电子的2p轨道发生sp杂化,形成两个能量等同的sp杂化轨道:
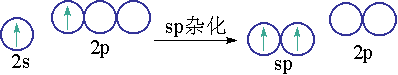
其中每一个sp杂化轨道都含有![]() 轨道和
轨道和![]() 轨道的成分。每个sp轨道的形状都是一头大,一头小。成键时,都是以杂化轨道大的一头与Cl原子的成键轨道重叠而形成两个σ键。根据理论推算,这两个sp杂化轨道正好互成180°,亦即在同一直线上。
轨道的成分。每个sp轨道的形状都是一头大,一头小。成键时,都是以杂化轨道大的一头与Cl原子的成键轨道重叠而形成两个σ键。根据理论推算,这两个sp杂化轨道正好互成180°,亦即在同一直线上。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
今天整理完整版氢键核心笔记,概念、形成、分类、性质影响一...
提到化学,我们最先想到的往往是化学键断裂与重组的化学反应...
一、概念与本质类易错点 •易错1:混淆氢键与化学键——氢键...
高中化学物质结构板块里,配位键和配位化合物一直是高频考点...
...
...