
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
氯化氢等气体在喷泉实验中形成的美丽喷泉让人难以忘怀,那么喷泉形成的原理是什么呢?如何诱发喷泉的形成呢?用于作喷泉实验的气体的性质又有什么特点呢?
一、喷泉实验形成的物理原因
众所周知:公园、广场上的喷泉产生的原因是水承受的压强大于大气压。氯化氢气体、氨气在适当的装置中所产生的喷泉也是因为提供液体的地方与液体喷出的地方存在着较大的压强差(如下图中a、b两处),并且在实验中,压强差能迅速达到某一数值以上(这是形成喷泉的关键所在)。压强差的形成可以是因烧瓶内的压强减小形成的,也可以是由烧瓶外压强增大(体系是密闭的)形成的。
例1:如图,烧瓶中充满了某种气体X,气体体积为500mL(标准状况),烧杯中盛的是水,导管长h=50cm,其中有12cm在水面以下,实验开始时,胶头滴管能向烧瓶中挤压出0.5mL 水,
(1)试通过计算判断能否产生喷泉现象(假设实验操作无错误,在标准状况下,1体积的水最多能溶解40体积的X压强的微小变化对气体溶解度的影响忽略不计)。
(2)在上述条件下,X的溶解度(s)应大于多少时才能形成喷泉?
|
解析:由物理学原理可知,水要想从a处喷出形成喷泉,当胶头滴管挤压出的0.5mL 水溶解了一部分X气体后,烧瓶中剩余气体的压强与导管中水柱产生的压强之和应小于大气压。
(1)由于0.5mL 水能溶解20mL 的气体X,由阿佛加德罗推论知:溶解20mLX后烧瓶内压强为:101325Pa×(500—20)÷500 = 97272Pa,导管水柱产生的水压约为:ρgh = 1×9.8×(50×10 — 12×10) = 3724(Pa),二者之和为97272+3724 = 100999(Pa) < 101325Pa ,故可以形成喷泉。(2)同理应有101325×(500—S) ÷500 +3724 < 101325,S > 19,即1体积水中溶解的X体积要大于19体积就可形成喷泉。
二、产生压强差的途径
使a、b两处产生压强差的基本途径有两种:通过使烧瓶中气体数量减少(溶解或排出一部分)或降温使瓶中压强降低;通过升温使提供液体外的压强增大(当体系处于封闭状态时)。其中用于实验的气体就应易溶于所用的液体(不一定是水,如CO2气体与NaOH溶液也可作喷泉实验)。
例2:分别用右图1、2、3、三种装置进行喷泉实验:
|
1.引发图(1)水上喷的方法是_______,其原理是_______。
2.引发图(2)水上喷的方法是_______,原理是________。
3.使图(3)能形成喷泉的方法有________。原理是______。
解析:图1、图2处于非密闭体系,故应设法使烧瓶内气体压强减少。故1.打开止水夹,挤出胶头滴管中的水即可。因为水溶解了极易溶于水的HCl,使烧瓶内气体压强迅速减小。2打开止水夹,
三、产生喷泉现象的技术要求
为使喷泉最终能形成,实验中所用气体应易溶于水可易溶于用作喷泉实验的液体之中。盛放气体的仪器内干燥且充满气体,此外整个装置气密性应良好,导管的长度要适当,所用导管的出口应该比较小。
四、喷泉颜色的多样性
喷泉实验中喷泉的颜色取决于液体、气体的性质及所用指示剂的种类:当液体是水,指示剂为石蕊试液时,用HCl作实验时,看到的是红色喷泉(酸使石蕊变红色);用NH3作实验时,喷泉为蓝色(碱使石蕊变蓝色);若用FeCl3溶液作喷泉实验,则可看到棕黄色的喷泉。
五、喷泉结束时所形成的溶液的浓度
如果实验是在标准状况下进行(或视为在标准状况下进行)的,则喷泉所形成的溶液物质的量浓度可通过计算求出,过程如下:设溶解的气体体积为V(升),则喷泉形成的溶液的体积也是V(升),标准状况下V(升气体为)V/22.4(mol),所以溶液的物质的量浓度为V/22.4/V = 1/22.4 ≈ 0.045 (mol/L)。这表明:喷泉实验所得到的溶液物质的量浓度是个常数,它与实验结束时,液体是否充满烧瓶无关。但用于喷泉实验的气体在实验时若发生化学反应,则应结合具体反应的方程式进行计算。
例3:若用体积比为1∶4的NO2、O2(已知4NO2+O2+2H2O = 4HNO3)混合气体作喷泉实验,则实验结束(标准状况)时所得溶液的物质的量浓度为___。
解析:由反应方程式4NO2+O2+2H2O = 4HNO3知:溶解5mol 的混合气体会生成4mol 硝酸(溶质),得到5×22.4L 的溶液,所以溶液物质的量浓度为:设混合气体体积为VL即V/22.4 mol,生成的硝酸为![]() ×
×![]() mol,所得溶液的体积为VL,故硝酸的浓度为
mol,所得溶液的体积为VL,故硝酸的浓度为![]() ×
×![]() ÷V=1/28(mol/L) 。
÷V=1/28(mol/L) 。
需要说明的是:若是用试管收集满气体然后将其倒置于水中进行溶解,若不考虑溶质的扩散,则试管中所得溶液的物质的量浓度与喷泉实验形成的溶液浓度一样。
六、创新思维:喷泉实验的姊妹 一 “喷烟”实验
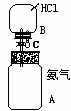
受喷泉实验原理的启发,可用如右图所示装置作“喷烟”的实验。实验的方法是:先将A瓶收集满NH3气体,将B瓶收集满HCl并连接好,然后从胶头滴管中挤出几滴水,使少量水进入B中溶解HCl,从而使B中的压强减少,然后打开弹簧夹,A瓶中的NH3气体就会喷到B瓶中与NH3发生反应生成NH4Cl固体小微粒而产生浓烟滚滚的现象。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、认识双氧水:从分子结构说起 化学名称:过氧化氢(Hydro...
一、总方法:接触法 整个工业制硫酸分为三个阶段、三个设备、...
1.硫代硫酸钠(Na 2 S 2 O 3 ): Na 2 S 2 O 3 ·5H 2 O俗名海波或大苏打,...
...
磷作为周期表第 ⅤA 族核心元素,兼具 “生命不可替代性”(构...
硫酸盐 俗名 颜色 用途 2CaSO 4 H 2 O 熟石膏 白色 CaSO 4 2H 2 O 生石膏...