
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
分子缔合作用,是由于分子间氢键的形成,钳环化则是由于分子内氢键的形成。两者对于化合物的性质的影响是显著的,并且往往是相反的,现简述如下。
(1)对沸点和熔点的影响
分子间氢键的形成使物质的沸点和熔点升高,因为要使液体气化,必须破坏大部分分子间的氢键,这需要较多的能量;要使晶体熔化,也要破坏一部分分子间的氢键。所以,形成分子间氢键的化合物的沸点和熔点都比没有氢键的同类化合物为高。
分子内氢键的生成使物质的沸点和熔点降低,如邻位硝基苯酚的熔点为45 ℃,而间位和对位硝基苯酚的熔点分别是96 ℃和114 ℃。这是由于间位和对位硝基苯酚中存在着分子间氢键,熔化时必须破坏其中的一部分氢键,所以它们熔点较高;但邻位硝基苯酚中已经构成内氢键,不能再构成分子间氢键了,所以熔点较低。
(2)对溶解度的影响
在极性溶剂里,如果溶质分子与溶剂分子间可以生成氢键,则溶质的溶解度增大。如果溶质分子钳环化,则在极性溶剂里的溶解度减小。例如,对硝基苯酚中O—H基,能同水的氧原子缔合成氢键,促使它在水中溶解,因此溶解度大,在水蒸气里不挥发。但邻硝基苯酚的O—H基,通过氢原子能与其邻位上硝基的氧原子钳环化,即不能再同水的氢原子形成氢键,因此溶解度减小,而且易被水蒸气蒸馏出去。邻位与对位硝基苯酚在20 ℃的水里的溶解度之比为0.39。钳环化的化合物在非极性溶剂里,其溶解度与上述情况相反。
(3)对酸性的影响
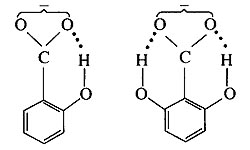
如苯甲酸的电离常数为K,则在邻位、间位、对位上带有羟基时,电离常数依次为15.9 K、1.26K和0.44 K。如左右两边邻位上各取代一羟基,则电离常数为800 K。这是由于邻位上的羟基与苯甲酸根生成带氢键的稳定的阴离子,从而增加了羧基中氢原子的电离度。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
归纳 过二硫酸根 中的过氧键(—O—O—)与过氧化氢结构式(...
电子效应通过改变电子云分布(尤其是化学键的极性、电子离域程...
1、真题呈现: (2023山东--节选)ClO2中心原子为Cl,Cl2O中心原子...
一、螯合物的定义与特点 1. 定义 螯合物是由中心金属离子(或...
一、无机阴离子配体:铜配合物的基础“搭建模块” 无机阴离子...
...