
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
物质内部都储存着能量,即内能。前述“反应物的能量”或“生成物的能量”指的就是相关物质的内能。发生化学反应时,这些内能部分释放。
物质在化学反应中释放(或补充)的能量称为化学能。化学能其实就是反应物总能量与生成物总能量的差值。当化学能以热能形式释放或补充时,对应的热量变化叫做反应的热效应。热效应为零的巧事几乎不能找到。
化学反应的过程是:断开旧键(使原分子拆分为原子或者离子)然后形成新键(原子或离子形成新的分子)。反应过程的能量改变为:断键吸收能量,从而使整个体系能量升高,继而形成新键释放能量从而使体系能量降低,整个过程可以表示为:
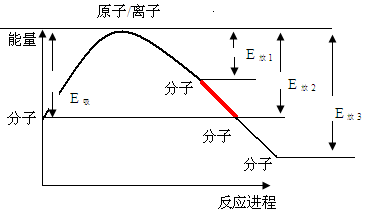
反应拆键所需能量为E吸,合键释放能量为E放,则化学反应过程能量改变为E吸—E放。
化学反应过程的能量改变(反应是吸热还是放热反应)是由断键过程吸收的总能量与合键过程的总能量共同确定的,与反应类型无关;但大多数化合、氧化还原、复分解、置换属于放热变化;分解反应大部分属于吸热过程。这只能说算是一种巧合,没有必然联系。
同样道理是否加热也不是判断反应吸热还是放热的依据
溶解过程大部分可以看做分子拆为离子过程,因此大部分属于吸热过程。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、热化学易错易混提醒 1.放热反应不一定在常温下就能反应,...
在学习《活化能》时,有学生注意到“反应进程—势能图”与学...
【导读】过渡态是反应中稍纵即逝的能量顶峰,化学键将断未断...
多数盐(如铵盐、弱酸盐)水解为吸热反应,典型的盐类水解(如...
化学反应热力学和动力学的区别与联系如下: 一、热力学和动力...
一、概念梳理 中和热是指在稀溶液中,酸与碱发生中和反应生成...