
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、热化学易错易混提醒
1.放热反应不一定在常温下就能反应,吸热反应在常温下也可能发生反应,如NH4Cl(s)与Ba(OH)2·8H2O的反应就是吸热反应,在常温下就能反应。
2.不能根据反应条件判断反应是放热还是吸热,需要加热才能进行的反应不一定是吸热反应,不需要加热就能进行的反应也不一定是放热反应。
3.有能量变化的过程不一定是放热反应或吸热反应,如水结成冰放热但不属于放热反应。
4.旧化学键的断裂和新化学键的形成是同时进行的,缺少任一个过程都不是化学变化。
5.物质发生化学变化都伴有能量的变化,不存在没有能量变化的反应,任何化学反应都具有热效应。
6.活化能越大,表明反应断裂旧化学键需要克服的能量越高。
7.吸热反应中,反应物化学键断裂吸收的总能量高于生成物形成化学键放出的总能量。
8.在化学反应中,反应物各原子之间的化学键不一定完全断裂。
9.同温同压下,反应H2(g)+Cl2(g)==2HCl(g)在光照和点燃条件下的ΔH相同,焓变与反应条件无关。
10.可逆反应的ΔH表示的是完全反应时的热量变化,与反应是否可逆无关、反应进行是否彻底无关。
11.催化剂能降低反应所需活化能,但不影响焓变的大小。
12.热化学方程式中,吸、放热的“+”“-”均不能省略,,且不用标反应条件,热化学方程式的方程系数与热量成比例。
13.有关燃烧热的判断,一看是否以1 mol 可燃物为标准,二看是否生成稳定氧化物。
14.有关中和热的判断,一看是否以生成1 mol H2O为标准,二看酸碱的强弱和浓度,应充分考虑弱酸、弱碱,电离吸热,浓的酸碱稀释放热等因素。
15.强酸和弱碱或弱酸和强碱的稀溶液发生反应,中和热一般小于57.3 kJ·mol-1,因为弱电解质的电离是吸热的。
16.中和反应的实质是H+和OH-化合生成H2O。若反应过程中有其他物质生成(如生成不溶性物质、难电离物质等),这部分反应热不在中和热之内。
17.对于中和热,燃烧热,它们反应放热是确定的,用文字表述燃烧热和中和热时,不用带“-”,而用ΔH表示时,必须带“-”。如甲烷的燃烧热为890.3 kJ·mol-1或甲烷燃烧时ΔH=-890.3 kJ·mol-1。
18.比较反应热大小时不要只比较ΔH数值的大小,还要考虑其符号,放热反应的ΔH数值越大就越小,吸热反应的ΔH数值越大就越大。
19.当反应物与生成物的状态相同时,化学计量数越大,放热反应的ΔH越小,吸热反应的ΔH越大。
20.对于可逆反应,参加反应的物质的量和状态相同时,反应的程度越大,热量变化越大。
二、化学反应历程、机理图分析中易错易混提醒
易错01反应机理
1.反应机理是用来描述某反应物到反应产物所经由的全部基元反应,就是把一个复杂反应分解成若干个基元反应,以图示的形式来描述某一化学变化所经由的全部反应,然后按照一定规律组合起来,从而阐述复杂反应的内在联系,以及总反应与基元反应内在联系。
2.反应机理详细描述了每一步转化的过程,包括过渡态的形成,键的断裂和生成,以及各步的相对速率大小等。典型的是基元反应碰撞理论和基元反应过渡态理论。
3.反应机理中包含的基元反应是单分子反应或双分子反应。完整的反应机理需要考虑到反应物、催化剂、反应的立体化学、产物以及各物质的用量。
4.认识化学反应机理,任何化合物的每一步反应都应该是在该条件下此类化合物的通用反应。
易错02有效碰撞理论
1.化学反应发生的条件:在化学反应中,反应物分子不断发生碰撞,大多数碰撞无法发生反应,只有少数分子的碰撞才能发生化学反应,能发生有效碰撞的分子是活化分子。普通反应物分子形成活化分子所需要的能量叫活化能。而活化分子的碰撞也不一定都能发生有效碰撞。发生有效碰撞不仅有能量的因素,还有空间因素,只有同时满足这两者的要求才能发生有效碰撞。
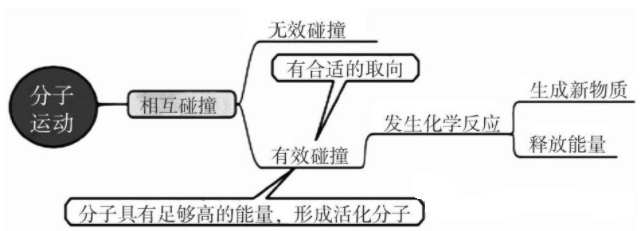
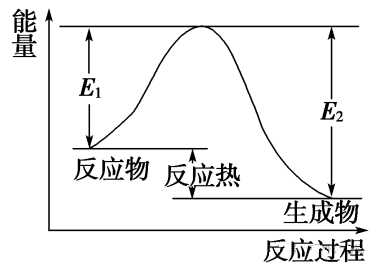
2.反应历程:发生有效碰撞的分子叫做活化分子,活化分子具有较高的能量。活化分子比普通分子所高出的能量称为活化能。活化能越小,普通分子就越容易变成活化分子。如图所示,反应的活化能是E1,反应热是E1-E2。
在一定条件下,活化分子所占的百分数是固定不变的。活化分子的百分数越大,单位体积内活化分子数越多,单位时间内有效碰撞的次数越多,化学反应速率越快。活化能越大,反应速率越慢,化学反应取决于最慢的一步。
易错03催化剂与化学反应
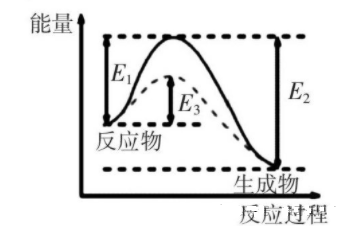
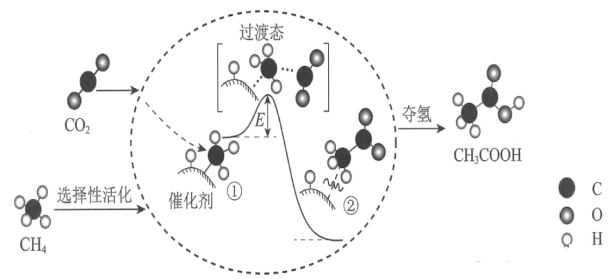
化学反应中,反应分子原有的某些化学键,必须解离并形成新的化学键,这需要一定的活化能。在某些难以发生化学反应的体系中,加入有助于反应分子化学键重排的第三种物质(催化剂)其作用可降低反应的活化能。催化剂能改变反应的途径、降低反应的活化能、加快反应速率,但不能改变反应热的符号与数值、不能改变平衡的移动方向。解答时注意题干信息的理解应用,通过分析化学反应过程,明确反应过程中催化剂的作用和能量变化、化学键的变化。左图虚线表示催化剂对反应的影响,右图为催化反应历程示意图。
易错04认识催化剂的五大误区
误区1:认为催化剂不参加化学反应,实质是:催化剂不是不参加化学反应,而是在化学反应前后,催化剂的化学性质基本不变。
误区2:认为一个反应只有一种催化剂,实质是:一个反应可以有多种催化剂,只是我们常选用催化效率高的,对环境污染小,成本低的催化剂,如双氧水分解的催化剂可以是二氧化锰,也可以是氯化铁,当然还可以硫酸铜等。
误区3:认为催化剂都是加快化学反应速率,实质是:催化剂有正催化剂与负催化剂,正催化剂加快化学反应速率,负催化剂是减慢化学反应速率的。
误区4:认为催化剂的效率与催化剂的量无关,实质是:催化剂参与了化学反应,是第一反应物。既然是反应物,催化剂的表面积,催化剂的浓度大小必然影响化学反应速率。比如高锰酸钾氧化草酸,开始慢,后来速率突然加快,就是开始时生成二价锰离子浓度小,后来生成锰离子浓度大了,氧化速率突然就加快了。催化剂的用量是会改变催化效率的。
误区5:认为催化剂反应前后的性质不变,实质是:催化剂反应前后的化学性质不变,物理性质会发生改变,比如,反应前是块状的,反应后变成了粉末状的。
易错05活化能与决速步
反应活化能较大,反应发生消耗的能量高,则该步反应难进行,其反应速率较小,决速步骤由反应慢的一步反应决定。
易错06催化剂与焓变、转化率
催化剂只能提高反应速率,缩短反应达到平衡的时间,不能改变反应的焓变,也不能控制反应进行的程度。
易错07催化剂与中间产物
催化剂:在连续反应中从一开始就参与了反应,在最后又再次生成,所以仅从结果上来看似乎并没有发生变化,实则是消耗多少后续又生成了多少。
中间产物:在连续反应中为第一步的产物,在后续反应中又作为反应物被消耗,所以仅从结果上来看似乎并没有生成,实则是生成多少后续有消耗多少。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、热化学易错易混提醒 1.放热反应不一定在常温下就能反应,...
在学习《活化能》时,有学生注意到“反应进程—势能图”与学...
【导读】过渡态是反应中稍纵即逝的能量顶峰,化学键将断未断...
多数盐(如铵盐、弱酸盐)水解为吸热反应,典型的盐类水解(如...
化学反应热力学和动力学的区别与联系如下: 一、热力学和动力...
一、概念梳理 中和热是指在稀溶液中,酸与碱发生中和反应生成...