
|
学习小专题 |

|
学习小专题 |
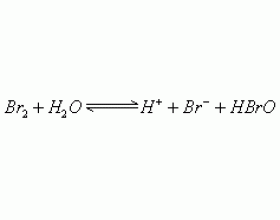 [元素化合物] 使溴水褪色的物质 作者:刘丽颖 来源:未知 日期:2013-03-28 10:27:04 点击:12967 所属专题:溴水
[元素化合物] 使溴水褪色的物质 作者:刘丽颖 来源:未知 日期:2013-03-28 10:27:04 点击:12967 所属专题:溴水
红棕色的单质 溴 溶于 水得到 的混合物俗称溴水,溶于水的 溴只有 少量与水反应。在溴水中存在如下平衡: 溴水中存在三种分子,四种离子,但由于这一反应趋势很小,因此在溴水中 溴主要 以分子形式存在。溴水的颜色由于溶有 溴 单质而呈现橙色。溴水是中学阶段常用于物...
 [元素化合物] 如何正确书写无机化学反应方程式 作者:章金莲 来源:未知 日期:2016-01-17 20:58:27 点击:7991 所属专题:化学方程式
[元素化合物] 如何正确书写无机化学反应方程式 作者:章金莲 来源:未知 日期:2016-01-17 20:58:27 点击:7991 所属专题:化学方程式
化学反应方程式是中学化学基础知识的重要组成部分,只要我们认真分析高中涉及到和高考中所考查的化学反应方程式,就会发现其中蕴涵的规律,下面就如何正确书写无机化学反应方程式谈几点做法。 一、把握高中最重要的两种反应类型 1.复分解反应(以广义酸、碱之间的中和反...
 [元素化合物] 每种酸的特点小结 作者:汪峰 来源:未知 日期:2012-03-06 15:15:00 点击:12378 所属专题:常见酸
[元素化合物] 每种酸的特点小结 作者:汪峰 来源:未知 日期:2012-03-06 15:15:00 点击:12378 所属专题:常见酸
(1)氢氟酸是一种可以腐蚀玻璃的一元弱酸(离子方程式中HF应写成分子式,氟化钠溶液显碱性,请用离子方程式表示其原因),氟化氢分子间因形成氢键而使得它的沸点在卤化氢中最高。 (2)盐酸是一种一元强酸,浓盐酸具有挥发性(瓶口有白雾)、还原性(加热时可以被二氧化锰氧化...
 [元素化合物] 高中无机反应类比失误的教训 作者:汤芹 来源:未知 日期:2012-03-05 18:14:04 点击:14154 所属专题:信息题 类比
[元素化合物] 高中无机反应类比失误的教训 作者:汤芹 来源:未知 日期:2012-03-05 18:14:04 点击:14154 所属专题:信息题 类比
1.金属铁投入硫酸铜溶液发生置换反应有铜析出:Fe+CuSO 4 ===Cu+FeSO 4 类比失误:金属钠投入硫酸铜溶液发生置换反应有铜析出:2Na+CuSO 4 ===Cu+Na 2 SO 4 失误原因: Cu 2+ 的氧化性强于H + ,但Cu 2+ 与金属钠的反应速率远小于水与金属钠的反应速率,故金属钠投入硫酸铜...
 [元素化合物] 化学反应的类比迁移18例 作者:张安荣 来源:未知 日期:2022-08-11 16:27:04 点击:17477 所属专题:化学反应 类比
[元素化合物] 化学反应的类比迁移18例 作者:张安荣 来源:未知 日期:2022-08-11 16:27:04 点击:17477 所属专题:化学反应 类比
类比思维能帮助我们认识一类本质相似的问题,找出物质变化遵循的共同规律,是利用“已知”解决“未知”的一种有效策略,达到举一反三、触类旁通、以点带面、事半功倍的学习效果。现将中学化学中可类比的部分物质性质举例如下。 1.H 2 O与NH 3 类比 电离:2H 2 O H 3 O ...
 [元素化合物] 中学化学中硫酸的作用 作者:张扬 来源:未知 日期:2016-06-01 15:32:21 点击:12604 所属专题:硫酸作用
[元素化合物] 中学化学中硫酸的作用 作者:张扬 来源:未知 日期:2016-06-01 15:32:21 点击:12604 所属专题:硫酸作用
一、制取许多气体的重要试剂 1.制H 2 (利用硫酸的酸性或H + 离子的氧化性): Zn+H 2 SO 4 (稀)==ZnSO 4 +H 2 ↑;Fe+H 2 SO 4 (稀)==FeSO 4 +H 2 ↑ 2.制SO 2 (①利用硫酸的酸性;②利用硫酸的强氧化性和酸性): ①Na 2 SO 3 +H 2 SO 4 (中等浓度)==Na 2 SO 4 +...
 [元素化合物] 中学化学中氢氧化钠的作用 作者:张楠 来源:未知 日期:2023-03-02 10:37:44 点击:26226 所属专题:氢氧化钠
[元素化合物] 中学化学中氢氧化钠的作用 作者:张楠 来源:未知 日期:2023-03-02 10:37:44 点击:26226 所属专题:氢氧化钠
氢氧化钠是学生从初中开始学习化学时就接触到的强碱性物质,它在整个高中学习中有着极其重要的作用,广泛用于各种生产生活过程和化学解题过程中。如果能熟练地运用氢氧化钠的性质,将整个高中的知识贯穿起来,使其成为联系各类物质的纽带,那么,以氢氧化钠为主体的完整...
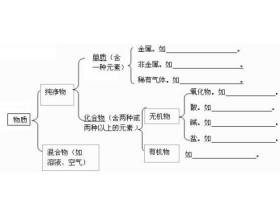 [注解与辨疑2] 酸碱盐知识归纳 作者:孙法军 来源:未知 日期:2016-01-17 15:01:05 点击:15217 所属专题:物质分类 酸碱盐
[注解与辨疑2] 酸碱盐知识归纳 作者:孙法军 来源:未知 日期:2016-01-17 15:01:05 点击:15217 所属专题:物质分类 酸碱盐
一 、酸、碱、盐的概念 物质 酸 碱 盐 概念 电离时解离出的阳离子全部是 氢离子 的化合物 电离时解离出的阴离子全部是 氢氧根 离子的化合物 由金属阳离子(或NH 4 + )和酸根阴离子组成的化合物 形式 酸 = H + + 酸根阴离子 碱 = 金属阳离子+OH - 盐=金属阳离子+酸根阴...
 [元素化合物] 常见的既能与酸又能与碱反应的物质 作者:章文 来源:未知 日期:2012-03-02 09:39:38 点击:3511 所属专题:两性物质
[元素化合物] 常见的既能与酸又能与碱反应的物质 作者:章文 来源:未知 日期:2012-03-02 09:39:38 点击:3511 所属专题:两性物质
⑴金属:Al、Zn ⑵非金属:Si(Si +3HCl SiHCl 3 +H 2 ↑) S(3S+6NaOH 2Na 2 S+Na 2 SO 3 +3H 2 O) ⑶两性氧化物:Al 2 O 3 、ZnO ⑷两性氢氧化物:Al(OH) 3 、Zn(OH) 2 ⑸弱酸的铵盐:(NH 4 ) 2 S、(NH 4 ) 2 SO 3 、CH 3 COONH 4 ⑹弱酸的酸式盐:NaHCO 3 、NaHS...
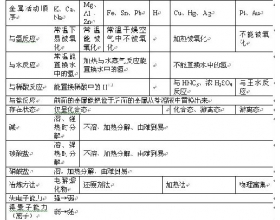 [元素化合物] 金属活动性顺序在化学反应中的应用 作者:黄晓东 来源:未知 日期:2012-03-02 09:50:07 点击:12814 所属专题:金属活动顺序表
[元素化合物] 金属活动性顺序在化学反应中的应用 作者:黄晓东 来源:未知 日期:2012-03-02 09:50:07 点击:12814 所属专题:金属活动顺序表
⑴金属与酸反应:K Ca Na Mg A l Zn Fe Sn Pb (H) Cu Hg Ag Pt Au a、氢以前的金属能置换非氧化性酸中的氢:2Al+3H 2 SO 4 =Al 2 (SO 4 ) 3 +3H 2 ↑ b、氢以后的金属不能跟非氧化酸反应。只能与强氧化性酸反应: 3Cu+8HNO 3 (稀)=3Cu(NO 3 ) 2 +2NO↑+4H 2 O ...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。鲍林在研究含氧酸时,将其化学式一般写作 HRO,其中 R 代表中心原子,羟基(–OH)与...
...
一、银47Ag 银亲硫,极化能力强。在自然界中常以自然银、硫化物等形式存在,因其离子...
一、镓Ga 从铝土矿Al 2 O 3 或闪锌矿Zns的冶炼过程中提取,最后经电解制得纯净镓。 门...
一、铁 Fe 古代社会铁器时代大约起始于 前 2000 年 ,最早发现和使用的铁是来自外空的...
一、钪Sc 1、单质是柔软、银白色。熔点1500℃以上。钪常用来制特种玻璃、轻质耐高温合...
一、氢 H 1 、 H ,是原子半径最小的元素,有 H (氕)、 D (氘)、 T (氚)等核素...
一、钠Na 大量存在于海水中,矿物主要有钠长石NaAlSi3O8、岩盐NaCl、钠硝石NaNO3等。 ...