
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
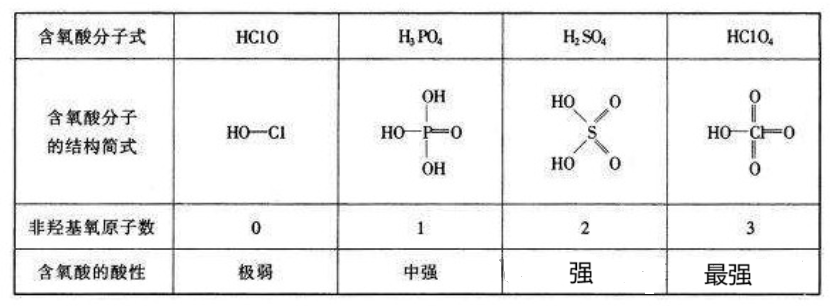
鲍林在研究含氧酸时,将其化学式一般写作 HₘROₙ,其中 R 代表中心原子,羟基(–OH)与非羟基氧原子共存。鲍林发现,含氧酸的酸性主要取决于分子中非羟基氧原子(n)的数量。当 n 增加时,R 原子的氧化态提高,其电负性增强,从而对羟基氧起到较强的电子拉吸作用,使 O–H 键极化加剧,H⁺ 更容易离解。简言之,非羟基氧原子越多,酸性越强。例如:
硅酸(H₄SiO₄)
中心原子硅的氧化态较低(n = 0),酸性非常弱;
磷酸(H₃PO₄)
含有 1 个非羟基氧(n = 1),酸性中等;
硫酸(H₂SO₄)
含有 2 个非羟基氧(n = 2),酸性强;
高氯酸(HClO₄)
含有 3 个非羟基氧(n = 3),属于极强酸。
鲍林对强弱酸的划定
按上述规则,鲍林的划分如下:
最弱酸:
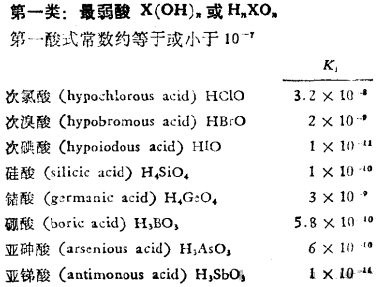
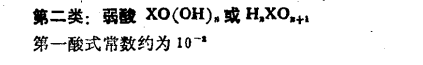



例外的酸:


 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
...
【导读】无机非典型水解遵循正价接OH⁻,负价接H⁺的核心“电...
1.P 4 常见危险化学品的标志,主要知道常见物质的性质与标志相...
1. 还原性 Fe 粉可做干燥剂,脱氧剂又可叫做双吸剂,抗氧化剂...
化学的世界五彩缤纷,物质的颜色不仅构成了化学学科的视觉美...
磷作为周期表第 ⅤA 族核心元素,兼具 “生命不可替代性”(构...