
|
学习小专题 |

|
学习小专题 |
 [元素化合物] 酸的浓度不同,反应情况不同的小结 作者:赵胜 来源:未知 日期:2022-08-12 10:27:36 点击:15379 所属专题:常见酸
[元素化合物] 酸的浓度不同,反应情况不同的小结 作者:赵胜 来源:未知 日期:2022-08-12 10:27:36 点击:15379 所属专题:常见酸
当化学反应进行时,反应物不断被消耗,随反应的进行,反应物浓度不断改变,发生反应情况就会各不相同,现小结如下,并结合有关化学方程式以及相对应的试题解析理解不同反应情况的本质原因。 1 .酸的浓度不同,产物可能不同。 如过量的金属与浓酸反应的情况。 ①在一定...
 [元素化合物] 典型物质的典型性质 作者:陈女婷 来源:未知 日期:2013-02-28 11:20:14 点击:7393 所属专题:重要物质
[元素化合物] 典型物质的典型性质 作者:陈女婷 来源:未知 日期:2013-02-28 11:20:14 点击:7393 所属专题:重要物质
一,钠: 1. 钠的存在与获取(化合态,电解熔融盐); 2. 钠的活泼性(与水或酸,与氧或氯等非金属,与醇); 3. 过氧化钠作供氧剂(与水和二氧化碳反应,其他过氧化物); 4. 碳酸钠与碳酸氢钠的比较(热稳定性,水解与碱性,溶解性,与酸反应); 5 .碱金属性质递变小结...
 [元素化合物] 高中化学反应先后分析方法 作者:韩富军 来源:未知 日期:2016-01-07 12:42:17 点击:8715 所属专题:化学先后
[元素化合物] 高中化学反应先后分析方法 作者:韩富军 来源:未知 日期:2016-01-07 12:42:17 点击:8715 所属专题:化学先后
打扫卫生,先擦窗还是先擦桌椅?擦窗要踩在桌椅上,桌椅还得重擦。穿衣服,先穿内衣还是先穿外套?是否得重来。搭建实验装置,先固定下位还是上位,实际也是一个是否需要重来的问题。 [例1]已知氧化性,Br 2 Fe 3+ I 2 ;还原性I - Fe 2+ Br - (1)将少量Cl 2 通入FeBr 2...
 [元素化合物] 学法指导:非金属元素及其化合物复习方法 作者:杨帆 来源:未知 日期:2020-03-05 12:14:33 点击:25064 所属专题:非金属及其化合物
[元素化合物] 学法指导:非金属元素及其化合物复习方法 作者:杨帆 来源:未知 日期:2020-03-05 12:14:33 点击:25064 所属专题:非金属及其化合物
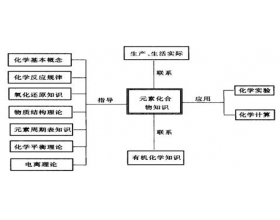
考纲要求: 常见非金属元素(如 H 、 C 、 N 、 O 、 Si 、 S 、 Cl 等) 1 .掌握常见非金属元素单质及其重要化合物的主要性质,了解其应用。 2 .了解常见非金属元素单质及其重要化合物对环境质量的影响。 3 .以上各部分知识的综合应用 知识网络 学法指导 1 . 构建...
 [元素化合物] 中学化学中常见酸的特殊性质归纳 作者:李留记 来源:未知 日期:2016-01-07 12:48:36 点击:12370 所属专题:常见酸 一般与特殊 反常
[元素化合物] 中学化学中常见酸的特殊性质归纳 作者:李留记 来源:未知 日期:2016-01-07 12:48:36 点击:12370 所属专题:常见酸 一般与特殊 反常
1 、不稳定性酸 这部分酸包括 H 2 CO 3 、 H 2 SO 3 、 HClO 、 HNO 3 (浓)、 H 4 SiO 4 、氢硫酸( H 2 S )、氢碘酸( HI )、氢硒酸( H 2 Se )、氢碲酸( H 2 Te )等。 ( 1 )常温(或微热)易分解的酸: H 2 CO 3 、 H 2 SO 3 、 HNO 3 (浓)、 H 4 SiO 4 等...
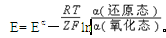 [元素化合物] 剖析金属活动性顺序表在中学化学中的运用 作者:张红 来源:未知 日期:2016-01-18 16:19:59 点击:16054 所属专题:金属活动性顺序表
[元素化合物] 剖析金属活动性顺序表在中学化学中的运用 作者:张红 来源:未知 日期:2016-01-18 16:19:59 点击:16054 所属专题:金属活动性顺序表
一、金属活动性顺序表的发现 1865年,俄国学者贝开托夫(Beketob)在实验的基础上,研究了金属单质与水、酸及盐溶液间进行置换反应的速度,发表了《对某一元素为另一元素所置换的研究》论文,总结出金属活动性顺序为: K Na Ca Mg Zn Fe Sn Pb (H) Cu Hg Ag Pt Au 在这...
 [元素化合物] 利用配平诗集配平 作者:刘明 来源:未知 日期:2012-05-09 21:53:35 点击:33732 所属专题:化学方程式配平
[元素化合物] 利用配平诗集配平 作者:刘明 来源:未知 日期:2012-05-09 21:53:35 点击:33732 所属专题:化学方程式配平
这部分诗包括六首小诗,前五首向你介绍了化学反应方程式的五种配平方法,第六首诗告诉你在实际配平过程中,如何灵活巧妙地运用这五种方法。如果你能记住并理解这六首小诗,那么你就可以自豪地说:“世界上没有一个化学反应方程式我不会配平……” 歧化反应的简捷配平法 三种...
 [元素化合物] 话说酸的“六个”不一定 作者:陈恒 来源:未知 日期:2021-10-12 15:00:47 点击:5113 所属专题:常见酸 是非判断
[元素化合物] 话说酸的“六个”不一定 作者:陈恒 来源:未知 日期:2021-10-12 15:00:47 点击:5113 所属专题:常见酸 是非判断
㈠.名称叫酸的物质不一定是酸。 例如:石炭酸(苯酚),虽然它显示出了一定的弱酸性,但是它仍然属于酚而不属于酸。 ㈡.无氧酸不一定是非金属元素的氢化物的水化物。 例如:氢氰酸(HCN)。 ㈢.酸的元数不一定等于其分子中的H原子数。 例如:亚磷酸(H 3 PO 3 )是二元...
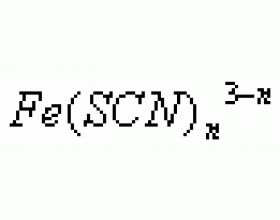 [元素化合物] 常见的物质颜色 作者:王瑜 来源:未知 日期:2012-03-27 09:08:52 点击:12213 所属专题:物质颜色
[元素化合物] 常见的物质颜色 作者:王瑜 来源:未知 日期:2012-03-27 09:08:52 点击:12213 所属专题:物质颜色
一. 常见的物质颜色 1. 红色 部分含三价铁的化合物:Fe(OH) 3 红褐色(胶体或沉淀), 血红色溶液,Fe 2 O 3 红棕色粉末,Fe 2 O 3 ·nH 2 O(铁锈)红棕色固体。 液Br 2 为深红棕色液体,Br 2 蒸气和NO 2 为红棕色气体。红磷为红棕色固体,苯酚在空气中久置变为粉红色。 2....
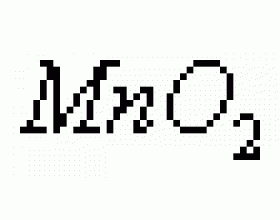 [元素化合物] 条件不同 产物各异 作者:田兴虎 来源:未知 日期:2016-03-09 18:37:55 点击:18778 所属专题:条件与产物
[元素化合物] 条件不同 产物各异 作者:田兴虎 来源:未知 日期:2016-03-09 18:37:55 点击:18778 所属专题:条件与产物
在化学反应过程中,由于反应条件、反应物的物质的量不同等原因,往往使反应进程发生改变,导致反应生成物的不同。中学化学中涉及到的这类反应很多,学习、掌握和运用这些反应,不仅可以深刻理解化学反应实质,且有利于培养严谨的科学态度,使知识得以升华。 一、反应物...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。鲍林在研究含氧酸时,将其化学式一般写作 HRO,其中 R 代表中心原子,羟基(–OH)与...
...
一、银47Ag 银亲硫,极化能力强。在自然界中常以自然银、硫化物等形式存在,因其离子...
一、镓Ga 从铝土矿Al 2 O 3 或闪锌矿Zns的冶炼过程中提取,最后经电解制得纯净镓。 门...
一、铁 Fe 古代社会铁器时代大约起始于 前 2000 年 ,最早发现和使用的铁是来自外空的...
一、钪Sc 1、单质是柔软、银白色。熔点1500℃以上。钪常用来制特种玻璃、轻质耐高温合...
一、氢 H 1 、 H ,是原子半径最小的元素,有 H (氕)、 D (氘)、 T (氚)等核素...
一、钠Na 大量存在于海水中,矿物主要有钠长石NaAlSi3O8、岩盐NaCl、钠硝石NaNO3等。 ...