
|
学习小专题 |

|
学习小专题 |
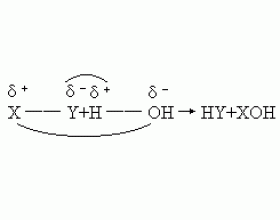 [有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11696 所属专题:水解反应 有机反应
[有机化学] 水解反应面面观 作者:周广 来源:未知 日期:2016-01-08 22:24:24 点击:11696 所属专题:水解反应 有机反应
所谓水解反应,即物质跟水发生的相互变换成分的反应.用通式可表示为: 反应的机理可简单地认为是:共价键(X—Y键、H—O键)断裂(一般地,一个水分于中只有一个H—O键断裂),再按异电相吸原则,重新组合成新键即得产物.至于离子键则视为共价键的极限情形.各类水解...
 [注解与辨疑j] 酸式盐水溶液的酸碱性概括小结 作者:徐志宏 来源:未知 日期:2012-05-16 09:43:40 点击:8056 所属专题:酸式盐 酸碱性判断
[注解与辨疑j] 酸式盐水溶液的酸碱性概括小结 作者:徐志宏 来源:未知 日期:2012-05-16 09:43:40 点击:8056 所属专题:酸式盐 酸碱性判断
(1)强碱强酸酸式盐 由于在水溶液中只能进一步电离出H + ,不会发生水解,所以只具备酸性,可代替一元强酸使用,如: NaHSO 4 +NaHCO 3 =Na 2 SO 4 +H 2 O+CO 2 ↑ NaHSO 4 +NaCl Na 2 SO 4 +HCl↑ (2)强碱弱酸酸式盐 由于强碱弱酸酸式盐中含有弱酸酸式根,既可以进一步...
 [注解与辨疑j] FeCl3溶液与Na2S溶液反应生成什么? 作者:张劲辉 来源:未知 日期:2012-05-16 09:22:31 点击:9706 所属专题:氯化铁 双水解反应
[注解与辨疑j] FeCl3溶液与Na2S溶液反应生成什么? 作者:张劲辉 来源:未知 日期:2012-05-16 09:22:31 点击:9706 所属专题:氯化铁 双水解反应
问:“在FeCl 3 溶液中加入Na 2 S溶液发生的反应有两种说法,一是: 2Fe 3+ +S 2- =2Fe 2+ +S↓; 又一为: 2Fe 3+ +3S 2- +6H 2 O=2Fe(OH) 3 ↓+3H 2 S↑ 这两种说法哪个正确? 答:一般说来,Fe 3+ 具有较强的氧化性,而S 2- 则具有还原性,因此当Fe 3+ 与S 2- 相遇时,Fe...
 [注解与辨疑j] 影响电离度的因素 作者:吴传鹏 来源:未知 日期:2012-05-16 09:19:41 点击:12177 所属专题:电离度 电离平衡
[注解与辨疑j] 影响电离度的因素 作者:吴传鹏 来源:未知 日期:2012-05-16 09:19:41 点击:12177 所属专题:电离度 电离平衡
①电解质的结构 具有离子键或强极性的分子在水溶液中的电离度均很大,几乎是100%。弱极性或非极性分子在水中呈微弱电离甚至不电离。电解质中键的极性越大,其电离度也越大。离子化合物的电离度取决于离子电荷及离子半径。离子电荷越高,半径越小,则其电离度越...
 [注解与辨疑j] 电离常数和电离度有什么关系? 作者:羊绍敬 来源:未知 日期:2012-05-16 08:41:29 点击:40830 所属专题:电离平衡常数 电离度
[注解与辨疑j] 电离常数和电离度有什么关系? 作者:羊绍敬 来源:未知 日期:2012-05-16 08:41:29 点击:40830 所属专题:电离平衡常数 电离度
(1)弱电解质的电离是一种可逆过程。以醋酸的电离为例,醋酸溶于水后,它的分子即电离为H+离子和CH 3 COO - 离子,这是正过程,同时逆过程是H + 离子和CH 3 COO - 离子重新结合成醋酸分子。 CH 3 COOH H + +CH 3 COO - 在这个过程中,CH 3 COOH分子电离的速率(正反应的速率)...
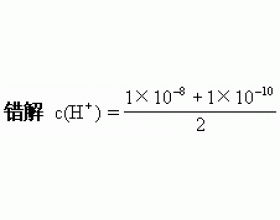 [注解与辨疑j] pH拾零 作者:潘祥泰 来源:未知 日期:2016-02-02 19:49:52 点击:9057 所属专题:ph值 ph计算
[注解与辨疑j] pH拾零 作者:潘祥泰 来源:未知 日期:2016-02-02 19:49:52 点击:9057 所属专题:ph值 ph计算
一、pH与酸碱性 1.溶液酸碱性的强弱由pH决定,与温度、溶质无关。如:pH均为2的硫酸溶液与醋酸溶液酸度相同。 2.pH等于7的溶液不一定呈中性。(“pH=7为中性”习惯上指常温时) 二、 pH的计算 1.计算时先确定溶液的酸碱性,计算顺序为:酸性→c(H + )→pH;碱性→c(O...
 [注解与辨疑j] 为什么要引入“pH” 作者:罗翊轩 来源:未知 日期:2016-03-09 21:47:08 点击:3179 所属专题:ph值
[注解与辨疑j] 为什么要引入“pH” 作者:罗翊轩 来源:未知 日期:2016-03-09 21:47:08 点击:3179 所属专题:ph值
溶液的酸碱度,可用[H + ]或[OH - ]表示。但我们常碰到的某些溶液的酸度或碱度很...
 [注解与辨疑j] 小议强酸和弱酸的区别 作者:熊振典 来源:未知 日期:2012-05-15 18:31:07 点击:7366 所属专题:强酸与弱酸比较
[注解与辨疑j] 小议强酸和弱酸的区别 作者:熊振典 来源:未知 日期:2012-05-15 18:31:07 点击:7366 所属专题:强酸与弱酸比较
1强酸在水溶液中全部电离,不存在溶质分子;弱酸在水溶液中部分电离,因存在电离平衡,所以既含溶质离子,又含溶质分子. 2 pH相同的强酸和弱酸,弱酸的物质的量浓度大于强酸的. 3同温度、同浓度的强酸溶液的导电性强于弱酸溶液的. 4中和同体积、同pH的强酸和弱酸,弱酸的...
 [注解与辨疑j] 纯水的电离度是多大? 作者:刘学超 来源:未知 日期:2012-05-15 18:26:17 点击:7825 所属专题:水的电离 电离度
[注解与辨疑j] 纯水的电离度是多大? 作者:刘学超 来源:未知 日期:2012-05-15 18:26:17 点击:7825 所属专题:水的电离 电离度
生活中,我们一般会认为纯水是不导电的。但根据精确的实验证明,水是一种极弱的电解质,它能微弱地电离,生成水合氢离子和氢氧根离子。其电离方程式可表示为: H 2 O+H 2 O H 3 O + +OH - 可简写为:H 2 O H + +OH - ,从纯水的导电实验测得,在25℃(常温)时,纯水中H + 和...
 [注解与辨疑j] 酸碱中和反应三种终点的比较 作者:翟娜 来源:未知 日期:2016-02-02 20:25:30 点击:14717 所属专题:中和滴定
[注解与辨疑j] 酸碱中和反应三种终点的比较 作者:翟娜 来源:未知 日期:2016-02-02 20:25:30 点击:14717 所属专题:中和滴定
酸碱中和反应的终点在理论上应是酸碱恰好完全反应的点(即化学反应的计量点)。但在中和滴定实验中,被滴定的溶液通常不发生任何外观变化,需要借助酸碱指示剂的颜色变化来指示滴定的终点。另外有时还会提出中和至中性的点。上述三种终点之间的区别和联系,我们在学习时...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【易错点01】弱电解质的判断有关的易错点 (1)在相同浓度、相同...
金属离子沉淀PH值表格(20℃) 金属离子浓度 10^-1 10^-2 10^-3 10^-4 1...
在高中化学的教学中,我们常常会将一些题目练习中总结出来的...
一.碱线 Fe(OH)3的溶度积,Ksp=[Fe3+][OH-]3,在直角坐标图中,[Fe...
沉淀转化不只看 K sp 大小!这些反应原理高中生必须掌握 在高中...
酚酞变红的核心原理,是它在碱性溶液中发生了分子结构的转变...
什么是“软硬酸碱理论”,1963 年,拉尔夫・皮尔逊提出软硬酸...
水溶液中NH水解显酸性,CO、HCO水解显碱性,二者会发生“相互促...