
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑j] 透析电解质中的八大关系 作者:舒龙昌 来源:未知 日期:2016-02-02 20:34:29 点击:32017 所属专题:电解质判断 弱电解质判断
[注解与辨疑j] 透析电解质中的八大关系 作者:舒龙昌 来源:未知 日期:2016-02-02 20:34:29 点击:32017 所属专题:电解质判断 弱电解质判断
一.电解质、非电解质概念间的关系 电解质是指在水溶液中或熔化状态下能够导电的化合物;非电解质是指在水溶液中和熔化状态下都不能够导电的化合物。显然电解质和非电解质是对化合物的一种分类,因此混合物既不是电解质也不是非电解质。此外“不是电解质”与非电解质不...
 [注解与辨疑j] 强电解质和弱电解质怎么分? 作者:黄元 来源:未知 日期:2014-11-25 10:37:37 点击:5125 所属专题:弱电解质判断
[注解与辨疑j] 强电解质和弱电解质怎么分? 作者:黄元 来源:未知 日期:2014-11-25 10:37:37 点击:5125 所属专题:弱电解质判断
在水溶液中全部电离的电解质叫做强电解质,部分电离的电解质叫做弱电解质。 强酸、强碱和绝大多数可溶性的盐在水溶液里都能全部电离,它们都是强电解质。弱酸、弱碱在水溶液里只能部分电离,它们都是弱电解质。 从化合物结构来看,有典型离子键的化合物(如强碱和大部分...
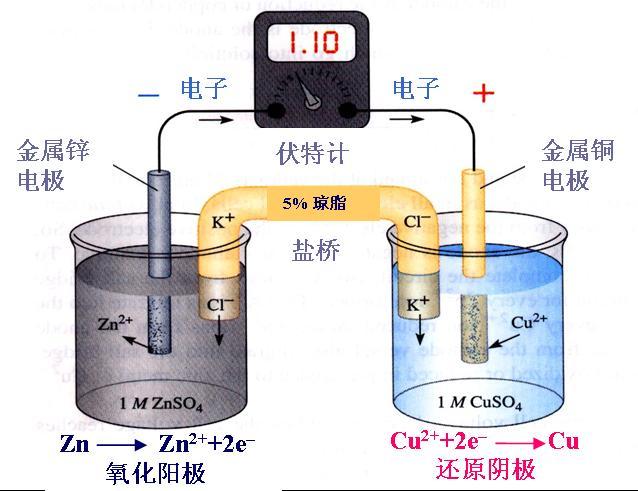 [注解与辨疑j] 同离子效应 作者:黄元 来源:未知 日期:2016-02-02 20:47:55 点击:8557 所属专题:同离子效应
[注解与辨疑j] 同离子效应 作者:黄元 来源:未知 日期:2016-02-02 20:47:55 点击:8557 所属专题:同离子效应
由于加入含相同离子的强电解质,使弱电解质电离度减小或使难溶盐溶解度降低的效应,叫同离子效应。分别说明如下: ①使弱电解质电离度减小 例如,在醋酸溶液中加人醋酸钠,由于醋酸钠是强电解质、在水中全部电离成Na + 和Ac - ,溶液中Ac - 浓度增大,大量的Ac - 同H + ...
 [注解与辨疑j] 盐效应 作者:许雁祥 来源:未知 日期:2012-03-12 19:28:47 点击:12614 所属专题:盐效应
[注解与辨疑j] 盐效应 作者:许雁祥 来源:未知 日期:2012-03-12 19:28:47 点击:12614 所属专题:盐效应
在弱电解质溶液中,如加入其他强电解质盐时,则该弱电解质的电离度将会增大。例如在 0 . 1 mol/L HAc 溶液中,加入 0 . 1 mol/L NaCl 则 c ( H + )不再是 1 . 33 × 10 -3 mol/L ,而是 1 . 68 × 10 -3 mol/L ;其电离度也不是 1 . 33% ,而是 1 . 68% 了。这种影响,叫...
 [注解与辨疑j] 决定强、弱电解质的因素是什么? 作者:龙立球 来源:未知 日期:2018-07-19 16:27:16 点击:19541 所属专题:弱电解质
[注解与辨疑j] 决定强、弱电解质的因素是什么? 作者:龙立球 来源:未知 日期:2018-07-19 16:27:16 点击:19541 所属专题:弱电解质
决定强、弱电解质的因素较多,有时一种物质在某种情况下是强电解质,而在另一种情况下,又可以是弱电解质。下面从键型、键能、溶解度、浓度和溶剂等方面来讨论这些因素对电解质电离的影响。 (1)电解质的键型不同,电离程度就不同。 已知典型的离子化合物,如强碱(NaOH、...
 [注解与辨疑j] 盐类是否都是强电解质? 作者:张超鹏 来源:未知 日期:2017-04-18 11:36:43 点击:7614 所属专题:强电解质
[注解与辨疑j] 盐类是否都是强电解质? 作者:张超鹏 来源:未知 日期:2017-04-18 11:36:43 点击:7614 所属专题:强电解质
大多数盐类是强电解质,少数的盐有形成共价键的倾向,电离度很小,属于弱电解质。 例如,氯化汞、碘化镉等虽然也是由离子组成的,但是Hg 和Cd 容易被阴离子所极化,而C1 、I 等又是容易极化的阴离子,由于阳、阴离子间的相互极化作用,电子云产生较大的变形,引起了键的...
 [注解与辨疑j] 三氯化铁溶液的水解及应用 作者:董啸 来源:未知 日期:2016-02-02 21:08:47 点击:21938 所属专题:三氯化铁 盐类水解应用
[注解与辨疑j] 三氯化铁溶液的水解及应用 作者:董啸 来源:未知 日期:2016-02-02 21:08:47 点击:21938 所属专题:三氯化铁 盐类水解应用
一、基本原理: FeCl 3 属于强酸弱碱盐,溶于水后Fe 3+ 发生水解,使溶液显酸性。 FeCl 3 +3H2O Fe(OH) 3 +3HCl,离子方程式为Fe 3+ +3H2O Fe(OH) 3 +3H + 。实验测得,FeCl 3 的水解程度较大,在加热或稀释条件下,水解平衡正向移动,如果加入电解质会影响到溶液中H+浓...
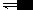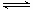 [注解与辨疑j] 电离平衡中疑点、易错点 作者:汪峰 来源:未知 日期:2013-02-26 15:42:07 点击:15599 所属专题:电离平衡
[注解与辨疑j] 电离平衡中疑点、易错点 作者:汪峰 来源:未知 日期:2013-02-26 15:42:07 点击:15599 所属专题:电离平衡
1 电离平衡 疑点一:电解质和非电解质的概念 解析:电解质:在水溶液里或熔化状态下能够导电的化合物。 非电解质:在水溶液里或熔化状态下都不导电的化合物。 (1)电解质、非电解质均是化合物,它们是根据在一定条件下能否电离加以区分的,单质、混合物既不是电解质也不...
 [注解与辨疑j] 相等pH的弱酸和强酸混合的pH计算 作者:李兴 来源:未知 日期:2016-02-02 19:47:24 点击:14555 所属专题:ph计算
[注解与辨疑j] 相等pH的弱酸和强酸混合的pH计算 作者:李兴 来源:未知 日期:2016-02-02 19:47:24 点击:14555 所属专题:ph计算
题目 : 将 pH=3 的 HCl 和 pH=3 的 CH 3 COOH 等体积混合时,所得溶液的 pH 是( ) A. 3 B. 小于 3 C. 大于 3 题解 : pH=3 的 HCl 和 pH=3 的 CH 3 COOH 等体积混合,若平衡 CH 3 COOH= H + +CH 3 COO 右移,混合溶液的 pH 小于 3 ,若平衡左移, pH 大于 3 ,若平衡...
 [注解与辨疑j] 碳酸氢钠溶液中离子浓度大小的比较 作者:李小明 来源:未知 日期:2012-01-12 09:37:22 点击:21187 所属专题:碳酸氢钠01 离子浓度大小比较
[注解与辨疑j] 碳酸氢钠溶液中离子浓度大小的比较 作者:李小明 来源:未知 日期:2012-01-12 09:37:22 点击:21187 所属专题:碳酸氢钠01 离子浓度大小比较
碳酸氢钠溶液中离子浓度大小的比较问题存在着较大的分歧,最关键的问题是[OH - ]、[H + ]和[CO 3 2- ]的大小比较。 观点为1:在碳酸氢钠溶液中每电离1mol HCO 3 - ,便产生1mol CO 3 2- 和1mol H + ,在这个基础上再考虑水的电离,而每1mol水的电离便产生1mol H + 和1mol OH...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
【易错点01】弱电解质的判断有关的易错点 (1)在相同浓度、相同...
金属离子沉淀PH值表格(20℃) 金属离子浓度 10^-1 10^-2 10^-3 10^-4 1...
在高中化学的教学中,我们常常会将一些题目练习中总结出来的...
一.碱线 Fe(OH)3的溶度积,Ksp=[Fe3+][OH-]3,在直角坐标图中,[Fe...
沉淀转化不只看 K sp 大小!这些反应原理高中生必须掌握 在高中...
酚酞变红的核心原理,是它在碱性溶液中发生了分子结构的转变...
什么是“软硬酸碱理论”,1963 年,拉尔夫・皮尔逊提出软硬酸...
水溶液中NH水解显酸性,CO、HCO水解显碱性,二者会发生“相互促...