
|
学习小专题 |

|
学习小专题 |
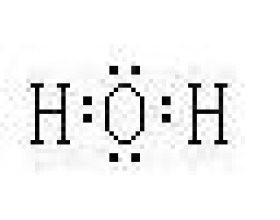 [探讨与扩展e] 路易斯结构理论与路易斯结构式 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 11:36:27 点击:3584 所属专题:路易斯结构式
[探讨与扩展e] 路易斯结构理论与路易斯结构式 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 11:36:27 点击:3584 所属专题:路易斯结构式
由于对简单的非过渡元素分子或离子,通过观察即可写出其路易斯结构式,所以路易斯结构理论实际上是中学化学中最重要的结构理论。虽然人们因其不能解释PCl5等类物质的结构,而常对其加以质疑,但仍无法撼动其在化学中的地位。以至于现在有相当一部分大学化学教材和教学参考书...
 [探讨与扩展e] 几种价层电子数计算方法间的关系 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 11:24:59 点击:4497 所属专题:价层电子对数计算
[探讨与扩展e] 几种价层电子数计算方法间的关系 作者:伍伟夫 来源:化学原理补正 日期:2021-08-16 11:24:59 点击:4497 所属专题:价层电子对数计算
在用价层电子对互斥理论来讨论分子的空间构型时,要先确定某中心原子的价层电子数,进而得到价层电子对数。在不同的教材中,确定中心原子价层电子对数目的方法往往有显著区别,但判别结果都能相同。了解这诸多的方法间共同的合理内核,对推广价层电子对互斥理论的应用肯定是...
 [探讨与扩展e] 比电负性差值更能精准确定键型的方法——Ketelaar三角 作者:化学自习室 来源:一个芦老师 日期:2021-07-22 09:09:38 点击:2491 所属专题:共价键 离子键
[探讨与扩展e] 比电负性差值更能精准确定键型的方法——Ketelaar三角 作者:化学自习室 来源:一个芦老师 日期:2021-07-22 09:09:38 点击:2491 所属专题:共价键 离子键
高中教学中, 电负性差值是一种非常简单的判断化学键键型的方法:成键的两种元素电负性差值小于 1.7 即为共价键(或者说以共价键为主),大于 1.7 即为离子键(或者说以离子键为主)。但这是很粗糙,并且不能够完全适用的方法。举几个例子来说明:金属 Na 中元素的电负...
 [探讨与扩展e] 臭氧是含非极性键的非极性分子吗? 作者:苑凌云 来源:追寻化学教育的本源 日期:2021-07-08 16:29:47 点击:1866 所属专题:分子极性
[探讨与扩展e] 臭氧是含非极性键的非极性分子吗? 作者:苑凌云 来源:追寻化学教育的本源 日期:2021-07-08 16:29:47 点击:1866 所属专题:分子极性
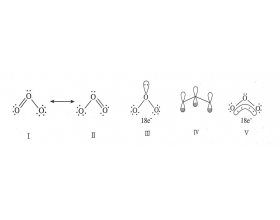
Ⅰ和Ⅱ为路易斯结构式;Ⅲ标出了总电子数;Ⅳ表明了3个平行p轨道;Ⅴ为大π键的结构式。 中心氧原子的杂化类型:sp 2 杂化 ;成键类型:2个σ键,1个 离域大π键; 立体构型:V形。 键长:127.8 pm(该键长正好介于氧原子间的单键键长148 pm与双 键键长112 pm之间); 键角:1...
 [探讨与扩展e] 解密非常规氢键 作者:化学自习室 来源:未知 日期:2021-03-02 09:01:56 点击:859 所属专题:氢键02
[探讨与扩展e] 解密非常规氢键 作者:化学自习室 来源:未知 日期:2021-03-02 09:01:56 点击:859 所属专题:氢键02
一、氢键的形成条件 参考文献: 1、周公度《结构和物性—化学原理的应用》第三版P95和P78 2、麦松威《高等无机结构化学》P333 3、徐光宪《物质结构》P586 氢键以X-Y…H表示,其中X和Y的电负性越大,半径越小,则氢键越强。 如N、O、F, C的电负性不够大,但是与它连接的...
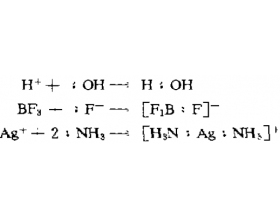 [探讨与扩展e] 软硬酸碱规则与配合物的稳定性 作者:化学自习室 来源:未知 日期:2021-05-21 11:10:51 点击:12249 所属专题:配合物稳定性
[探讨与扩展e] 软硬酸碱规则与配合物的稳定性 作者:化学自习室 来源:未知 日期:2021-05-21 11:10:51 点击:12249 所属专题:配合物稳定性
路易斯酸碱理论是在1923年提出的,其酸碱定义是:凡是能给出电子对的分子、离子或原子团都叫做碱,凡是能接受电子对的分子、离子或原子团都叫做酸,如 以上反应中H + 、BF 3 、Ag + 接受电子对是酸,而OH - 、F - 、N 给出电子对是碱,它们的产物都是配位键形成的“...
 [探讨与扩展e] 无机含氧酸的酸性全面解读 作者:化学自习室 来源:未知 日期:2020-03-03 15:58:06 点击:10267 所属专题:含氧酸酸性
[探讨与扩展e] 无机含氧酸的酸性全面解读 作者:化学自习室 来源:未知 日期:2020-03-03 15:58:06 点击:10267 所属专题:含氧酸酸性
无机含氧酸可以的分子式为HmROn,其通式可以写成Hl-Rm-(OH)n,〔其中l,m可以为0,n≥0〕,也可写成ROm-n(OH)n,其中R称为成酸元素,无机含氧酸在水溶液中的酸强度取决于酸分子中羟基-O-H的电离程度,也可以用Pka值来衡量。酸分子羟基中的质子在电离过程中脱离氧原子,转...
 [探讨与扩展e] 大π键解读 作者:黄元 来源:未知 日期:2017-10-07 23:04:16 点击:20138 所属专题:大π键
[探讨与扩展e] 大π键解读 作者:黄元 来源:未知 日期:2017-10-07 23:04:16 点击:20138 所属专题:大π键
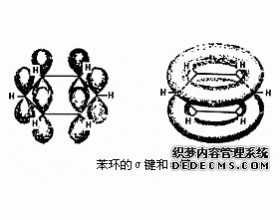
1.定义: 在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离域π键,或大π键。 2.形成大π键的条件 ①这些原子都在同一平面上;②这些原子有相互平行的p轨道;③p轨道...
 [探讨与扩展e] 物质热稳定性、溶解性原理探讨之阴阳离子半径比 作者:郑益强 来源:未知 日期:2016-04-24 18:46:24 点击:7758 所属专题:稳定性 溶解性
[探讨与扩展e] 物质热稳定性、溶解性原理探讨之阴阳离子半径比 作者:郑益强 来源:未知 日期:2016-04-24 18:46:24 点击:7758 所属专题:稳定性 溶解性
在无机化学中有这样一条规律:离子半径较大(或较小)的阳离子和离子半径较大(或较小)的阴离子形成的离子化合物热稳定性高,在水中的溶解度小;离子半径大小悬殊的阴阳离子形成的离子化合物热稳定性差,易溶于水,即大大结合稳 定,小小结合稳定,大小结合不稳定。这就是...
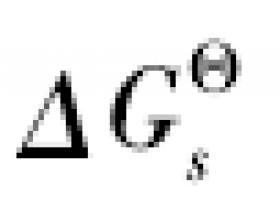 [探讨与扩展e] 离子性盐类溶解性解析 作者:童建军 来源:未知 日期:2016-03-24 22:04:06 点击:4347 所属专题:溶解性
[探讨与扩展e] 离子性盐类溶解性解析 作者:童建军 来源:未知 日期:2016-03-24 22:04:06 点击:4347 所属专题:溶解性
盐的溶解性是元素及化合物所研究的重点领域之一,了解该特性有助于正确合成路线的选择化合物的分离、提纯及检测,揭示其中的规律不仅是科学研究的需要,更是理论指导实践的必然选择, 1、离子性盐类溶解性慨况 离子性盐类主要包括碱金属和碱土金属的卤化物、硝酸盐、硫...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
无机化合物的键型和晶型、溶解度、熔沸点,甚至颜色都可用离...
一、什么是超分子化学? 在高中化学的学习中,我们接触最多的...
超分子的识别和自组装是高中结构化学中的一部分,我们可以援...
在化学体系中,配合物(Coordination Compounds)是一类由中心离子(...
共价键就是俩原子凑一对电子,八隅体是铁律,氢只能连1个原子...
d 轨道杂化是原子轨道杂化的重要类型,以中心原子价层中的 ...
一般来说,同主族元素形成的R-R键键能从上至下,键长逐渐增大...
离子极化与影响元素 离子极化理论是离子键理论的重要补充。...