
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
冠醚是一类大环多醚化合物,其分子结构呈环状,环上均匀分布有多个醚键氧原子。这类化合物与碱金属离子(如Li⁺、Na⁺、K⁺等)相互作用,形成稳定的主-客体配合物,是超分子化学中的经典研究体系。
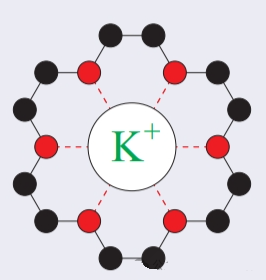
一、主要作用力:离子-偶极相互作用
冠醚与碱金属离子的结合,主要驱动力是离子-偶极静电相互作用。
作用本质:碱金属离子(M⁺)带正电荷。冠醚环上的氧原子具有孤对电子,其电负性高于碳原子,使得C–O键成为极性共价键,氧原子一端呈部分负电(δ⁻)。因此,带正电的金属离子与氧原子偶极的负端相互吸引。
结构基础:冠醚的环状骨架将多个氧原子以特定几何构型固定,形成一个预先组织的、富含电子(富电子)的配位空腔。金属离子进入该空腔后,与多个氧原子同时发生离子-偶极相互作用,产生加合效应。
二、“弱配位键”的界定
在描述这种相互作用时,需要注意概念的精确性:
专业术语:在超分子化学与配位化学中,冠醚与碱金属离子之间的键合属于非共价相互作用。其形成的主-客体复合物具有配位化合物的许多特征(如特定的化学计量比、空间结构、热力学稳定性),但结合力本质是静电作用,并未发生典型的电子共享或电子对给予形成强共价键。
教学语境中的“弱配位键”:在高中或入门级教学中,为了便于理解其“选择性结合”和“配位”的特征,可将其类比或简称为“弱配位键”。这是一种教学上的合理模型,用于区别于经典的强共价配位键(如过渡金属络合物)。但需明确,其严格物理本质是静电作用,键能较弱(通常为几十kJ/mol),且具有较高的可逆性。
三、关键特征:尺寸选择性
冠醚与不同碱金属离子的结合强度,主要取决于空腔半径与离子半径的匹配度。例如:
18-冠-6(环上有6个氧原子)的空腔半径(~1.3–1.6 Å)与K⁺离子半径(1.38 Å)匹配最佳,因此对K⁺的结合能力远强于Na⁺(0.102 Å)或Li⁺(0.76 Å)。
15-冠-5(空腔较小)则对Na⁺有较好的选择性。 这种基于尺寸的分子识别是超分子化学的核心概念之一。
四、主要应用领域
相转移催化:冠醚能与溶于水相的碱金属盐阳离子结合,形成疏水性的阳离子-冠醚复合物,使其可溶于有机相,从而显著提高阴离子在有机相中的反应活性。
离子载体:用于构建离子选择性电极的敏感膜,能高选择性识别特定离子(如K⁺),广泛应用于血液电解质分析。
金属离子分离与提取:利用其对不同离子结合能力的差异,实现金属离子的分离与富集。
实验安全提示
多数冠醚化合物具有毒性,并能透过皮肤吸收。中学阶段不进行涉及冠醚的实体实验,其相关知识以理论学习和原理探究为主。
结论
冠醚-碱金属体系清晰地展示了基于非共价相互作用的分子识别。其作用力本质为离子-偶极相互作用,在教学模型中可理解为一种“弱配位作用”。该体系是连接经典配位化学与超分子化学的重要桥梁,体现了结构匹配在分子间作用中的核心地位。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
归纳 过二硫酸根 中的过氧键(—O—O—)与过氧化氢结构式(...
电子效应通过改变电子云分布(尤其是化学键的极性、电子离域程...
1、真题呈现: (2023山东--节选)ClO2中心原子为Cl,Cl2O中心原子...
一、螯合物的定义与特点 1. 定义 螯合物是由中心金属离子(或...
一、无机阴离子配体:铜配合物的基础“搭建模块” 无机阴离子...
...