
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【导读】过渡态是反应中稍纵即逝的能量顶峰,化学键将断未断、将成未成的一种状态,中间产物是能量谷底,可短暂驻留的相对稳定的产物,化学键已重组完成。
如同登山者跨越山脊。
①过渡态≈脚踏山巅的瞬间:摇摇欲坠,无法停留,下一步必坠向任意一侧;
②中间产物≈半山腰的营地:可搭帐篷休整,积蓄力量再出发。
一、什么是过渡态(Transition State, TS)?
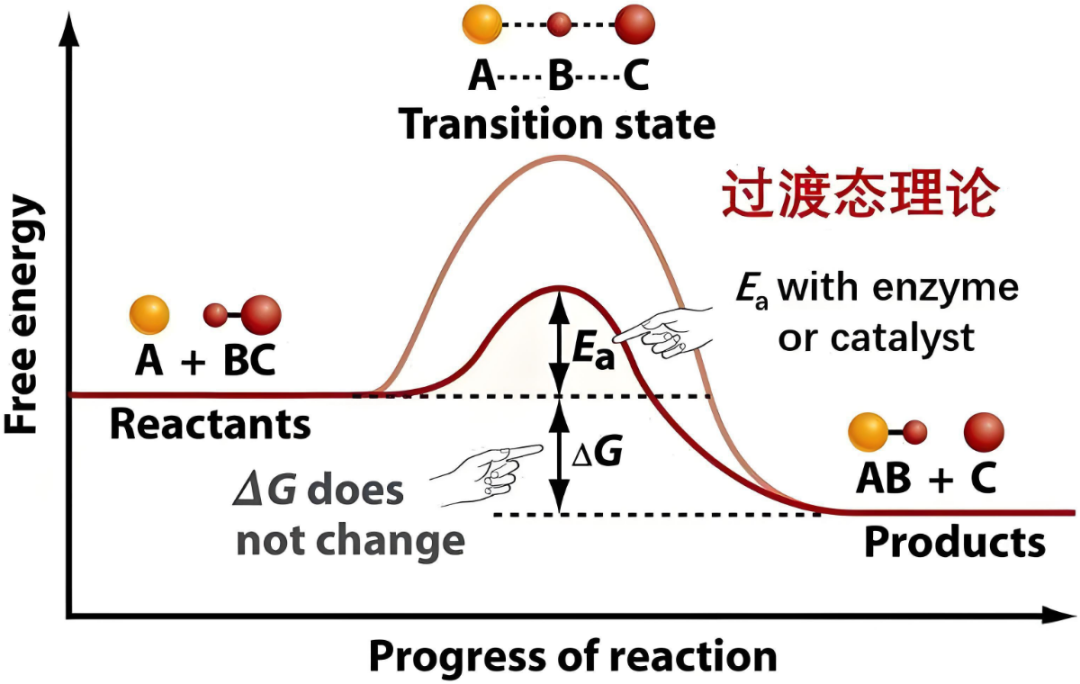
过渡态是反应物转化为产物的过程中,体系能量达到最高点时的不稳定状态,它位于描述反应进程路径坐标能量曲线的峰顶。
过渡态具有以下特点:
①能量最高点:反应物分子必须克服这个能垒才能变成产物。
②寿命极短:存在时间极短(约10⁻¹³秒),无法被分离或直接观测。
③结构特殊:是旧键即将断裂、新键即将形成的临界构型。
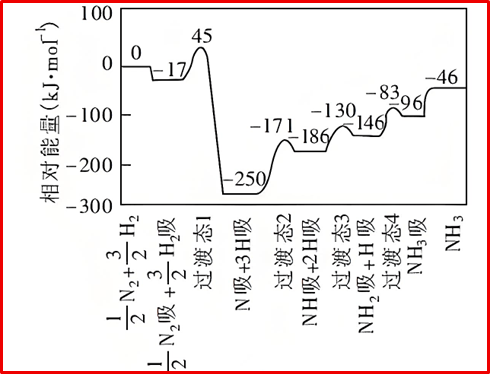
如上面的反应历程图中明确标注了“过渡态1”、“过渡态2”、“过渡态3”、“过渡态4”四个点,均位于能量曲线的峰顶。如“过渡态1”位于“N₂吸+3/2H₂吸”(反应物吸附态)和“N吸+3H吸”(第一个中间态)之间的能量最高点,约45kJ/mol。
每个过渡态都对应着反应路径上的一个关键步骤(如N≡N键断裂、N-H键形成等)需要克服的最高能垒。
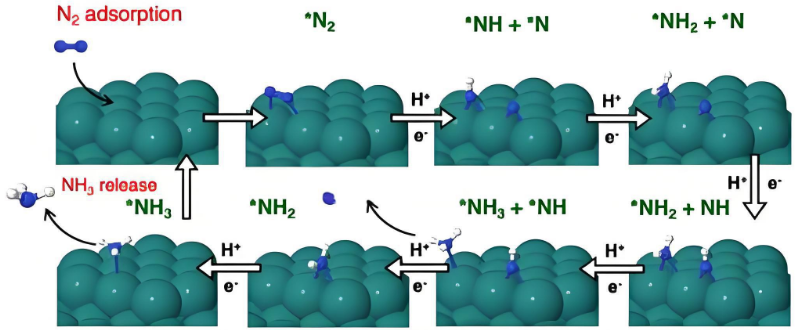
二、什么是中间产物?
中间产物是反应路径上位于两个过渡态之间的、能量相对较低且相对稳定(相对于过渡态而言)的物种,可以被认为是反应的“驿站”。
中间产物的特点:
①能量谷底:位于能量曲线的局部最低点。
②有限寿命:寿命比过渡态长得多(可能被检测到),但通常仍比最终产物短或不稳定。
③可表征性:在催化反应中,它们常对应于催化剂表面吸附的特定物种(吸附中间体)。
如上面的反应历程图中标注了多个能量局部最低点,它们就是中间态。
①中间产物“N吸+3H吸”,能量约-250kJ/mol,表示N原子吸附在催化剂表面,同时3个H原子也吸附在表面。这通常发生在N₂分子在催化剂表面解离吸附(N₂→2N*)之后,并与吸附的H原子共存。
②中间产物“NH吸+2H吸”,能量约-186kJ/mol),表示一个NH基团吸附在表面,同时还有2个H原子吸附。
③中间产物“NH₂吸+H吸”,能量约-146kJ/mol),表示一个NH₂基团吸附在表面,还有一个H原子吸附。
④中间产物“NH₃吸”,能量约-96kJ/mol,表示完整的NH₃分子吸附(化学吸附)在催化剂表面。
这些中间产物都比它们前后的过渡态能量低,也比最终气态产物的能量低,因为吸附是放热的。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
一、热化学易错易混提醒 1.放热反应不一定在常温下就能反应,...
在学习《活化能》时,有学生注意到“反应进程—势能图”与学...
【导读】过渡态是反应中稍纵即逝的能量顶峰,化学键将断未断...
多数盐(如铵盐、弱酸盐)水解为吸热反应,典型的盐类水解(如...
化学反应热力学和动力学的区别与联系如下: 一、热力学和动力...
一、概念梳理 中和热是指在稀溶液中,酸与碱发生中和反应生成...