
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
一、锡单质
(1)锡有三种同素异形体,他们之间的转化关系为灰锡(α锡),白锡(β锡)、脆锡。
锡制品是白锡的制成,但是长期处于低温会毀坏,这是β锡转变为α锡的缘故,这一现象叫做锡瘟,灰锡是粉末状,β锡在低于13.6℃转变为α锡,α锡本身就是这类反应的催化剂。
(2)锡是两性金属,与稀盐酸缓慢作用,与浓盐酸在加热条件下反应加快:
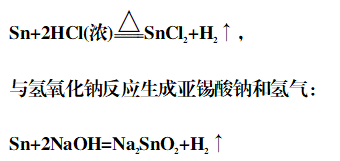

二、氧化物
二氧化锡是锡最重要的化合物,是锡石的主要成分。它不溶于水,也难溶于酸或碱的水溶液,但与NaOH或Na2CO3和S共熔,可转变为可溶性的盐:

SnO2+2NaOH=Na2SnO3(锡酸钠)+ H2O,
SnO2+2Na2CO3+4S=Na2SnS3(硫代锡酸钠)+ Na2SO4+2CO2↑
三、氢氧化物
氢氧化锡是两性氢氧化物,既可溶于酸又可溶于
Sn(OH)2+2HCl=SnCl2+2H2O,
Sn(OH)2+2NaOH=Na2SnO2+2H2O.
四、锡盐
Sn2+与Sn4+均易水解:
SnCl2+H2O=Sn(OH)Cl(白色)+HCl;
SnCl4+4H2O=Sn(OH)4↓+4HCl;
故配制SnCl2溶液要使用盐酸,抑制Sn2+水解;
Sn2+在空气中被氧气氧化:
2Sn2++O2+4H+=2Sn4++2H2O,
要加入单质Sn,防止Sn2+被氧化,这一点与Fe2+相似。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
锰(Mn)是元素周期表第四周期第 ⅦB 族的过渡金属元素,原子...
镁(Mg,原子序数 12,第 ⅡA 族碱土金属元素)是典型的活泼金...
在第ⅡA族(碱土金属)元素家族中,铍(Be)以其极致的轻金属特性、...
1.皓矾: ZnSO 4 ·7H 2 O 2.钡餐,重晶石: BaSO 4 3.绿矾,皂矾,青矾...
少量、适量、足量和过量,这几个词是化学实验和计算中的核心...
一、基础概念:从 “温度强度” 看五者的核心差异 首先需明确...