
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
第一节:烷烃的物理性质
烷烃都不溶于水而溶于有机溶剂和乙醇、乙醚等。密度小于 lg/cm3。它们是无色的气体、液体或固体。沸点和熔点随相对分子 质量的增加而升高,10个碳以上的烷烃沸点升高很有规则,每增 加一个“CH2”对沸点来说约升高19°C,但低级的烷烃则每增加 一个“CH2”对沸点影响很大,差值在20~48°C之间。其他的物理 常数,如熔点也随相对分子质量的增加而逐渐升高。但熔点差别随同系列升高而越来越小,见下表。
表烷烃的物理性质
烷烃 | 分子式 | 沸点,°c | 沸点差值,°c | 熔点,°c | 熔点差值,°c |
甲烷 | CH4 | -164 | 71 | -184 | |
乙烷 | C2H6 | -93.0 | 48 | _171.4 | |
丙烷 | c3h8 | -45.0 | 44.5 | -190 | |
丁烷 | c4h10 | -0.5 | 36.5 | -138.3 | |
戊烷 | C5H12 | 36 | 32.7 | -129.7 | |
己烷 | CfiHi4 | 68.7 | 29.7 | -95.5 | |
庚烷 | c7h16 | 98.4 | 27.4 | -90.8 | |
辛烷 | c8h18 | 125.8 | 24.9 | -56.8 | |
壬烷 | C9H20 | 150.7 | 223 | -53.8 | 21.8 |
癸烷 | C10H22 | 173 | 22 | -32 | 5.5 |
十一烷 | C11H24 | 195 | 20 | -26.5 | 14.5 |
十二烷 | C12H26 | 215 | 19 | -12 | 5,8 |
十三烷 | C13H28 | 234 | 18 | -6.2 | 1L2 |
十四烷 | C14H30 | 252 | 18 | 5.0 | 5.0 |
十五烷 | C15H32 | 270 | 17 | 10.0 | 8.0 |
物态也随相对分子质量的增加而改变,C1〜C4的烷烃是气态, C5〜C16的烷烃是液态,C17以上的烷烃是固态。
含偶数碳原子的烷烃比邻近的含奇数碳原子的烷烃熔点高 些,随着相对分子质量的增加,差别逐渐减小。这种现象也存在 于其他的同系列中。原因是熔点与晶体中的碳链排列有关。由于 烷烃分子中的碳原子的四个价键都是正四面体构型,所以含偶数 碳原子的烷烃的原子排列更规则些,它在晶体中的排列也就更紧 密些,因此熔点相应的高些。
同级烷烃的各个异构体,它们的性质是有区别的,一般说来 直链烷烃沸点高些,支链越多则沸点低。例如:正戊烷沸点36°C, 异戊烷沸点27.9°C,新戊烧沸点9.5°C。
C6H14异构体的沸点(°C)如下:
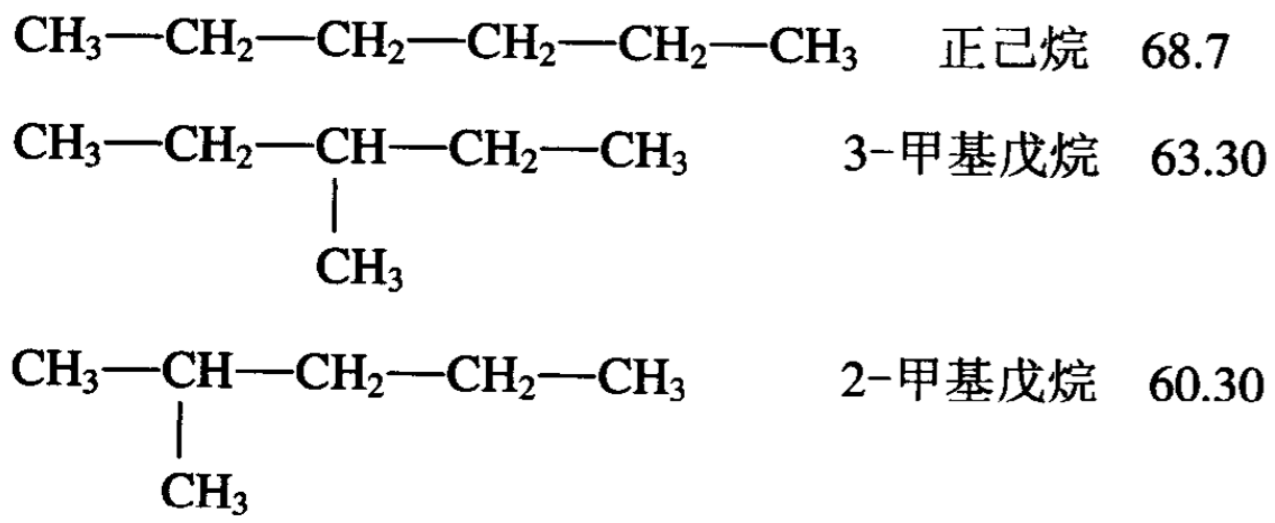
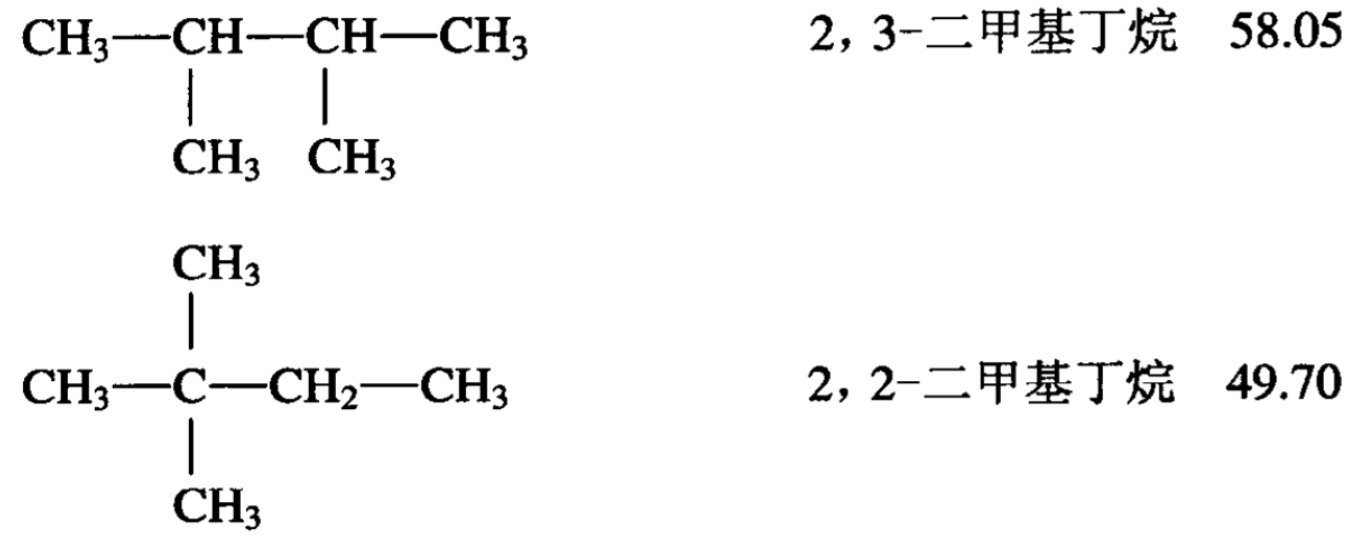
第二节:烷烃的化学性质
烷烃加合能放氢
脱氢环化成芳烃
加氣光照能取代
受热裂解成烯烃
空气能把烷氧化
加氯光照变卤烃
—、烷烃加合能放氢
烷烃在“过酸性”催化剂的催化下,可以由一种烷烃加合成 为另一种烷烃,并放氢。以甲烷为例,其连续进行的反应式为:

甲烷转化成正甲烷离子,正甲烷离子继续转化为更为稳定的 正碳离子,例如叔丁基阳离子。这种现象可写为如下的总反应式:
![]()
二、脱氢环化成芳烃
烷烃脱氢可环化成芳烃(C6-脱氢环化)。通常脱氢环化指从 烷烃形成芳烃,但同时存在着另一反应,如烷烃转化成环戊烷, 这也是脱氢环化过程。为了避免混淆,把这两种过程分别称之为 C6-脱氢环化和C5-脱氢环化。用含10%左右的氧化铬催化剂,在500°C左右处理C6~C9的烷烃,可得到收率很高的相应芳烃。
三、加氯光照能取代
烷烃和氯在室温和黑暗中不起反应,但在强光的照射下则发 生猛烈的反应,甚至引起爆炸,生成碳和氯化氢:
![]()
但在漫射光、加热或催化剂作用下,甲烷分子中的氢原子可逐步地被氯取代,得出如下四种氯代甲烷混合物,它们往往不易分离。 下式是表示连续氯化的部分产物:
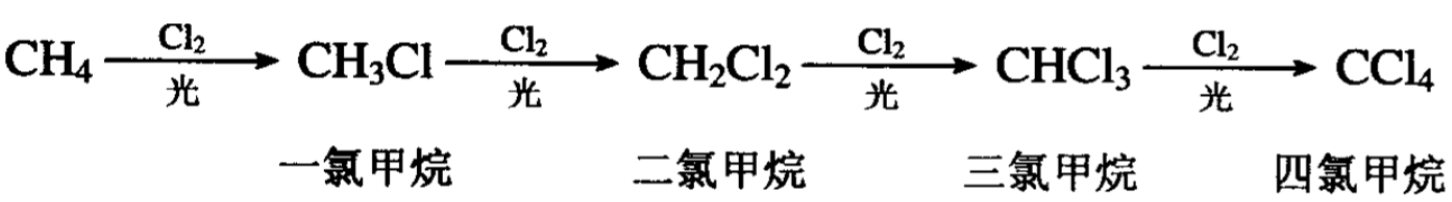
高级的烷烃氯化时,比较容易控制,可以得到一氯代烷,产 品中有几种同分异构体,这类产品一般不加分离而作溶剂用。
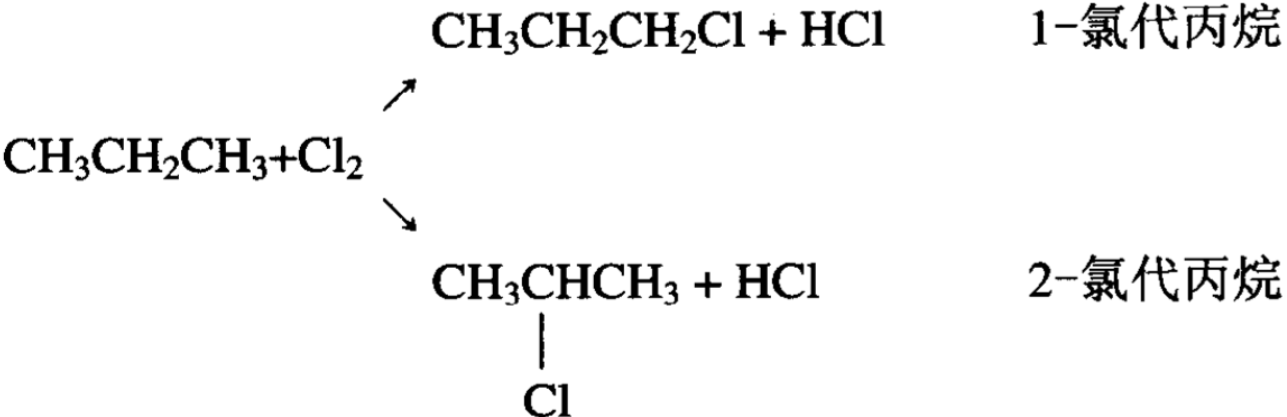
氯代反应实际上是氯取代了烷烃分子上的氢原子。我们把烃 中的氢被氯原子或其他原子团替代的反应称为取代反应。发生取 代反应后的产物是氯化烷,分子中的碳仍保持四价,碳和氯也是 以共价键相连,只是氯代替了一个氢的位置。举例来说,丙烷的 一氯代反应,可以发生在“第一”碳上,也可以发生在“第二”碳上,因此产物是两个,一是1-氯代丙烷,另一个是2-氯代丙烷。 高级烷烃的氯代产物中,异构体就更多了。
四、受热裂解成烯烃
烷烃受热时键断裂而变为较小的分子叫做裂解(或裂化)。随 着烷烃相对分子质量的增大和碳链增长,C—C键间断裂的机会也 越大,因此对热的稳定性越差。由于裂解可在C一H键和C一C 键间发生,所以反应后的产物很复杂。
例如:
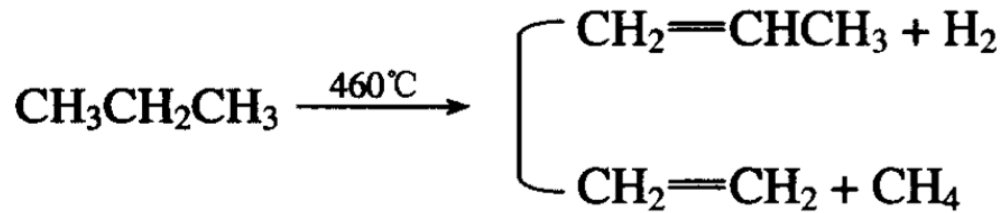
五、空气能把烷氧化
烷烃分子大多数是以共价键组成的,它们分子内的原子间没 有明显的电子转移,很少有化合价的变化。在有机化学反应中一般把与氧化合或失去氢的反应叫氧化,把与氧化合失去氧的反应 叫做还原。例如纯净的烷烃在空气中完全燃烧都生成二氧化碳和 水,如果控制氧化条件,使反应缓慢进行,则可使烷烃发生部分 氧化,得到其他不同的含氧化合物。例如,戊烷在催化剂的作用 下,能被空气氧化生成各种羧酸:
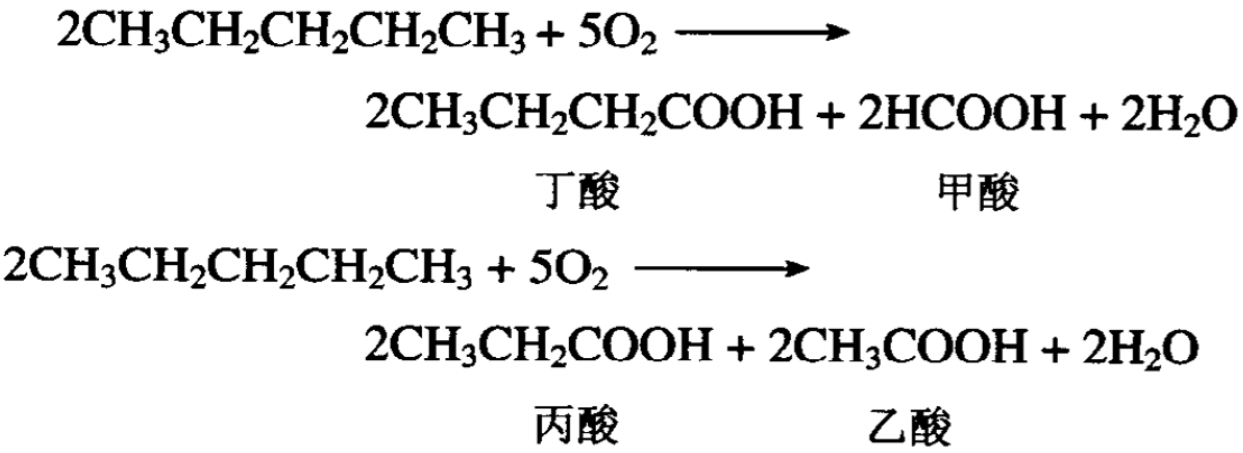
在适当的条件下将低级烷烃进行部分氧化,也可以得到甲酸、 甲醇、乙醛、乙酸、丙酮等含氧的有机化合物,它们都是重要的 化工原料。烷烃在氧化反应中不使1^04酸性溶液褪色。
烷烃在普通温度下,与氧气不起作用。温度若达着火点以上 则在空气中燃烧,生成二氧化碳和水,并放出大量的热量。
挥发性烷烃的蒸气和空气的混合物遇到火花会发生 爆炸。经测定发生爆炸的气体混合物的浓度有一个上限和下限, 浓度低于或高于这个范围不发生爆炸。例如甲烷的爆炸极限是 5.3%~14.0% (体积分数),其他烷烃的爆炸极限比甲烷的要小些而 且窄些,如己烷的爆炸极限为1.9%~4.7% (体积分数)。
六、加氯光照变卤烃
烷烃的取代反应是游离基历程,以甲烷的卤代反应来说明这 个历程。
氯分子的活化能比较低,C1 一C1键受光照就断裂成两个氯 原子:
![]() ①
①
游离的氣原子因有一个未成对的孤电子而化学反应活泼性提 高,一旦游离基产生,反应就会顺利进行。游离的氯原子先和甲 烷分子中的一个氢原子结合生成氯化氢,并产生一个游离甲基:
![]() ②
②
游离甲基如有一个未成对的孤电子,它则和氯分子作用生成 一个氯甲烷和氯原子:
![]() ③
③
游离的氯原子又可以和另一个甲烷分子作用,重复②③的反 应,亦可以与氯甲烷分子作用:
![]() ④
④
![]() ⑤
⑤
只要有游离基存在,这种反应就可以继续下去,最后甲烷分 子中的氢全部被氯取代,生成四氯化碳。这种反应称为链锁反应。
如果游离基相互结合,不再产生游离基了,反应即刻停止:
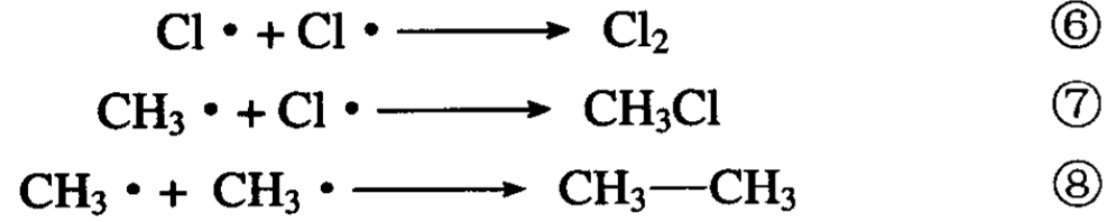
反应①称为链引发阶段,这个阶段反应速度慢,时间长;反 应②③④⑤称为链传播阶段;这个阶段反应速度极快,反应⑥⑦ ⑧称为链终止阶段。所有的游离基反应都经历这三个阶段。链终 止的方式,不仅是游离基的相互结合,引入氧(或其他杂质)使 之与游离基结合,也可以使链终止,这样的物质称为阻止剂。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
在高考中考查: 近几年新高考中最早出现非苯环芳香烃相关考查...
立体结构差异 椅式环己烷结构中,碳原子构成的环近似于一个三...
电子效应,在大多数反应中,由于取代基(与氢原子相比)倾向...
一、芳香烃的定义 具有芳香性的烃称为芳香烃,一般是指分子中...
一、一些特殊反应 1、醇解反应: 卤代烃与醇钠的醇溶液反应,...
烷的取代反应主要是自由基反应。比如: Cl 2 →2Cl· CH 4 →CH 3...