
|
学习小专题 |
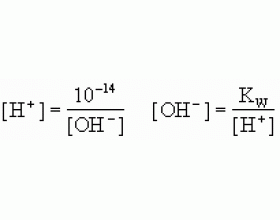 有关pH的计算公式有哪些
日期:2020-02-28 15:09:32
点击:26978
好评:3
有关pH的计算公式有哪些
日期:2020-02-28 15:09:32
点击:26978
好评:3
(1)pH= -lg[H + ];[H + ]=10 -pH (2)pOH= -lg[OH - ];[OH - ]=10 -pOH (3)K W =[H + ]·[OH - ]=1×10 -14 (4)pH+pOH=14 (5)pH=-lg[H + ]= -lg(m×10 -n )=n-lgm (注意:不指明温度时,温度为常温25℃) 下表是常用到的几个lg值:...
 用电离平衡常数求解强碱弱酸盐溶液的pH
日期:2017-06-26 15:23:49
点击:4703
好评:0
用电离平衡常数求解强碱弱酸盐溶液的pH
日期:2017-06-26 15:23:49
点击:4703
好评:0
...
 当无限稀释强酸、强碱溶液时pH是怎么变化的?
日期:2017-04-17 15:04:44
点击:1977
好评:0
当无限稀释强酸、强碱溶液时pH是怎么变化的?
日期:2017-04-17 15:04:44
点击:1977
好评:0
当无限稀释强酸或强碱溶液时, c (H + )或 c (OH - )变化得很小,此时就不能忽略水的电离平衡的影响,即应将水电离出得H + 和OH - 得浓度计算在内。由于水电离出 c (H + )和 c (OH - )为1×10 -7 mol/L,则计算出 c (H + )或 c (OH - )值必小于或接近于1×10 -7 m...
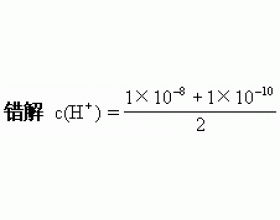 pH拾零
日期:2016-02-02 19:49:52
点击:9049
好评:0
pH拾零
日期:2016-02-02 19:49:52
点击:9049
好评:0
一、pH与酸碱性 1.溶液酸碱性的强弱由pH决定,与温度、溶质无关。如:pH均为2的硫酸溶液与醋酸溶液酸度相同。 2.pH等于7的溶液不一定呈中性。(“pH=7为中性”习惯上指常温时) 二、 pH的计算 1.计算时先确定溶液的酸碱性,计算顺序为:酸性→c(H + )→pH;碱性→c(O...
 常见pH计算的关键
日期:2016-02-02 19:49:28
点击:7179
好评:0
常见pH计算的关键
日期:2016-02-02 19:49:28
点击:7179
好评:0
一、强酸稀释 关键:必须抓H + ;当酸电离出的H + 很少时,H 2 O的电离不可忽略。 例 1. 将pH=3的盐酸溶液稀释100倍、10 5 倍后其pH各变为多少? 解析: 原溶液中[H+]=1×10 -3 mol/L。 稀释:100倍后,抓H+可知[H + ]=1×10 -3 ÷100=1×10 -5 mol/L,能得出正确结果p...
 为什么碱溶液混合求pH必须要先求C(OH-)?
日期:2015-02-12 19:37:14
点击:2482
好评:1
为什么碱溶液混合求pH必须要先求C(OH-)?
日期:2015-02-12 19:37:14
点击:2482
好评:1
我们知道任何水溶液中H + 、OH - 都是共存的,而 c (H + ) c (OH - )= K w , 在常温 时 K w =1×10 -14 , 在酸溶液 c (H + )> c ( OH - ),例如:在pH=5的盐酸溶液 c (H + )=10 -5 mol/L, c ( OH - )=10 -9 mol/L,显然前者浓度的远远大于后者的浓度。...
 酸性及碱性的缓冲溶液的PH计算
日期:2015-01-28 21:04:23
点击:7485
好评:0
酸性及碱性的缓冲溶液的PH计算
日期:2015-01-28 21:04:23
点击:7485
好评:0
1.已知25℃时,CH 3 COOH的电离常数为1.8×10 -5 。 则25℃时,0.1mol/L 的CH 3 COOH和0.1mol/L 的CH 3 COONa按体积比1:1混合后,所得混合液的pH是多少?请计算说明。 2.已知25℃时,NH 3 ·H 2 O的电离常数为1.8×10 -5 。 则25℃时,0.1mol/L 的氨水和0.1mol/L 的NH 4 C...
 碳酸钠溶液和碳酸氢钠溶液定量分析
日期:2015-01-28 15:40:41
点击:3906
好评:0
碳酸钠溶液和碳酸氢钠溶液定量分析
日期:2015-01-28 15:40:41
点击:3906
好评:0
已知:二元弱酸碳酸的解离常数: K a 1 =4.2×10 -7 ; K a 2 =5.6×10 -11 。 (一)碳酸发生两步解离: H 2 CO 3 HC O 3 - +H + ; HC O 3 - H + + C O 3 2 - ∵ K a 1 ≥100 K a 2 ,说明H 2 CO 3 二级解离可忽略。 ∴H 2 CO 3 以一级解离为主。 ...
 酸,碱加水稀释后PH的计算
日期:2014-05-15 09:31:06
点击:12700
好评:0
酸,碱加水稀释后PH的计算
日期:2014-05-15 09:31:06
点击:12700
好评:0
一、强酸强碱稀释后pH的计算 例1:以下是某些学生的答卷: pH=3的盐酸稀释10倍,pH=4; pH=3的盐酸稀释10000倍,pH=7; pH=3的盐酸稀释100000倍,pH=8 解析:其解题思路是稀释前后, n (H + )不变,若稀释10 n 倍, c (H + )减至原来的1/10 n ,故pH增大n个单位。显然后两...
 溶液pH计算的基本方法
日期:2014-01-16 17:38:06
点击:492
好评:0
溶液pH计算的基本方法
日期:2014-01-16 17:38:06
点击:492
好评:0
溶液pH计算的基本方法...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。