
|
学习小专题 |
 pH=5的稀盐酸加水冲稀1000倍,稀释后溶液的pH=?请通过计算说明
日期:2024-08-20 16:09:24
点击:516
好评:0
pH=5的稀盐酸加水冲稀1000倍,稀释后溶液的pH=?请通过计算说明
日期:2024-08-20 16:09:24
点击:516
好评:0
问题呈现:pH=5的稀盐酸加水冲稀1000倍,稀释后溶液的pH=?请通过计算说明。 错解:由pH=5,知 c (H + )=10 -5 mol/L, 加水冲稀1000倍后, 由盐酸产生的 c (H + )=10 -8 mol/L, 由水产生的 c (H + )=10 -7 mol/L, 所以溶液总的 c (H + )=10 -8 mol/L + 10 -7 m...
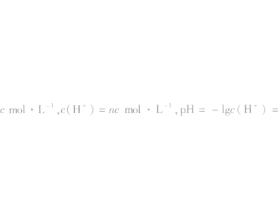 溶液pH的计算方法
日期:2023-12-18 09:32:33
点击:1376
好评:0
溶液pH的计算方法
日期:2023-12-18 09:32:33
点击:1376
好评:0
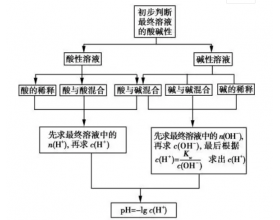
溶液pH计算的整体思路是:根据pH的定义pH=-lg c (H + ),溶液pH计算的核心是确定溶液中的 c (H + )相对大...
 pH值计算的思维路径
日期:2022-12-19 17:46:23
点击:544
好评:0
pH值计算的思维路径
日期:2022-12-19 17:46:23
点击:544
好评:0
一、原理:影响水的电离平衡因素 H 2 O H + +OH - 1.25 ℃, → c (H + ) H2O = c (OH - ) H2O =1×10 -7 → K w =1×10 -14 2.25 ℃,加CH 3 COOH、H + →平衡向左移动→ c (H + ) H2O = c (OH - ) H2O <1×10 -7 3.25 ℃,加NH 3 ·H 2 O、OH - →平衡向...
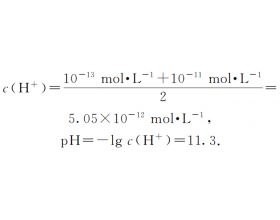 关于pH计算与测定的问题讨论
日期:2021-10-29 15:10:50
点击:1077
好评:0
关于pH计算与测定的问题讨论
日期:2021-10-29 15:10:50
点击:1077
好评:0
问题1、不同pH溶液混合时,计算混合液的pH何时以H + 为准,何时以OH - 为准? 请看如下实例:把pH=13和pH=11的烧碱溶液等体积混合,求混合溶液的pH。 解法1:混合溶液的 解法2: 两溶液的 c (OH - )分别为10 -1 mol·L -1 和10 -3 mol·L -1 . 混合溶液的 哪一个结...
 酸、碱和盐稀释和混合时的pH变化
日期:2021-08-22 12:20:53
点击:3154
好评:0
酸、碱和盐稀释和混合时的pH变化
日期:2021-08-22 12:20:53
点击:3154
好评:0
酸、碱和绝大多数盐都是电解质,除强酸强碱盐由于本身不含水解离子,不会影响水的电离平衡,其盐的水溶液稀释前后也不改变,室温条件下均为7。因此本文讨论范围限定在酸、碱和可水解的盐。 1、酸稀释时溶液的pH变化 。 pH概念为溶液中氢离子浓度的负对数之值。应当分为强酸...
 溶液的pH计算专题专练
日期:2020-10-09 16:48:24
点击:296
好评:0
溶液的pH计算专题专练
日期:2020-10-09 16:48:24
点击:296
好评:0
溶液的pH计算专题专练...
 pH的计算方法与规律
日期:2020-02-16 11:14:48
点击:13412
好评:0
pH的计算方法与规律
日期:2020-02-16 11:14:48
点击:13412
好评:0
一.溶液pH的计算 1、基本思路 2、类型方法 ①单一溶液 溶液类型 相关计算 强酸(HnA) 设HnA的浓度为cmol/L,则c(H + )=ncmol/L,pH=lgc(H + )=lgnc 强碱[B(OH)n] 设B(OH)n的浓度为cmol/L,则c(OH)=ncmol/L,c(H + )=mol/L,pH=lgc(H + )=14+lgnc ②混合溶液 二.酸...
 微课视频:强酸和强碱溶液混合时pH计算
日期:2020-02-01 17:18:50
点击:312
好评:0
微课视频:强酸和强碱溶液混合时pH计算
日期:2020-02-01 17:18:50
点击:312
好评:0
微课视频:强酸和强碱溶液混合时pH计算...
 乐乐课堂:pH的计算类型和解题规律
日期:2020-01-27 13:59:19
点击:752
好评:0
乐乐课堂:pH的计算类型和解题规律
日期:2020-01-27 13:59:19
点击:752
好评:0
第1集:pH的计算类型和解题规律1 第2集:pH的计算类型和解题规律2 第3集:pH的计算类型和解题规律3 第4集:pH的计算类型和解题规律4 第5集:pH的计算类型和解题规律5 第6集:pH的计算类型和解题规律6 第7集:pH的计算类型和解题规律7 第8集:pH的计算的例题分析...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。