
|
学习小专题 |
 通俗讲义:醋酸是张银行卡
日期:2020-03-05 10:56:41
点击:1856
好评:2
通俗讲义:醋酸是张银行卡
日期:2020-03-05 10:56:41
点击:1856
好评:2
两瓶体积相同的溶液,一瓶醋酸,一瓶盐酸,pH同为2.5,即[H + ]同为约0.003mol/L。盐酸是强电解质,完全电离,[H + ]是这个数字,[HCl]也是这个数字。 醋酸是弱电解质,少部分电离,聚多离少。 CH 3 COOH≒ CH 3 COO - +H + 与这个可逆电离相应的平衡叫作电离平衡。因...
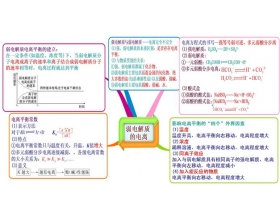 弱电解质的电离平衡之思维导图
日期:2018-07-19 15:59:58
点击:5837
好评:1
弱电解质的电离平衡之思维导图
日期:2018-07-19 15:59:58
点击:5837
好评:1
...
 电离平衡计算中的分析浓度与平衡浓度
日期:2017-03-02 10:04:10
点击:2103
好评:0
电离平衡计算中的分析浓度与平衡浓度
日期:2017-03-02 10:04:10
点击:2103
好评:0
...
 氨水稀释时的电离度与OH-离子浓度情况分析
日期:2016-02-02 21:37:29
点击:5499
好评:0
氨水稀释时的电离度与OH-离子浓度情况分析
日期:2016-02-02 21:37:29
点击:5499
好评:0
氨水是氨气的水溶液,在氨水中存在下列平衡: NH 3 +H 2 O NH 3 · H 2 O NH 4 + +OH - 。在饱和氨水中仍有一些 NH 3 · H 2 O 发生电离,因此,其电高度和 OH - 离子浓度都不能认为是从零开始。 浓氨水稀释,开始时电离度增大, [OH - ] 也增大,但稀释到一定程度后,若再...
 稀释有利于水解,亦有利于电离
日期:2016-02-02 20:11:42
点击:11726
好评:0
稀释有利于水解,亦有利于电离
日期:2016-02-02 20:11:42
点击:11726
好评:0
为什么 弱电解质溶液加水冲稀 电离平衡右移? 1.在其他条件不变的情况下,向一定浓度的弱电解质溶液中加水,由于水分子数增多,使得弱电解质电离的离子之间的距离增大,离子间相互碰撞结合成分子的机会减小,单位时间内离子间的有效碰撞次数减少。另外,弱电解质分子由于...
 为什么计算只考虑氢氧化铁的溶解平衡,不考虑电离平衡?
日期:2015-01-27 15:21:56
点击:2711
好评:0
为什么计算只考虑氢氧化铁的溶解平衡,不考虑电离平衡?
日期:2015-01-27 15:21:56
点击:2711
好评:0
氢氧化铁的溶液一般只考虑沉淀溶解平衡,而不去考虑弱电解质的电离平衡了,为啥?比如计算三价铁的量,直接用Ksp,而不管电离常数了。 溶解的氢氧化铁是完全电离的。氢氧化铁不是弱的吗?溶解的怎么是全部电离的?完全电离为什么还是弱电解质?碳酸钙硫酸钡不都算强电解质么...
 浅析几个与电离平衡相关的问题集
日期:2013-11-14 09:44:07
点击:3642
好评:0
浅析几个与电离平衡相关的问题集
日期:2013-11-14 09:44:07
点击:3642
好评:0
1 、弱电解质电离平衡体系中加水及加入相应弱电解质平衡移动方向及电离程度变化是否一致? 在弱电解质溶液中加水或加入相应弱电解质均可使电离平衡正向移动,但电离程度变化两者恰好相反,加水电离程度增大,加入相应弱电解质则电离程度减...
 影响电离度的因素
日期:2012-05-16 09:19:41
点击:12173
好评:0
影响电离度的因素
日期:2012-05-16 09:19:41
点击:12173
好评:0
①电解质的结构 具有离子键或强极性的分子在水溶液中的电离度均很大,几乎是100%。弱极性或非极性分子在水中呈微弱电离甚至不电离。电解质中键的极性越大,其电离度也越大。离子化合物的电离度取决于离子电荷及离子半径。离子电荷越高,半径越小,则其电离度越...
 关于“弱电解质溶液越稀,电离程度越大”的几种解释方法
日期:2007-05-14 14:32:18
点击:11797
好评:0
关于“弱电解质溶液越稀,电离程度越大”的几种解释方法
日期:2007-05-14 14:32:18
点击:11797
好评:0
1 .用有效碰撞理论解释 在其他条件不变的情况下,向一定浓度的弱电解质溶液中加水,由于水分子数增多,使得弱电解质电离的离子之间的距离增大,离子间相互碰撞结合成分子的机会减小,单位时间内离子间的有效碰撞次数减少。另外,弱电解质分子由于受到极性分子的作用,...
 弱酸碱稀释时的电离度与离子浓度
日期:2006-10-15 08:01:52
点击:6580
好评:2
弱酸碱稀释时的电离度与离子浓度
日期:2006-10-15 08:01:52
点击:6580
好评:2
1.一元弱酸稀释时的电离度与H+离子浓度 以醋酸为例加以说明。 无水冰醋酸基本不电离,其电离度可视为零,冰醋酸中也没有离子,只有CH3COOH分子。 当对冰醋酸加水稀释时,随着水量的增加,醋酸的电离度增大,[H+]也增大,所含H+物质的量也增大。但当加水到一定量时,即...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。