
|
学习小专题 |
 化学平衡移动前后气体体积分数变化的讨论
日期:2023-10-07 16:12:27
点击:6824
好评:0
化学平衡移动前后气体体积分数变化的讨论
日期:2023-10-07 16:12:27
点击:6824
好评:0
在一个恒温恒容的密闭容器里,充入2mol SO 2 和1mol O 2 ,发生如下反应并建立化学平衡: 2SO 2 (g) + O 2 (g)2SO 3 (g), 若向该容器中再充入一定量SO 3 气体,当达到新平衡时,下列相关说法错误的是( ) (A)正、逆反应速率均比原平衡大 (B)SO 2 的体积分数比原平衡大 ...
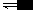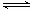 加入惰性气体对化学平衡有影响吗?
日期:2022-08-12 15:32:00
点击:36265
好评:0
加入惰性气体对化学平衡有影响吗?
日期:2022-08-12 15:32:00
点击:36265
好评:0
首先应当指出:这里的惰性气体泛指不参与某反应的气体。除了通常所说的氦、氖、氩、 氪、氙等惰性气体之外,还要視具体情况而决定。例如:在烷烃的裂化过程中充入水蒸气,合成氨反应中充入甲烷,二氧化硫的催化氧化中充入氮气等都看作惰性气体。 在气体反应达到平衡后...
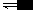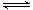 关于恒温、恒压条件下化学平衡移动的探讨
日期:2016-05-16 21:20:44
点击:8130
好评:0
关于恒温、恒压条件下化学平衡移动的探讨
日期:2016-05-16 21:20:44
点击:8130
好评:0
化学平衡理论是中学化学的重要理论之一,也是 教学的重点和难点。恒温、恒压是化学实验和化工生 产中常见的条件,该条件下平衡移动的正确判断对培养和提升学生的辩证观点和化学素养都有重要作用。 1、问题的提出 以 aA(g)+bB(g) dD(g)+eE(g)为例(本文的 反应均指该反应),...
 恒压体系下,通入反应物,化学平衡一定正向移动吗?
日期:2016-05-16 12:46:31
点击:1925
好评:0
恒压体系下,通入反应物,化学平衡一定正向移动吗?
日期:2016-05-16 12:46:31
点击:1925
好评:0
...
 绝热体系中化学平衡三类问题解析
日期:2016-05-16 10:26:45
点击:9845
好评:0
绝热体系中化学平衡三类问题解析
日期:2016-05-16 10:26:45
点击:9845
好评:0
绝热体系就是体系与环境之间没有热量传递对于一个化学反应,当平衡还未建立或者平衡发生移动的时候,反应总要放出或吸收热量,温度会随之升高或降低,从而对反应本身或对其他共存的反应带来影响。 近几年高考中,频繁出现绝热体系中的化学平衡问题,成为一大难点,常见...
 化学平衡移动方向判断的误区
日期:2016-05-12 21:19:35
点击:17482
好评:1
化学平衡移动方向判断的误区
日期:2016-05-12 21:19:35
点击:17482
好评:1
化学平衡是现行高中化学中的一个重要的化学反应原理,由于教材对化学平衡移动方向原理描述的缺失与混乱,不同的教师对化学平衡移动原理理解的不同,对化学平衡移动方向判断选择的标准不同,会导致同一个试题得出相反的结论与解释。在一次市统测的命题过程中,教师对“H ...
 氯化钾不影响平衡吗?
日期:2016-04-25 10:47:47
点击:1591
好评:0
氯化钾不影响平衡吗?
日期:2016-04-25 10:47:47
点击:1591
好评:0
问题:向平衡体系FeCl 3 + 3KSCN Fe(SCN) 3 + 3KCl中加人KCl固体,究竟能否影响该化学平衡呢? 对此问题的一般的解答是从理论上进行推导 的。根据勒夏特列原理,改变体系中物质浓度能 影响化学平衡,其前提条件是改变参与反应的物质的浓度。由于该可逆反应是离子反应,...
 怎样理解气体的体积分数与平衡移动关系
日期:2016-02-01 14:33:00
点击:4276
好评:0
怎样理解气体的体积分数与平衡移动关系
日期:2016-02-01 14:33:00
点击:4276
好评:0
...
 “化学平衡移动”的疑难问题集解析
日期:2015-12-23 11:27:07
点击:827
好评:0
“化学平衡移动”的疑难问题集解析
日期:2015-12-23 11:27:07
点击:827
好评:0
...
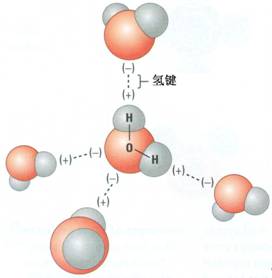 化学平衡移动时,v正与v逆的变化情况
日期:2006-12-29 10:00:42
点击:25032
好评:0
化学平衡移动时,v正与v逆的变化情况
日期:2006-12-29 10:00:42
点击:25032
好评:0
以 mA( 气 )+nB( 气 ) pC( 气 )+ qD( 气 )+ Q 为例说明。原平衡时的反应速率为 v 正 、 v 逆 ,外界条件改变后的正、逆反应速率为 v ' 正 、 v ' 逆 。 (1) 增大物质的浓度:增大反应物浓度时 v 正 、 v 逆 都增大,但 v 正 突然增大, v 逆 随后逐渐增大,且 v 正...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。