
|
学习小专题 |
 互促水解反应完全进行的条件及其推论
日期:2024-11-12 10:40:22
点击:11108
好评:0
互促水解反应完全进行的条件及其推论
日期:2024-11-12 10:40:22
点击:11108
好评:0
弱酸根离子与弱碱阳离子在水溶液中互相促进水解,水解程度增大。有些互促水解反应不能完全进行,有些互促水解反应能完全进行(俗称双水解反应)。那么,哪些弱酸根离子与弱碱阳离子在水溶液中互相促进水解反应能完全进行呢?由于中学化学教学中往往仅列出能发生双水解...
 为什么氯化铜溶液跟碳酸钠溶液反应的产物是氢氧化铜,而不是碳酸
日期:2017-04-15 15:10:13
点击:11222
好评:0
为什么氯化铜溶液跟碳酸钠溶液反应的产物是氢氧化铜,而不是碳酸
日期:2017-04-15 15:10:13
点击:11222
好评:0
氯化铜溶液跟碳酸钠溶液进行反应时,实验的结果是除有蓝色沉淀产生外,还有二氧化碳气体产生。这是由于氯化铜溶液跟碳酸钠溶液混和,水解反应很完全的缘故。 Cu 2+ +C O 3 2 - +H 2 O=Cu(OH) 2 ↓+CO 2 ↑ 为什么Cu 2+ 跟C O 3 2 - 不结合成碳酸铜呢?比较常温...
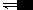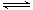 如何定量判断盐能否发生彻底水解?
日期:2016-04-22 22:57:38
点击:3113
好评:0
如何定量判断盐能否发生彻底水解?
日期:2016-04-22 22:57:38
点击:3113
好评:0
对于CH 3 COONH 4 、NH 4 F等弱酸弱碱盐,它们的阴、阳离子都会发生水解导致水解相互促进。一般情况下,如CH 3 COONa、NH 4 F的水解程度虽然较大,但其溶液中主要还是以盐的形式存在,水解未进行彻底。 对于Al 2 S 3 、(NH 4 ) 2 S等弱酸弱碱盐,它们的阴、阳离子都会发生水...
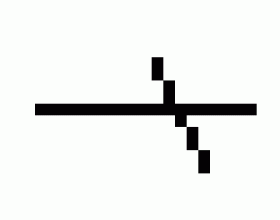 盐和盐的反应规律
日期:2016-02-02 20:18:35
点击:12155
好评:0
盐和盐的反应规律
日期:2016-02-02 20:18:35
点击:12155
好评:0
由于盐的水解及某些盐具有氧化性,还原性,当盐和盐反应时,有下列四种情况: (1)氧化还原反应 当盐和盐反应时,如果有一种盐是氧化剂,另一种盐是还原剂,则发生的是氧化还原反应,例如: 2FeCl 3 +Na 2 S=2FeCl 2 +2NaCl+S↓ 2FeCl 3 +2KI=2FeCl 2 +2KCl+I 2 (2)...
 由于双水解在溶液中不能大量共存的离子组总结
日期:2016-02-02 20:17:51
点击:7723
好评:0
由于双水解在溶液中不能大量共存的离子组总结
日期:2016-02-02 20:17:51
点击:7723
好评:0
弱酸根离子与弱碱阳离子在水溶液中 不能 大量 共存 的情况常见的有:...
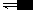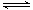 某些水解为什么能“进行到底”
日期:2015-06-09 22:43:30
点击:3132
好评:0
某些水解为什么能“进行到底”
日期:2015-06-09 22:43:30
点击:3132
好评:0
一.水解平衡常数小,无法进行到底 例1.关于醋酸铵溶液――不能进行到底 Ac - + H 2 O = HAc + OH - NH 4 + + H 2 O = NH 3 ・H 2 O + H + 由于生成的H + 和OH - 会结合生成水,所以促进醋酸铵的水解,两式相加得醋酸铵总的水解方程: Ac - + NH 4 + + H...
 弱碱阳离子与弱酸根一定不能大量共存吗?
日期:2013-03-07 10:43:29
点击:4626
好评:0
弱碱阳离子与弱酸根一定不能大量共存吗?
日期:2013-03-07 10:43:29
点击:4626
好评:0
分析:弱碱阳离子与弱酸很能不能大量共存,不能一概而论。而在中学不少资料上的离子能否共存习题中都认为:弱碱阳离子与弱酸根不能大量共存,这是错误的。如醋酸铵、碳酸氢铵等就是弱碱阳离子与弱酸根可以大量共存的例子。而有些弱碱阳离子与弱酸根互促水解程度大,甚至...
 BaS 溶解性为“―”
日期:2012-11-25 17:22:12
点击:11153
好评:0
BaS 溶解性为“―”
日期:2012-11-25 17:22:12
点击:11153
好评:0
工业制BaS 的方法是:混合重晶石粉(主要成分是BaSO4) 和煤粉(质量比为4∶1) 于1120 ℃加热一段时间, 冷却后粉碎,溶于水、除杂,蒸浓、冷却析出BaS・6H2O 晶体[ 无机化学丛书,第二卷,75 - 76 页,科学出版社 (1990) ] ,因此,不宜用“ ―”表示其溶解性。可能是因为有文献报...
 弱碱阳离子与弱酸根不能大量共存?
日期:2012-05-28 18:40:22
点击:4069
好评:0
弱碱阳离子与弱酸根不能大量共存?
日期:2012-05-28 18:40:22
点击:4069
好评:0
弱碱阳离子与弱酸很能不能大量共存,不能一概而论。而在中学不少资料上的离子能否共存习题中都认为:弱碱阳离子与弱酸根不能大量共存,这是错误的。如醋酸铵、碳酸氢铵等就是弱碱阳离子与弱酸根可以大量共存的例子。而有些弱碱阳离子与弱酸根互促水解程度大,甚至生成沉淀或...
 FeCl3溶液与Na2S溶液反应生成什么?
日期:2012-05-16 09:22:31
点击:9635
好评:1
FeCl3溶液与Na2S溶液反应生成什么?
日期:2012-05-16 09:22:31
点击:9635
好评:1
问:“在FeCl 3 溶液中加入Na 2 S溶液发生的反应有两种说法,一是: 2Fe 3+ +S 2- =2Fe 2+ +S↓; 又一为: 2Fe 3+ +3S 2- +6H 2 O=2Fe(OH) 3 ↓+3H 2 S↑ 这两种说法哪个正确? 答:一般说来,Fe 3+ 具有较强的氧化性,而S 2- 则具有还原性,因此当Fe 3+ 与S 2- 相遇时,Fe...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。