
|
学习小专题 |

|
学习小专题 |
 [探讨与扩展j] 软硬酸碱理论概述及应用 作者:化学自习室 来源:未知 日期:2025-08-26 10:04:45 点击:119 所属专题:酸碱理论
[探讨与扩展j] 软硬酸碱理论概述及应用 作者:化学自习室 来源:未知 日期:2025-08-26 10:04:45 点击:119 所属专题:酸碱理论
...
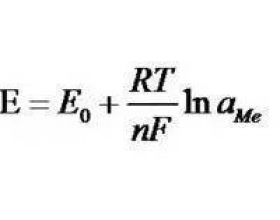 [探讨与扩展j] pH计基本原理介绍 作者:化学自习室 来源:未知 日期:2023-05-15 17:08:03 点击:706 所属专题:pH计
[探讨与扩展j] pH计基本原理介绍 作者:化学自习室 来源:未知 日期:2023-05-15 17:08:03 点击:706 所属专题:pH计
什么是PH?PH是拉丁文“Pondushydrogenii”一词的缩写(Pondus=压强、压力hydrogenium=氢),用来量度物质中氢离子的活性。这一活性直接关系到水溶液的酸性、中性和碱性。水在化学上是中性的,但不是没有离子,即使化学纯水也有微量被离解:严格地讲,只有在与水分子水合作...
 [探讨与扩展j] 如何计算酸溶液pH? 作者:化学自习室 来源:未知 日期:2022-01-03 10:42:22 点击:1289 所属专题:缓冲溶液pH计算
[探讨与扩展j] 如何计算酸溶液pH? 作者:化学自习室 来源:未知 日期:2022-01-03 10:42:22 点击:1289 所属专题:缓冲溶液pH计算
强酸溶液氢离子浓度: HCl 溶液中,完全电离,因此 [H + ]=[ Cl - ] =[H Cl ] 弱酸 溶液氢离子浓度: 醋酸 CH 3 COOH ( 经常简写做 HAc) 溶液中存在着平衡: HAc + H 2 O H 3 O + + Ac - 平衡常数表达式 : K HAc 解离平衡常数, [H 3 O + ] 、 [Ac - ] 和 [HAc] 分别...
 [探讨与扩展j] 如何计算多元弱酸溶液中的粒子浓度大小? 作者:化学自习室 来源:未知 日期:2022-01-03 11:05:46 点击:1475 所属专题:离子浓度大小比较 缓冲溶液
[探讨与扩展j] 如何计算多元弱酸溶液中的粒子浓度大小? 作者:化学自习室 来源:未知 日期:2022-01-03 11:05:46 点击:1475 所属专题:离子浓度大小比较 缓冲溶液
多元弱酸在水中是分步电离的,因此,计算时应考虑电离 / 反应程度。 向 0.10mol/L 草酸溶液中加 NaOH固体 溶液至 pH=6, 试求溶液中 H 2 C 2 O 4 、 HC 2 O 4 - 和 C 2 O 4 2- 的浓度。 已知: H 2 C 2 O 4 的 K 1 =5.4*10 -2 、 K 2 =5.4*10 -5 题目中尽管使用 K, 经验...
 [探讨与扩展j] 为什么形成原电池能加快化学反应速率? 作者:胡娟 来源:未知 日期:2021-11-10 18:18:56 点击:3096 所属专题:原电池
[探讨与扩展j] 为什么形成原电池能加快化学反应速率? 作者:胡娟 来源:未知 日期:2021-11-10 18:18:56 点击:3096 所属专题:原电池
—、问题的提出 电化学理论知识是学生在高二化学学习中遇到的难点之一,也是高考重要的考点。在实际教学过程中,演示实验里“粗锌(含少量铅、铜等不活泼杂质)和稀硫酸反应比纯锌和稀 硫酸反应制氢气速率要快很多”,这时教师就会给学生一个 结论:“粗锌中由于有杂质,杂...
 [探讨与扩展j] 酸碱理论概述 作者:化学自习室 来源:未知 日期:2021-06-17 08:06:12 点击:12422 所属专题:酸碱理论
[探讨与扩展j] 酸碱理论概述 作者:化学自习室 来源:未知 日期:2021-06-17 08:06:12 点击:12422 所属专题:酸碱理论
在中学化学阶段,我们对酸和碱有了初步的了解,但是,碳酸钠水溶液是显碱性的,它为什么不是碱呢,经过现在的深入的学习,我对酸碱理论有了初步的了解,对于酸碱 定义的理论是在不断拓展中前进的,酸碱的形式也在不断的拓展延伸着。 1 、阿伦尼乌斯酸碱理论——酸碱电离理论...
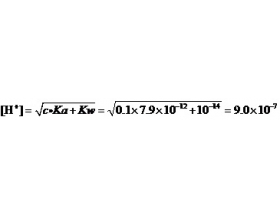 [探讨与扩展j] 判断金属离子强酸盐溶解时是否有氢氧化物沉淀产生的计算 作者:化学自习室 来源:化学原理补正博客 日期:2020-04-14 09:37:14 点击:1191 所属专题:溶度积计算 氢氧化物沉淀
[探讨与扩展j] 判断金属离子强酸盐溶解时是否有氢氧化物沉淀产生的计算 作者:化学自习室 来源:化学原理补正博客 日期:2020-04-14 09:37:14 点击:1191 所属专题:溶度积计算 氢氧化物沉淀
对一定浓度的含有某金属离子的溶液来说,判断其中是否有氢氧化物沉淀出现的方法其实是很简单的。因为根据溶度积规则,只要满足条件[M n+ ][OH - ] n ≧ K sp ,溶液中就会有M[OH] n 沉淀生成。 要注意的是,当金属离子有较强的水解趋势时,金属离子的分析浓度 c 并不...
 [探讨与扩展j] 两性离子自身间的争夺质子反应 作者:伍伟夫 来源:化学原理补正的博客 日期:2021-11-29 19:33:53 点击:12110 所属专题:自耦电离
[探讨与扩展j] 两性离子自身间的争夺质子反应 作者:伍伟夫 来源:化学原理补正的博客 日期:2021-11-29 19:33:53 点击:12110 所属专题:自耦电离
诸如HC O 3 - 、HP O 4 2 - 类的离子,在水溶液中都可以继续电离给出质子,也可以通过水解来结合质子而产生氢氧根离子。或表现为既能与碱反应,又能与酸反应。故都可以将它们称为两性离子。 对所有两性离子来说,除上述人们熟知的电离和水解这两个性质外,还有一个经...
 [探讨与扩展j] 缓冲溶液解读 作者:化学自习室 来源:未知 日期:2019-11-15 10:58:19 点击:2403 所属专题:缓冲溶液
[探讨与扩展j] 缓冲溶液解读 作者:化学自习室 来源:未知 日期:2019-11-15 10:58:19 点击:2403 所属专题:缓冲溶液
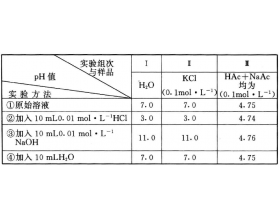
例 :取纯水、KCl溶液、HAc与NaAc的混合液各 90 mL 进行实验,实验做法和结果见下表。 问:(1)从实验结果可得出什么结论? (2) 试解释第I组实验的实验结果? (3) 试推测哪类溶液可具有第I组溶液的性质? [解析](1)实验结果表明,加入少量酸或碱后,纯水和KCl 溶液的pH值发生...
 [探讨与扩展j] 强电解质有无“强”、“弱”之分? 作者:化学自习室 来源:未知 日期:2019-11-11 16:49:07 点击:754 所属专题:弱电解质
[探讨与扩展j] 强电解质有无“强”、“弱”之分? 作者:化学自习室 来源:未知 日期:2019-11-11 16:49:07 点击:754 所属专题:弱电解质
高中化学教材指出“HClO 4 是已知酸中最强的一种酸”,这表 明不同的强电解质仍有强度的差别。从酸分子结构的分析确实可以得出这个结论。 但是为什么这些强酸在水溶液中都几乎完全电 离呢?这是因为按照酸喊的质子理论,和HClO 4 、HNO 3 、HX等 强酸的共轭碱Cl O 4 - 、N...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。...
什么是PH?PH是拉丁文“Pondushydrogenii”一词的缩写(Pondus=压强、压力hydrogenium=...
一、水的离子积计算 水的离子积( K w )是一个使用频率较高的化学数据。而一个电极反应...
多元弱酸在水中是分步电离的,因此,计算时应考虑电离 / 反应程度。 向 0.10mol/L 草...
强酸溶液氢离子浓度: HCl 溶液中,完全电离,因此 [H + ]=[ Cl - ] =[H Cl ] 弱酸 溶...
我们接触到的溶剂大部分是水,因而把能够在电离产生水中阳离子(H 3 O + )的物质叫...
碳酸氢钠能和氯化钙反应的道理可以用碳酸氢根离子的“自偶”电离来解释以上现象;碳酸...
有关自偶电离特别是非水溶剂中自偶电离的试题不断涌现,逐渐成为了各类考试特别是高中...