
|
学习小专题 |

|
学习小专题 |
 [注解与辨疑6] 说说铜的冶炼 作者:化学自习室 来源:未知 日期:2020-04-02 16:46:55 点击:2167 所属专题:铜的冶炼
[注解与辨疑6] 说说铜的冶炼 作者:化学自习室 来源:未知 日期:2020-04-02 16:46:55 点击:2167 所属专题:铜的冶炼
目前世界上生产电解铜的冶炼方法主要分为两大类:火法冶炼和湿法冶炼。湿法炼铜源于我国,古称“胆水浸铜法”,我国西汉时的炼丹家刘安所著的《淮南万毕术》中就有记载“曾青得铁,则化为铜”。 目前精炼铜产量的80%以上是用火法冶炼生产的,湿法冶炼生产的精炼铜占20%左...
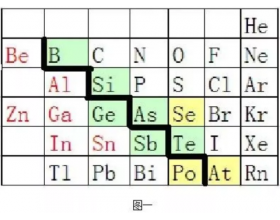 [注解与辨疑6] 如何理解化学中的“两性”概念 作者:化学自习室 来源:未知 日期:2020-02-16 13:13:09 点击:4242 所属专题:两性物质
[注解与辨疑6] 如何理解化学中的“两性”概念 作者:化学自习室 来源:未知 日期:2020-02-16 13:13:09 点击:4242 所属专题:两性物质
出于从化学性质角度来对化学物质进行归类的需要,人们引入了两性物质的概念。从字面上看,“两性”就是某物质同时具有两种相对立性质的意思,与“双性”有类似的含义。 但在化学上这种相互对立的性质有很多,如酸性与碱性、氧化性与还原性、金属性与非金属性。加之,人们有...
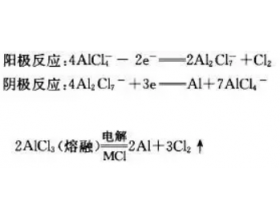 [注解与辨疑6] 有关铝的一些问题集 作者:化学自习室 来源:未知 日期:2020-01-30 14:51:10 点击:1331 所属专题:金属铝 铝的冶炼
[注解与辨疑6] 有关铝的一些问题集 作者:化学自习室 来源:未知 日期:2020-01-30 14:51:10 点击:1331 所属专题:金属铝 铝的冶炼
一、有关铝的制备 目前工业上大多数是用拜耳法生产氧化铝,拜耳法系奥地利拜耳(K.J.Bayer)于 1888年发明。其原理是用苛性钠(NaOH)溶液加温溶出铝土矿中的氧化铝,得到铝酸钠溶液。溶液与残渣(赤泥)分离后,降低温度,加入氢氧化铝作晶种,经长时间搅拌,铝酸钠分解析出氢氧...
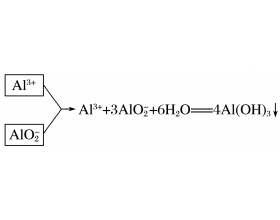 [注解与辨疑6] 氢氧化铝的三种制备方法 作者:化学自习室 来源:未知 日期:2019-12-25 09:39:49 点击:16213 所属专题:氢氧化铝
[注解与辨疑6] 氢氧化铝的三种制备方法 作者:化学自习室 来源:未知 日期:2019-12-25 09:39:49 点击:16213 所属专题:氢氧化铝
一、知识梳理 方法一:可溶性铝盐溶液与过量氨水反应 反应原理: Al 3 + + 3NH 3 ·H 2 O == =Al(OH) 3 ↓ + 3NH4+ 方法二:向可溶性偏铝酸盐溶液中通入过量 CO 2 反应原理: AlO2- + 2H 2 O + CO 2 == =Al(OH) 3 ↓ + HCO3- 方法三:相互促进水解法 二、应用与训练...
 [注解与辨疑6] 铁及其化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:40:48 点击:1054 所属专题:铁及其化合物 是非判断
[注解与辨疑6] 铁及其化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:40:48 点击:1054 所属专题:铁及其化合物 是非判断
一、正误判断 1.(2018·江苏)Cu与FeCl 3 溶液反应可生成CuCl 2 。( ) 2.(2015·广东)向FeSO 4 溶液中先滴入KSCN溶液再滴加H 2 O 2 溶液,加入H 2 O 2 后溶液变成血红色,说明Fe 2+ 既有氧化性又有还原性。( ) 3.(2015·全国卷Ⅰ)将稀硝酸加入过量铁粉中,充分反应后滴加...
 [注解与辨疑6] 镁铝化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:33:37 点击:1156 所属专题:铝及其化合物 是非判断
[注解与辨疑6] 镁铝化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:33:37 点击:1156 所属专题:铝及其化合物 是非判断
一、正误判断 1.(2017·全国卷Ⅱ)向2 mL 0.1 mol·L -1 的FeCl 3 溶液中加足量铁粉,振荡,加1滴KSCN溶液,现象为黄色逐渐消失,加KSCN溶液颜色不变,则还原性:Fe>Fe 2+ 。( ) 2.(2018·全国卷Ⅱ)向盛有2 mL 黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化...
 [注解与辨疑6] 铜及其化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:22:06 点击:757 所属专题:铜及其化合物 是非判断
[注解与辨疑6] 铜及其化合物是非判断 作者:化学自习室 来源:未知 日期:2019-11-14 19:22:06 点击:757 所属专题:铜及其化合物 是非判断
一、正误判断 1. (2017·全国卷Ⅲ)除去溶液中的Cl - ,可向溶液中同时加入Cu和CuSO 4 ,生成CuCl沉淀从而除去Cl - 。除Cl - 的反应为Cu+Cu 2+ +2Cl - ===2CuCl。( ) 2. 加热条件下氨可被CuO氧化成一种气体单质,该反应的化学方程式为3CuO+2NH 3 ==3Cu+N 2 +3H 2...
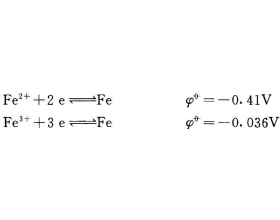 [注解与辨疑6] 如何理解Fe2+离子和Fe3+离子的稳定性及其相互转化? 作者:化学自习室 来源:未知 日期:2021-12-28 08:46:50 点击:4445 所属专题:铁三角
[注解与辨疑6] 如何理解Fe2+离子和Fe3+离子的稳定性及其相互转化? 作者:化学自习室 来源:未知 日期:2021-12-28 08:46:50 点击:4445 所属专题:铁三角
铁原子具有3d 6 4s 2 的价电子层结构,在化学反应中,铁原子 最外层上的4S电子首先失去,使铁呈+2价。由于半充满的D电 子层结构比较稳定,因此铁原子里6个3d电子中的1个电子也比较容易失去,于是铁也可呈现+ 3价。在一定条件下,铁还能呈+ 6价。 由上列电极电位可知...
 [注解与辨疑6] +1价铜与+2价铜相互转化关系分析 作者:化学自习室 来源:未知 日期:2019-11-13 08:42:35 点击:4797 所属专题:铜及其化合物
[注解与辨疑6] +1价铜与+2价铜相互转化关系分析 作者:化学自习室 来源:未知 日期:2019-11-13 08:42:35 点击:4797 所属专题:铜及其化合物
铜的外围电子构型是3d 10 4s 1 ,但具有变价。这是因为铜原子 中3d轨道上的电子和4s轨道上的电子,在能量上差别不大(相差 约1. 11. 4 KJ mol -1 ),故在通常条件下,铜不但可失去4s轨道 上1个电子,而且还可再失去3d轨道上的电子,因此具有可变化合价。铜有+1价、+2价和...
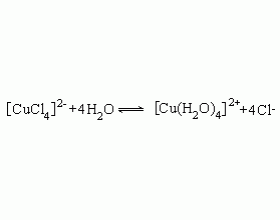 [注解与辨疑6] 为啥氯化铜溶液与硫酸铜溶液颜色不同? 作者:化学自习室 来源:未知 日期:2019-09-12 15:07:21 点击:4203 所属专题:氯化铜 硫酸铜
[注解与辨疑6] 为啥氯化铜溶液与硫酸铜溶液颜色不同? 作者:化学自习室 来源:未知 日期:2019-09-12 15:07:21 点击:4203 所属专题:氯化铜 硫酸铜
硫酸铜溶液显蓝色,氯化铜溶液为绿色。为什么同为铜盐,但颜色不同?如果仅仅用酸根离子不同作理由来解释,是不足以服人的。要透彻解释应该从 Cu 2+ 的络离子说起。 Cu 2+ 有配位数 2 、 4 、 6 的络离子。在胆矾 CuSO 4 · 5H 2 O 中,四个水分子以平行四边形配位在C...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
铜的化合物有硫酸铜(CuSO 4 )、醋酸铜[(CH 3 COO) 2 Cu]、氧化铜(CuO...
你是否还记得中学课本里的分类:碱性氧化物是能与酸反应生成...
...
一、建立轴线:形态随pH切换 中间: Al(OH) 3 (沉淀态) 左侧(强酸...
钛(化学符号 Ti,原子序数 22)是一种具有优异综合性能的过渡...
就高考备考中,尤其关于镁的知识给同学们列出以下复习提纲:...
关于亚铁离子与铁氰化钾的反应,简单来说,其核心产物是一种...
新型合金是指通过成分优化、微观结构调控、制备工艺创新形成...