
|
学习小专题 |

|
学习小专题 |
 [方法与规律1] 物质的量浓度计算方法 作者:胡长胜 来源:未知 日期:2018-07-13 10:45:21 点击:14234 所属专题:物质的量浓度计算 化学计算方法
[方法与规律1] 物质的量浓度计算方法 作者:胡长胜 来源:未知 日期:2018-07-13 10:45:21 点击:14234 所属专题:物质的量浓度计算 化学计算方法
物质的量浓度的计算是中学化学计算的重要组成部分,是近年各类考试的 “ 热点 ” ,此类题涉及的概念较多(如物质的量、质量、摩尔质量、气体的摩尔体积等),知识范围广,内容灵活多变。解题过程中,不少同学感到无所适从。其中最主要的原因是不知道解选择解题的思维起...
 [方法与规律1] 阿伏伽德罗常数问题的十种错误类型 作者:王兵 来源:未知 日期:2014-01-11 17:42:55 点击:3597 所属专题:阿伏伽德罗常数
[方法与规律1] 阿伏伽德罗常数问题的十种错误类型 作者:王兵 来源:未知 日期:2014-01-11 17:42:55 点击:3597 所属专题:阿伏伽德罗常数
一、阿伏伽德罗常数问题的十种错误类型 1 、没有用准分子、原子、离子等微粒的概念 例如: 1.00molNaCl 中含有 N A 个 NaCl 分子 分析: NaCl 是离子化合物,不存在分子。 2 、没有注意物质的状态 例如:标准状况下, 22 . 4LCHCl 3 中含有的氯原子数目为 3N A 分析:标准...
 [方法与规律1] 质量分数不等的两种溶液等质量或等体积混合后的浓度分析 作者:汪峰 来源:未知 日期:2013-07-09 08:59:27 点击:7184 所属专题:溶液混合
[方法与规律1] 质量分数不等的两种溶液等质量或等体积混合后的浓度分析 作者:汪峰 来源:未知 日期:2013-07-09 08:59:27 点击:7184 所属专题:溶液混合
原题: 质量分数不等的两种硫酸溶液等质量混合时,其质量分数为a%;而等体积混合时,质量分数为b%。质量分数不等地两种乙醇溶液等质量混合时,其质量分数为a%;而等体积混合时,质量分数为c%。则a、b、c、的大小关系是(B) A.abc B.bac C.cab D.acb 解析: 假设两种溶液的质...
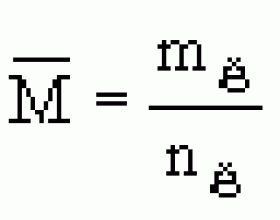 [方法与规律1] 气体平均相对分子质量的计算 作者:樊会武 来源:未知 日期:2018-08-13 11:34:33 点击:17348 所属专题:平均摩尔质量
[方法与规律1] 气体平均相对分子质量的计算 作者:樊会武 来源:未知 日期:2018-08-13 11:34:33 点击:17348 所属专题:平均摩尔质量
平均相对分子质量适用于混合物,常用于混合气体。平均相对分子质量相当于把混合物看作一个“单一组分”,这一“单一组分”的相对分子质量就是平均相对分子质量。相对分子质量求法与平均摩尔质量相同,只是单位不同而已,平均摩尔质量有几种计算方法: 1、已知混合气体的...
 [方法与规律1] 溶液稀释问题解析 作者:栾凯 来源:未知 日期:2013-03-07 16:07:42 点击:9156 所属专题:溶液稀释
[方法与规律1] 溶液稀释问题解析 作者:栾凯 来源:未知 日期:2013-03-07 16:07:42 点击:9156 所属专题:溶液稀释
有学生问起溶液稀释的计算型选择题有没有估算法,特分析如下,希望对这些同学有些帮助。但是涉及酒精与氨水的稀释时必须注意,在一般情况下,溶液的浓度越大,其密度越...
 [方法与规律1] 非标准状况气体体积的简算 作者:黄增春 来源:未知 日期:2016-01-17 10:57:12 点击:5671 所属专题:气体体积计算
[方法与规律1] 非标准状况气体体积的简算 作者:黄增春 来源:未知 日期:2016-01-17 10:57:12 点击:5671 所属专题:气体体积计算
非标准状况的气体体积计算似乎非用公式PV=nRT不可,其实是可以回避且能使计算得到简化的。 【例 1】 在273℃和1.01×105Pa条件下,将1.40g氮气、1.60g氧气和4.00g氩气混合,该气体的体积是[ ]。(1989年全国高考题) A.3.36L B.6.72L C.8.96L D.4.48L 解析: 本题...
 [方法与规律1] NA相关计算的常设陷阱 作者:邱东兰 来源:未知 日期:2016-01-17 14:57:52 点击:13984 所属专题:阿伏伽德罗常数
[方法与规律1] NA相关计算的常设陷阱 作者:邱东兰 来源:未知 日期:2016-01-17 14:57:52 点击:13984 所属专题:阿伏伽德罗常数
关于 N A 的计算与推断在历年高考化学试题多以选择题出现,解题方法与思路一般抓住基本概念,将物质的质量、气体的体积、溶液的浓度等物理量与指定粒子的物质的量进行换算,审题时关键注意以下易错点: 1 、 状况条件 :考查气体时,一定要特别关注是标准状况下还是非标...
 [方法与规律1] 硫酸稀释、混合计算小结 作者:程新 来源:未知 日期:2012-04-09 20:01:17 点击:15607 所属专题:溶液稀释 溶液混合
[方法与规律1] 硫酸稀释、混合计算小结 作者:程新 来源:未知 日期:2012-04-09 20:01:17 点击:15607 所属专题:溶液稀释 溶液混合
一、稀释前后质量分数与物质的量浓度之间的关系 例 1 、将质量分数为 2 、物质的量浓度为 c 1 的硫酸溶液加水稀释,使质量分数变为 ,物质的量浓度变为 c 2 ,则 c 1 与 c 2 的关系( ) A 、 c 1 = 2c 2 B 、 c 1 2c 2 C 、 c 1 2c 2 D 、 c 2 = 2c 1 解析 : 此题可用质量...
 [方法与规律1] 公式c=1000ρω/ M的推导及应用 作者:曹启凤 来源:未知 日期:2012-04-09 10:55:31 点击:16984 所属专题:物质的量浓度计算 浓度换算
[方法与规律1] 公式c=1000ρω/ M的推导及应用 作者:曹启凤 来源:未知 日期:2012-04-09 10:55:31 点击:16984 所属专题:物质的量浓度计算 浓度换算
一、推导 下面先通过一道题目的解析来获得推导结果。 题目:实验室常用的 98 % 的浓硫酸,其密度为 1.84g /mL ,计算浓硫酸的物质的量浓度。 解法 1 :设浓硫酸的体积为 1L , 1L 溶液中含有溶质 H 2 SO 4 的物质的量为: 则浓 H 2 SO 4 的物质的量浓度为: c(H 2 SO 4 ) =...
 [方法与规律1] 平均摩尔质量 作者:周书峰 来源:未知 日期:2018-08-13 11:35:35 点击:11905 所属专题:平均摩尔质量
[方法与规律1] 平均摩尔质量 作者:周书峰 来源:未知 日期:2018-08-13 11:35:35 点击:11905 所属专题:平均摩尔质量
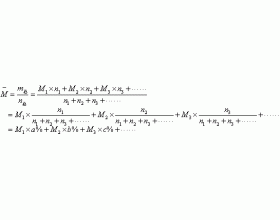
我们常常把每摩尔混合物的质量称为该混合物的 平均摩尔质量 。当它的单位为g/mol时,我们把它的数值叫做混合物的平均相对分子质量。根据定义可知:混合物的总质量除以混合物总物质的量即为 混合物 的 平均摩尔质量 。根据定义可得出适用于任何状态的下式: 式中: M x ...
 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。化学式子要配平,必须纯量代方程, 单位上下要统一,左右倍数要相等。 质量单位若用克...
1.化学方程式不正确就计算,这是最严重的问题. 2.把含杂质的质量直接应用在化学方程式...
有关阿伏伽德罗常数(N A )的计算是高考化学命题的一大热点,让考生对有关阿伏伽德罗...
一、高考定位 通过分析近几年的全国卷真题可知,该类试题多是通过阿伏加德罗常数将化...
角度一 常在气体摩尔体积的适用条件及物质的状态上设题 典 型 示 例 判 断 正 误 (1)...
物质的量浓度、质量分数、密度、体积大小类习题在高考题中出现的频率很高,这类题主要...
我们常常把每摩尔混合物的质量称为该混合物的 平均摩尔质量 。当它的单位为g/mol时,...
平均相对分子质量适用于混合物,常用于混合气体。平均相对分子质量相当于把混合物看作...