
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
【问题】如何检验阿司匹林中的酯基?
结构分析:阿司匹林分子中同时含有羧基和酯基。
检验的思维逻辑链:水解→酸化或碱化→显色。
阿司匹林(无酚羟基,不显色)→酸或碱水解→水杨酸(有酚羟基)→与FeCl₃显紫色。通过水解前后的显色变化,证明酯基的存在。
方法一:酸性水解路径
人教版选择性必修2教材是这样检验的:取阿司匹林溶液于试管中,加入2滴稀硫酸,加热后滴入几滴NaHCO3溶液,振荡。再向其中滴入几滴FeCl3溶液,振荡。观察现象。
加入NaHCO3溶液的目的?人教版教材解释:加入NaHCO3是为了中和过量的硫酸。
至于为什么要中和过量的酸,没有深入说明。
如果不加入NaHCO₃,在强酸性条件下,FeCl₃难与水杨酸(水解产物)生成特征性的紫色络合物,导致检验失败。
为什么强酸性体系会抑制显色?
水杨酸与FeCl3溶液反应显紫色的原因:
酚氧离子(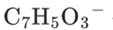 )和Fe3+形成配位键,形成显紫色的物质。
)和Fe3+形成配位键,形成显紫色的物质。
强酸性下,酚羟基的电离被强烈抑制(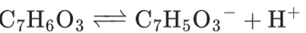 平衡左移),导致能与Fe³⁺配位的酚氧离子(
平衡左移),导致能与Fe³⁺配位的酚氧离子(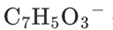 )浓度极低,无法形成稳定的紫色螯合物。
)浓度极低,无法形成稳定的紫色螯合物。
有老师曾做实验:水杨酸中滴加FeCl3溶液显紫色(不如苯酚的紫色明显),再逐滴加入稀盐酸,紫色逐渐褪去(颜色接近FeCl3溶液),再继续滴加NaHCO₃溶液,剧烈反应,产生气泡,紫色逐渐恢复。
实验证据表明,酸性强时,酚羟基不易与Fe³⁺络合。
方法二:碱性水解路径
其步骤为:阿司匹林溶液中加入NaOH溶液加热水解→冷却后用稀盐酸充分酸化至明显酸性(可用pH试纸测试)→滴加FeCl₃溶液观察紫色。
注意:酸化必须充分,否则残留的OH⁻会与Fe³⁺生成红棕色Fe(OH)₃沉淀,掩盖紫色。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
《选必3》课本P 69 1.试管要洁净,否则单质银不易附着在试管内...
一、三氯化铁与酚羟基显色 三氯化铁(FeCl₃)与酚羟基(—O...
【问题】如何检验阿司匹林中的酯基? 结构分析:阿司匹林分子...
其实,你被表面现象骗了。教科书对乙酸乙酯在水中的溶解性语...
苯酚的酸性极弱, 苯酚钠 在水溶液中会发生水解,溶液呈碱性...
一、乙醇的结构 首先,和水(H-OH)相比,乙醇(CHCH-OH)分子中的...