
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
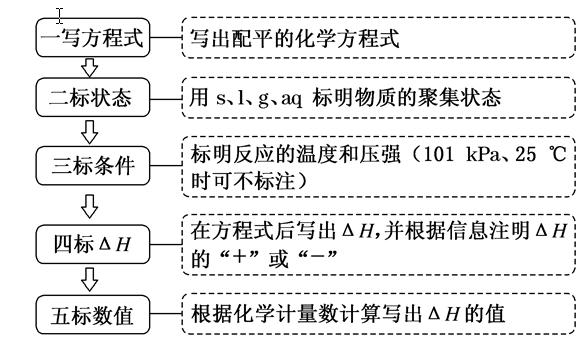
注意1、热化学方程式与普通方程式中的计量数是有区别的,热化学方程式的计量数可以是分数。
注意2、由于物质的能量与物质的状态相关,所以在热化学方程式中,必须用符号标出物质的聚集态。
s、l、g、aq四种符号分别表示固、液、气、溶液四种状态。注意l表示是纯净物,aq表示是混合物。聚集态不同,能量大小不一样。气态水的能量高于液态水。
注意3、物质的能量还与物质存在的温度与压强大小有关。
如液体水(l),60℃与0℃的水能量是不同的,60℃烫手,0℃冻手;实际上用四个量,温度、压强、聚集态、物质的量才能表示物质能量状态的。聚集态也不完全等同于固、气、液,同样是铁,块状与粉末状、纳米颗粒大小的铁的能量不一样。相同的条件,相同物质,物质的量越多能量越多。
热化学方程式一般不写反应条件,一是因为反应热的大小只与反应物、生成物的状态有关,与反应条件无关,二是因为反应热的数据无特别说明,都是在1大气压,25C时条件下测定的数据。
注意4、热化学方程式中的焓变是带加(+)减(-)符号的。
注意这里的“+”读作加号,是指体系(包括反应物与生成物)从环境中吸收了能量,反应体系的能量增加了,“-”读减号,是指反应放出能量,体系的能量减少了。
注意5、注意反应热的单位kJ/mol中/mol的含义。
我们知道使用mol作单位时,必须指明粒子的种数类。如1mol H2O。热化学方程式中的/mol对应的粒子集合体,是化学方程式中包含的所有粒子。如热化学方程式H2(g)+1/2O2(g)=H2O(l) Δ=-285.8kJ/mol中/mol,就是指/mol(H2(g)+1/2O2(g)=H2O(l))。热化学方程式2H(g)+O2(g)=2H2O(l) Δ=-2×285.8kJ·mol其中/mol指/mol(2H2(g)+ O2(g)=2HO(l)),这样同学们就明白,虽然都是1mol,但1mol(2H2(g)+ O2(g)=2H2O(l))的粒子数,是1mol(H2(g)+1/2O2(g)=H2O(l))中粒子数的两倍,当然放出的热量也应是两倍。
注意6、可逆反应,正反应的反应热与逆反应数值相等,但符号相反应。虽是可逆反应,但对应反应热的数值却是反应物完全转化为生成物的数值。同学们务必记住这一点。明白反应热与热效应是有区别的。反应热有符号,热效应只有数值,没有符号区别。

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
1、2025 陕甘青宁 高温下MgCO 3 分解产生的MgO催化CO 2 与H 2 反应生...
1.基元反应 一个化学反应往往需要经过多个反应步骤才能实现...
一、热化学方程式的书写 与普通化学方程式相比,书写热化学方...
2017年高考化学考试说明中特别增加了一条:了解反应活化能的概...
方法技巧 解答能量变化图像题需要注意的几点。 (1)反应热不能...
对于“环式”反应过程图像可表示为: (1)位于“环上”的物质一...