
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在“键的极性对化学性质的影响”一节中,高中阶段将会学习诱导效应对羧基的羟基的极性的影响。但所学知识相对简单:
即:拉电子集团使羟基的极性增强,从而使羧酸的酸性增强。
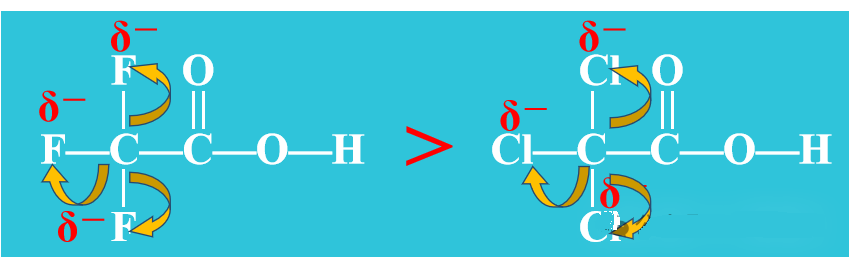
推电子集团使羟基的极性减弱,从而使羧酸的酸性减弱。
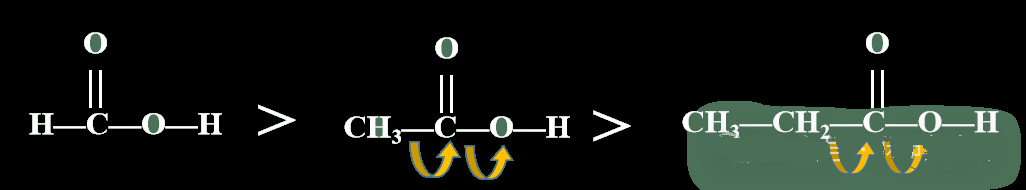
但是在解决以下题目时,依然存在困惑:
下列物质中酸性最强的是( )
A.碳酸 B.乙酸 C.丁酸 D.戊酸
由于烃基为推电子集团,因此烃基链越短,酸性越强。学生将目光停留在碳酸和乙酸上。两者在结构上的差异如下图所示:
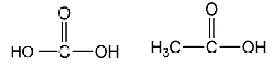
问题就改为探讨羟基和甲基对羧基的羟基的极性的影响。
部分学生认为:氧原子的电负性大于碳原子,因此充当了拉电子集团,酸性应该强。也有部分学生举出了鸡蛋壳和醋酸的反应,根据强酸制弱酸的原理,醋酸的酸性应该大于碳酸。
实验结果不会出错,那就应该是解释的时候出了差错。
简单运用一下有机化学中的知识。
在有机化学中:电子效应可以分为两类:诱导效应(根据电负性判断);共轭效应(σ-π的共轭,p-π的共轭等效应)
为了更加正确解释结果,笔者搜了一些文献,现将文献中结论呈现一下。
碳酸与乙酸比较
1.从诱导效应看,碳酸中与羧基相连的羟基也具有负诱导效应,而且比甲基的负诱导效应还强,使碳酸分子中的电子云发生如下的偏移:
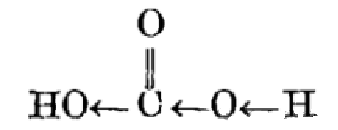
2.从共轭效应,羟基氧原子上的未共用电子对与羰基的π键发生p-π共轭,使得羟基氧原子上的未共用P电子向π键移动:
3.碳酸分子中的诱导效应与共轭效应也同时共存,方向相反,大小不等。但共轭效应大于诱导效应,使得碳酸的酸性也比甲酸弱。
以上来自于:张振华《也谈碳酸与甲酸的酸性强弱》

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
今天整理完整版氢键核心笔记,概念、形成、分类、性质影响一...
提到化学,我们最先想到的往往是化学键断裂与重组的化学反应...
一、概念与本质类易错点 •易错1:混淆氢键与化学键——氢键...
高中化学物质结构板块里,配位键和配位化合物一直是高频考点...
...
...