
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
在一定温度下的饱和溶液中,溶质、溶剂、溶液间有一定量的关系。由此可进行以下计算:
(1)根据饱和溶液溶质、溶剂的量推算溶解度;
(2)根据溶解度求算饱和溶液所含的溶剂和溶质量;
(3)根据溶解度求算饱和溶液在蒸发掉一定量溶剂后析出的结晶量;
(4)由于物质在不同温度下溶解度不同,可以根据不同温度下的溶解度求算出一定量饱和溶液由于温度改变(或同时有溶剂量改变),析出结晶的量。
(5)饱和溶液中溶解度与溶质的质量分数的换算。
一定温度下,某饱和溶液溶质的溶解度:
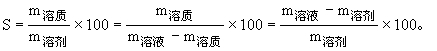
解题时要熟练运用下列比列关系:饱和溶液中

练习:
1.t℃时,Na2CO3的溶解度为Ag,现有饱和Na2CO3溶液(100+A)g,其溶质的质量分数为a%,向溶液中投入无水Na2CO3固体Ag,静置后析出少量晶体(Na2CO3·10H2O),加水使晶体全部溶解,所得溶液仍为饱和溶液,加入的水是 ( )
A.100g B.(100+A)g
![]()
2.有X、Y、Z三种盐,已知:
(1)25℃时,X饱和溶液其溶质质量分数为15%;
(2)25℃时,在100g质量分数为10%的Y溶液中加入5gY(无水盐)后,恰好达到饱和;
(3)25℃时,将一定量Z溶液蒸发掉5.75g水再恢复到25℃,或保持在25℃向其中加入6.3gZ的结晶水合物(Z·9H2O,摩尔质量=240),都恰好形成饱和溶液。
则25℃时,X、Y、Z的溶解度(指无水盐)大小顺序正确的是 [ ]
A.X>Y>Z B.Z>Y>X C.Y>Z>X D.Z>X>Y
3.取50mL2mol/L的硫酸溶液,跟6.5g金属锌充分反应,加热蒸发16.2g水,并冷却至10℃时,可析出ZnSO4·7H2O多少克(10℃时ZnSO4溶解度为32g,硫酸密度1.12g/cm3)?
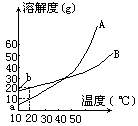
4.A、B两种化合物的溶解度曲线如下图所示,现要用结晶法从A、B混合物中提取A(不考虑A、B共存时,对各自溶解度的影响)
(1)取50g混合物,将它溶于100g热水,然后冷却至20℃。若要使A析出而B不析出,则混合物中B的质量分数(B%)最高不能超过多少?(写出推理及计算过程)
(2)取Wg混合物,将它溶于100g热水,然后冷却至10℃。若仍要使A析出而B不析出,请写出在下列两种情况下,混合物中A的质量分数(A%)应满足什么关系式?(以W、a、b表示,只需将答案填写在下列横线的空白处。)
当w<a+b时____
当w>a+b时____
参考答案
1.A;2.D;3.15.5g;
4.(1)在20℃时,若要B不析出,该溶液中B的质量不能超过20g,由于A、B质量共50g,所以这时A的质量超过30g,大于它的溶解度,A析出,符合题意。即50g×B%≤20g,B%≤40%。
2)当W<a+b时,A%>a/w;当W>a+b时,A%≥W-b/W;

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。
 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。
陷阱1、物质的状态。 命题中常涉及物质的体积,需考虑是否为...
类型一关于气体的摩尔体积 解题策略:有体积,无标况或非气态...
化学式子要配平,必须纯量代方程, 单位上下要统一,左右倍数...
1.化学方程式不正确就计算,这是最严重的问题. 2.把含杂质的质量...
有关阿伏伽德罗常数(N A )的计算是高考化学命题的一大热点,...
一、高考定位 通过分析近几年的全国卷真题可知,该类试题多是...