
|
学习小专题 |

|
学习小专题 |
版权申明:凡是署名为“化学自习室”,意味着未能联系到原作者,请原作者看到后与我联系(邮箱:79248376@qq.com)!
只要知道各元素的正化合价,便可用原酸脱水的规律确定该元素的氧化物的水化物是酸(几元酸)、是碱(几元碱),可以准确地写出酸、碱的分子式。其规则是“偶余2来奇余3,余3再减成偏酸;氮铋特殊不加偏,卤锰特称高某酸”。任何元素只要知道其正价,均可写成原酸式,即R(OH)x,原酸式中,x如果是偶数,则H原子为偶数,则脱掉水分子后余下2个H原子;x如果是奇数,则脱掉水分子后余下3个H原子,余下3个H原子之后,还可以再脱水,形成偏酸,只有三元酸才能进一步脱水形成偏酸。氮铋元素均为+5价,余3个H原子,形成三元酸,还可以再脱去1个水分子形成一元酸,不称偏某酸,称硝酸和铋酸。卤、锰元素的最高价均为+7价,x为奇数,余3个H原子,形成三元酸,还可脱去1个水分子,形成一元酸,不称作偏某酸,而称作高某酸。如果x为2或1时,则原酸式不能脱水。不能脱水为碱,所以碱均为一元碱或二元碱,举例说明如下:
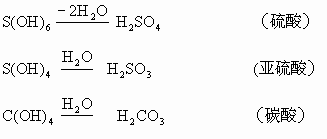
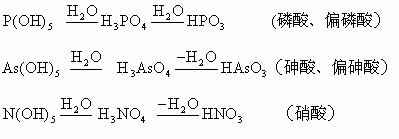
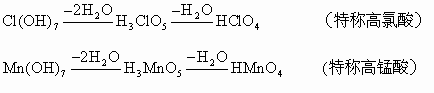
![]()

 欢迎订阅网站动态,手机扫一扫就可以。
欢迎订阅网站动态,手机扫一扫就可以。 欢迎使用化学自习室APP,扫码就可下载。
欢迎使用化学自习室APP,扫码就可下载。【定义】又称离子有效半径,是通过实验测定的。一般认为的离子半径是:离子晶体中相邻...
关于117号元素是金属元素还是非金属元素的讨论以下几种意见: 1、非金属元素 虽然根据...
氢是元素周期表中的第一号元素,元素名来源于希腊文,原意是水素。氢是由英国化学家卡...
在我们身边的物质世界中,有气体,有液体,也有固体。他们都是由许许多多的肉眼看不见...
...
碳位于第二周期ⅣA,氮位于第二周期VA,根据同周期元素气态氢化物的稳定性从左到右依...